
- •Свойства тройной с≡с связи
- •1.2. Гомологический ряд алкинов
- •1.3. Номенклатура алкинов
- •1.4. Изомерия
- •2. Способы получения алкинов
- •3. Свойства алкинов
- •3.1. Физические свойства
- •3.2. Общая характеристика химических свойств
- •3.3. Основные химические реакции
- •1) Реакции присоединения.
- •2) Реакции замещения
- •3) Реакции полимеризации
- •4) Реакции конденсации
- •5) Реакция окисления
- •4. Экологические аспекты химии алкинов
- •5. Вопросы и задачи по теме «алкины»
- •Литература
3. Свойства алкинов
3.1. Физические свойства
Температуры кипения, плавления алкинов обычно несколько ниже, чем у соответствующих алкенов и алканов. Ацетилен, метилацетилен – газы. Гомологи до С16 – жидкости, выше - твердые вещества. Все соединения бесцветны, нерастворимы в воде, растворяются в органических растворителях.
3.2. Общая характеристика химических свойств
Химические свойства алкинов обусловлены наличием тройной связи и подвижного (кислого) атома водорода, связанного с углеродом в sp-гибридизации. Алкины вступают в реакции электрофильного и, реже, нуклеофильного присоединения, а также в реакции замещения кислого атома водорода.
Кислые свойства ацетиленовых углеводородов невелики по сравнению с минеральными кислотами, но их кислотность в 1018 раз больше, чем кислотность водорода в алканах:
-
Соединение
Константа диссоциации Ка
Н2О
10-16
НССН
10-22
СН3 –СН3
10-40
Причиной кислых свойств ацетилена является сильная поляризация связи С-Н благодаря тому, что в sp гибридной форме углеродный атом (ядро) значительно сильнее удерживает электроны, чем в sp2- и sp3-гибридизации.
Кроме того, для алкинов возможны реакции полимеризации, изомеризации и окисления.
3.3. Основные химические реакции
1) Реакции присоединения.
Тройная связь по реакционной способности не превосходит по активности двойную связь. Реакции присоединения, характерные для кратных связей, в случае тройной связи происходят в две ступени.
Присоединения водорода (реакция гидрирования)
Водород в момент выделения не взаимодействует с тройной связью, так же как и с двойной связью, но газообразный водород в присутствии катализатора восстанавливает алкины до алканов:
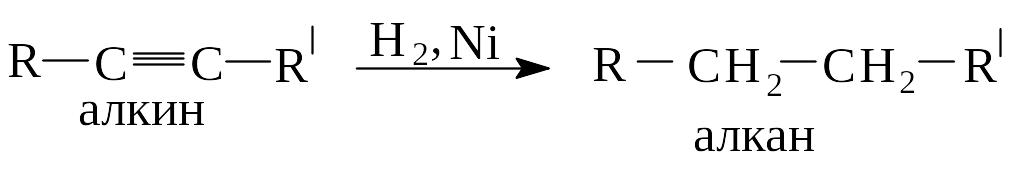
Можно восстановить алкин до алкена, если использовать менее активный катализатор (Pd, «отравленный» PbCO3, железо Ренея), при этом получаются цис-алкены. При восстановлении алкинов Na, Li в NH3 получают транс-алкены.
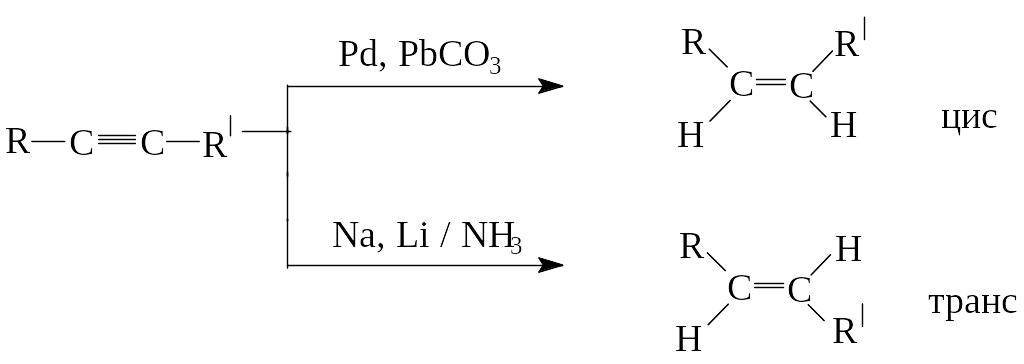
Присоединение галогенов
Реакция протекает в две стадии. Реакция с Br2 является качественной на двойную и тройную связь. Энергично протекает первая стадия, на которой могут образовываться цис- и транс-изомеры.
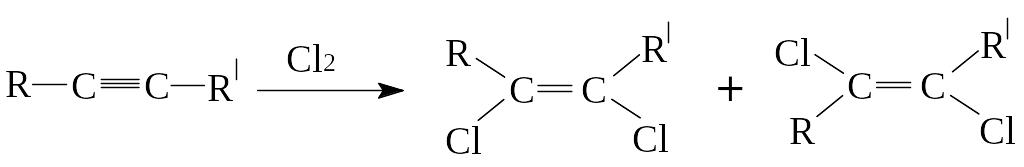
Скорость реакций гагогенирования уменьшается в ряду галогенов: Cl2, Br2, J2.
Присоединение галогеноводородов
Реакция идет в две стадии по правилу Марковникова:
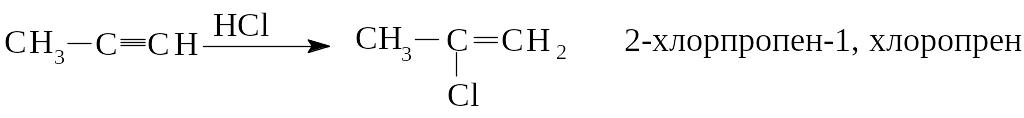
![]()
Это один из способов промышленного получения хлористого винила. Вторая молекула галогеноводорода присоединяется в соответствии с правилом Марковникова.
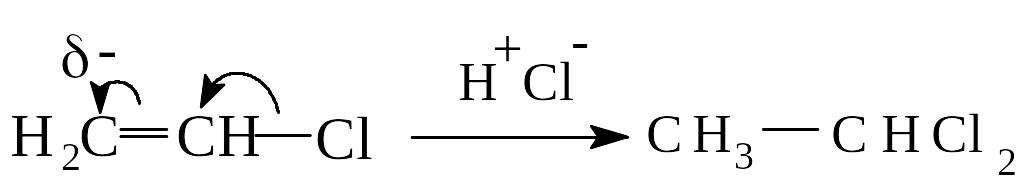
Присоединение воды
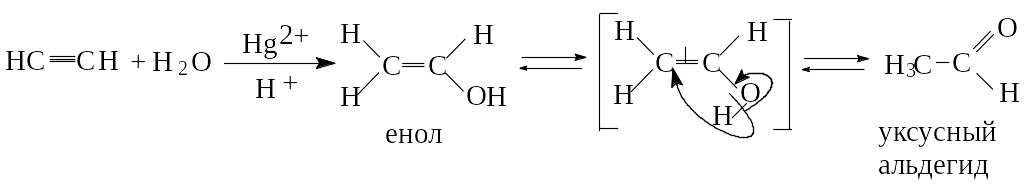
Реакция гидратации происходит в присутствии катализатора Hg2+ в кислой среде. Ацетилен, присоединяя воду, превращается сначала в енол (непредельный спирт), который затем перегруппировывается в альдегид. Реакция была открыта М.Г. Кучеровым и используется в промышленности для получения уксусного альдегида, из которого получают уксусную кислоту (А.Е. Фаворский, М.Ф. Шостаковский).
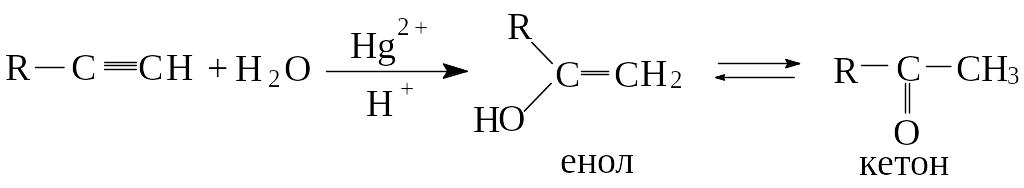
Присоединение воды к гомологам ацетилена происходит по правилу Марковникова. В результате перегруппировки из енолов образуются кетоны:
Присоединение спиртов
Алкины присоединяют спирты в присутствии солей ртути или меди, а также в присутствии алкоксидов или щелочи при нагревании, с образованием простых алкенильных эфиров. Реакция идет по механизму нуклеофильного присоединения:

Реакция используют в промышленности для получения полимеров.
Присоединение карбоновых кислот
В условиях гетерогенного катализа ацетилен присоединяет уксусную кислоту, образуя сложный виниловый эфир (винилацетат) – важный исходный продукт для получения поливинилацетата, легко гидролизируемого в поливиниловый спирт.
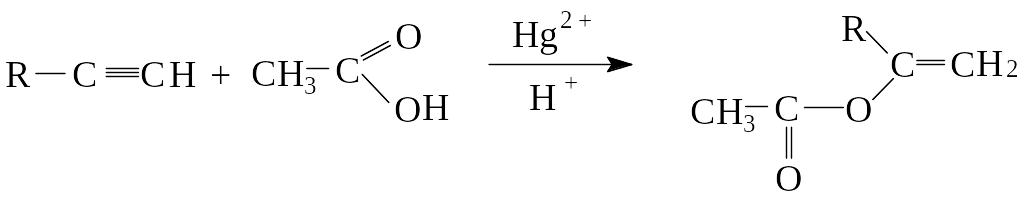
Присоединение HCN происходит в присутствии катализатора CuCl2+NH3:
HCCH + H-CN → H2C=CН-CN
Это один из промышленных способов получения акрилонитрила.
Присоединение трихлористого мышьяка происходит в присутствии катализаторов HgCl2, AlCl3 и др. в две стадии.
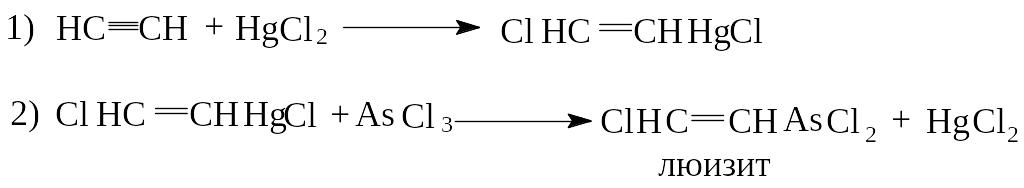
-хлорвинилдихлорарсин (люизит) – отравляющее вещество кожно-нарывного действия.
