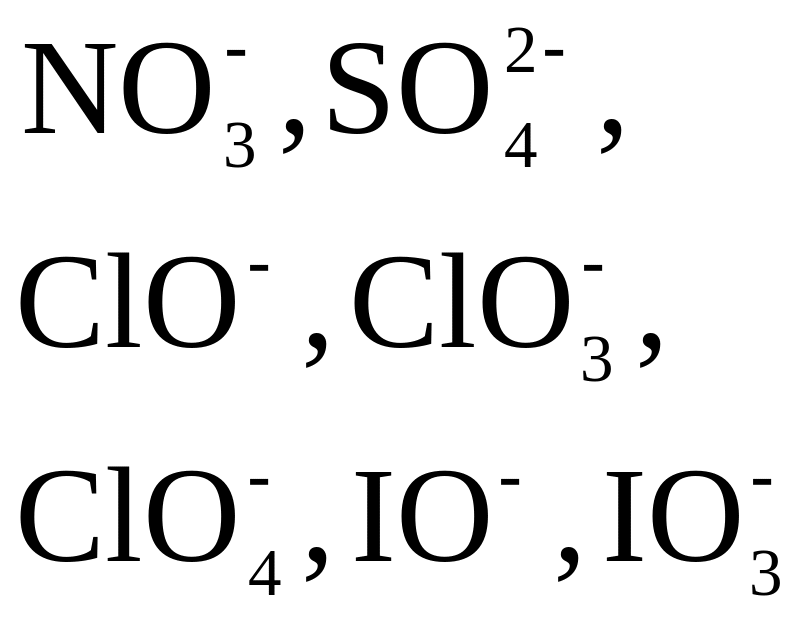- •Окисно-відновні реакції
- •Окисно-відновні реакції як процес перенесення електронів та зміни ступенів окиснення елементів
- •2. Найважливіші окисники та відновники
- •3. Класифікація окисно-відновних реакцій
- •2. Реакції диспропорціонування (самоокиснення-самовідновлення).
- •4. Методи підбору коефіцієнтів до окисно-відновних реакцій
- •5. Лабораторна робота Перманганатометричне титрування
- •Приготування стандартного розчину оксалатної кислоти (або нат-рій оксалату). Відомо, що калій перманганат взаємодіє в кислому середо-вищі з оксалатною кислотою:
- •Стандартизація розчину калій перманганату по оксалатній кислоті. Взяти чисту бюретку з краном, промити розчином калій перман-ганату і підготовити її до титрування.
- •Лабораторна робота Йодометричне титрування
- •Йодометричне визначення окисників та відновників. Титрування по заміщенню
- •Індикатор йодометричного титрування
- •Визначення вмісту Купруму(іі) у розчині. Йодометричне титрування застосовують для визначення Купруму(іі) в пестицидах, які містять мідь; за точністю воно не поступається електрохімічному визначенню.
- •6. Контрольні запитання
2. Найважливіші окисники та відновники
Про окисно-відновні властивості елементів у вигляді простих речовин (нейтральних атомів) можна судити за їх положенням у періодичній сис-темі. Якщо елемент знаходиться в сполуці, то його окисно-відновні влас-тивості залежать від його О.Ч.
Чим менш міцно пов’язані валентні електрони з ядром атома, тим вища відновна здатність атома. Таким чином, найбільш активними відновни-ками є атоми лужних металів і найбільш активний серед них – Францій. Атоми металів виявляють тільки відновні властивості. Виконуючи роль відновника, атоми металів переходять у позитивно заряджені іони:
Me –ne- Men+.
Активність металу як відновника у водних розчинах визначається його положенням у ряду стандартних електродних потенціалів, який, по суті, ві-дображає закономірність зміни потенціалів іонізації та електронегатив-ності.
Окисні властивості іонів металів збільшуються
![]()

Відновні властивості металів збільшуються
Д о
відновників належать і неметали, що
мають негативне О.Ч. До цієї групи
відновників належать кислоти, що не
містять Оксигену (HCl,
HBr,
HJ,
H2S,
H2Se,
H2Te)
та їх солі, гідриди лужних і лужноземельних
металів (NaH,
CaH2),
а також сполуки неметалів з Гідрогеном
(NH3,
N2H4,
PH3,
P2H4
тощо). Неметали, що входять до складу
цих відновників, здатні втрачати
електрони і переходити в нейтральні
атоми або ж підлягати подальшому
окисненню. Активність неметалів у
відповідному ряду сполук зростає в
пе-ріодичній системі зверху вниз.
Відновна здатність галогеноводнів
зростає в ряду:
о
відновників належать і неметали, що
мають негативне О.Ч. До цієї групи
відновників належать кислоти, що не
містять Оксигену (HCl,
HBr,
HJ,
H2S,
H2Se,
H2Te)
та їх солі, гідриди лужних і лужноземельних
металів (NaH,
CaH2),
а також сполуки неметалів з Гідрогеном
(NH3,
N2H4,
PH3,
P2H4
тощо). Неметали, що входять до складу
цих відновників, здатні втрачати
електрони і переходити в нейтральні
атоми або ж підлягати подальшому
окисненню. Активність неметалів у
відповідному ряду сполук зростає в
пе-ріодичній системі зверху вниз.
Відновна здатність галогеноводнів
зростає в ряду:
HF, HCl, HBr, HJ,
причому HF окиснюється лише електричним струмом на аноді.
До групи відновників належать позитивно заряджені іони металів, що мають нижчі О.Ч., здатні під час взаємодії з окисниками втрачати елек-трони з підвищенням О.Ч. Найпоширенішими відновниками є оксиди цих металів або їх солі:
|
|
|
|
|
|
|
Неметали можуть і приймати електрони, і віддавати їх, можуть вияв-ляти і окисні, і відновні властивості.
Чим більше електронів має атом на зовнішньому електронному шарі і чим ближче вони розташовані до ядра, тим сильніше виражена окисна здатність елемента. Найсильніші окисники – галогени, озон, кисень, сірка, сполуки металів, що мають найвищі позитивні О.Ч., іони благородних ме-талів. Атоми елементів підгрупи IV групи є слабкими окисниками.
Атом елемента в стані вищого ступеня окиснення виявляє тільки окис-ні властивості, оскільки може тільки приймати електрони (має тільки елек-тронно-акцепторні функції).
Метали, які мають найвище О.Ч., виконуючи функцію окисників, від-новлюються до нижчих О.Ч., а в деяких випадках до нейтральних металів. Найчастіше окисниками виступають такі метали, що мають найвище О.Ч.:
|
|
|
|
|
|
|
|
Іони благородних металів, які мають навіть низьке значення О.Ч., є досить сильними окисниками.
До групи окисників належать сполуки, що містять позитивно заряд-жений іон H+ (вода, кислоти), який при взаємодії з відновниками виявляє окисну дію:
2H+ +2e- H2.
Прикладом окисних властивостей іонів H+ можуть бути реакції актив-них металів із розведеними кислотами (крім нітратної).
До складу окисників належать метали з найвищим О.Ч. у вигляді оксидів, кислот та їх солей. Типовими представниками цих сполук є Mn2O7, KMnO4, HMnO4, CrO3, K2Cr2O7, K2CrO4, NaBiO3, Na2FeO4, V2O5, NaVO3 тощо.
Якщо в кількох сполуках елемент має найвище О.Ч., то сильнішим окисником за інших рівних умов буде та сполука, у якій масова частка цього елемента найбільша.
Окисні властивості мають також вищі оксигенвмісні кислоти немета-лів, їх ангідриди і солі.
Роль окисників можуть виконувати елементарні речовини (неметали), нейтральні атоми або молекули, які можуть приєднувати електрони і набувати негативного О.Ч.:
E0 + ne- E-n.
До цієї групи окисників належать р-елементи, що містять на зовніш-ньому шарі від семи до чотирьох електронів, для яких характерні велика спорідненість до електрона або велике значення електронегативності.
Для неметалів електронегативність і здатність приєднувати електрони зменшується у такій послідовності:
F, O, Cl, N, Br, S, J, Se, P, C, H, As, B, Si.
Молекули галогенів F2, Cl2, Br2, J2 при цьому перетворюються у не-гативно заряджені іони (F-, Cl-, Br-, J-).
Нейтральні молекули, атоми Оксигену, Сульфуру та їх аналогів пере-ходять до стану відновлення О-2, S-2 тощо.
Оксиген у атомарному стані і у складі простої речовини – кисню є дуже сильним окисником, особливо при високих температурах.
Сильні окисні властивості характерні для алотропічної модифікації Оксигену – озону. Як сильні окисники, озон і Флуор вбивають бактерії й тому застосовуються для дезинфекції повітря чи води. Щодо Флуору Оксиген виявляє відновні властивості:
![]()
2 |
1 |
|
(реакція окиснення); |
4 |
2 |
(реакція відновлення). |
Флуор і озон, як сильні окисники, спричиняють глибокі зміни в генах організмів за умови дуже низького їх вмісту в повітрі.
Озон використовують для оброблення питної води, зниження запахів у жирах і маслах, отримання альдегідів окисненням вуглеводнів тощо.
Практичне застосування як відбілювач має хлор, що під час взаємодії з вологою повітря утворює гіпохлоритну кислоту, яка розкладається з ви-діленням атомарного Оксигену:
HClO HCl + O.
Cульфур та його аналоги при підвищенні температури є окисниками щодо Гідрогену та металів. Продуктами відновлення Сульфуру є H2S та сульфіди металів.
Під час окиснення металів N, S, P, Si, C, B утворюються відповідно нітриди, сульфіди, фосфіди, силіциди, карбіди, бориди.
Найслабкішими окисниками серед простих речовин є неметали групи IVА (C, Si).
Хоча нейтральні атоми або молекули неметалів виявляють в основному окисні властивості, але, реагуючи з сильними окисниками (Флуором, озо-ном), вони віддають електрони і є відновниками.
Найпоширеніші окисники та відновники наведені у табл. 19.
Таблиця 19. Найпоширеніші окисники та відновники
Окисники |
Відновники |
||
Нейтральні атоми або молекули неме-талів |
F2, Cl2, Br2, J2, O2, S, P, O3 тощо |
Метали (лужні, лужноземельні та ін.) |
Li, K, Na, Rb, Cs, Ca, Sr, Ba, Mg, Zn, Al, Fe, Co, Ni, Cd, Sn, Pb, Cr, Mn |
Позитивно зарядже-ні іони металів з ви-соким ступенем окиснення |
Fe3+, Sn4+, Hg2+, Pb4+, Au3+, Co3+, Ni3+, Cu2+, Ti4+ тощо |
Негативно за-ряджені іони не-металів або не-метали у нега-тивному ступені окиснення |
Cl-, Br-, J-, S2-, Se2-, Te2- |
Оксигенметало-вмісні кислоти, їх ангідриди та солі |
Mn2O7, CrO3, V2O5, AuCl4
|
Позитивно за-ряджені іони ме-талів у нижчих ступенях окис-нення |
Fe2+, Sn2+, Cr2+, Mn2+, Ti2+, Cu1+ |
Вищі оксиген-вмісні кислоти неметалів |
|
Нижчі оксиген-вмісні кислоти, їх ангідриди та солі |
|
Атоми
елементів із проміжним ступенем
окиснення можуть мати як електронно-донорні,
так і електронно-акцепторні
функції та можуть вияв-ляти
як відновні,
так і окисні
властивості. Прикладом
таких речовин є
![]() та ін.
та ін.