- •Агрегатні стани речовини
- •1. Газоподібний стан речовини. Рівняння Клапейрона-Менделєєва
- •2. Рідинний стан
- •3. В’язкість. Рівняння де Гузмана
- •4. Структура рідини. Поверхневий натяг
- •5. Природні води
- •6. Забруднення природних вод. Очистка і опріснення води
- •7. Твердість води та методи її усунення
- •8. Важка вода, її застосування
- •9. Біологічна роль води
- •10. Іонний добуток води. Водневий показник
- •11. Буферні системи в організмі людини
- •12. Тверді тіла. Кристалічні ґратки
- •13. Металічний зв’язок
- •14. Будова високомолекулярних сполук
- •15. Контрольні запитання
РОЗДІЛ 6


Агрегатні стани речовини
Агрегатний стан речовини є функцією температури і тиску. Але ж це не означає, що, змінюючи температуру і тиск, можливо реалізувати для будь-якої речовини усі три агрегатні стани. Так, для кальцій карбонату можливий лише твердий стан, для сахарози, білкових речовин та інших – недосяжний газоподібний стан: при нагріванні вони розкладаються. З іншого боку, при певній температурі і певному тиску речовини можуть одночасно перебувати у всіх трьох агрегатних станах. Так, при 0,0076 С співіснують, знаходяться в рівновазі тверда вода (лід), рідка вода і газоподібна вода у вигляді насиченої пари з тиском 4,579 мм рт. ст.
1. Газоподібний стан речовини. Рівняння Клапейрона-Менделєєва
Головна риса газового стану – мала густина речовини, значна відстань між молекулами, малі сили зчеплення, в результаті чого газ прагне зайняти максимальний об’єм.
Закони ідеальних газів Бойля-Маріотта, Авогадро, Шарля і Гей-Люссака були встановлені дослідним шляхом і узагальнені в рівнянні Менделєєва-Клапейрона:
РV=RT, |
(58) |
де P – тиск; V – об’єм; Т – абсолютна температура.
Для будь-якого довільного числа молів газу рівняння набуває вигляду:
РV = RT. |
(59) |
Ці рівняння дають для різних температур кількісний зв’язок між об’ємом і тиском; їх називають рівняннями стану.
Константа R бере участь у багатьох фізико-хімічних залежностях і називається універсальною газовою сталою (R = 8,314 Дж/ моль К)). Оскільки R=PV/Т, то вона має певний фізичний зміст: це робота ізобарного розширення моля ідеального газу при підвищенні температури на один градус.
2. Рідинний стан
Рідинний стан вивчено менш повно, ніж газоподібний або твердий. Тому доцільно порівняти рідинний стан з твердим і газоподібним станами. У рідини, як і у газу, немає власної форми, але є власний об’єм, у той час як молекули газу займають увесь наданий їм об’єм. У рідинному стані текучі речовини набувають форми посудини, в яку вони розміщені. Речовини, які знаходяться в рідинному стані при 298 К і більш низькій температурі, називають рідинами. Якщо ж речовина переходить у рідинний стан при температурах, які перевищують 298 К, тоді такий стан називають розплавленим або розплавом.
Рідинний стан речовини обумовлено особливим характером розташування часток і особливим характером зв’язку, на відміну від газів у рідинах і розплавах частки знаходяться на відстанях того ж порядку, що і розміри самих часток.
У рідинах сили тяжіння співмірні з силами, які обумовлюють теплові коливання молекул. Частки можуть коливатися, переміщуватися і обертатися. Якщо сила, яка обумовлює теплові коливання частки, перевершує силу її зв’язку з іншою часткою, то вона може переміститися на відстань порядку її діаметра й утворити новий зв’язок з іншою часткою.
Стисливість рідин мала, їх густина близька до густини твердих тіл, але більш чутлива до змін температури.
При зниженні температури при постійному тиску речовини переходять із газоподібного стану, який характеризується відсутністю зв’язку між частками і формою, в рідинний стан, де частки взаємопов’язані, але форма не визначена, а потім у твердий стан із правильною фіксованою структурою. Однак, при зниженні температури рідина може заморожуватися без упорядкування структури. Тоді утворюється аморфна речовина, структура якої наближається до структури рідини.
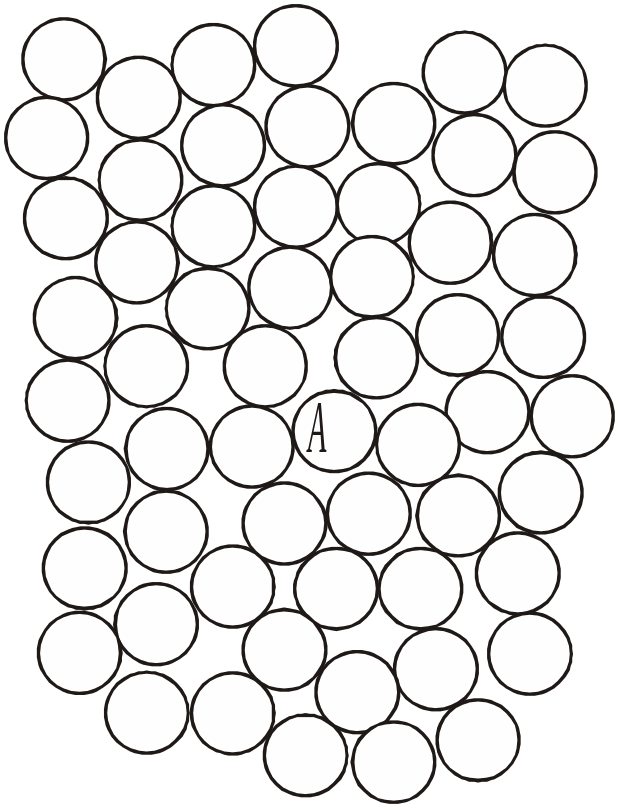
Наявність у рідині просторового упорядкування молекул підтверджується експериментальними даними по розсіюванню світла, дифракції рентгенівсь-кого випромінювання нейтронів і електронів. Рентгеноструктурні досліджен-ня показали, що в рідинах, які складаються із багатоатомних молекул, спосте-рігається не тільки упорядковане розташування молекул, але й відома зако-номірність у взаємній орієнтації часток. Ця орієнтація посилюється для поляр-них молекул й при формуванні водневого зв’язку. Але, як показано на рис. 28, лише поблизу даної частки спостерігається закономірне розташування су-сідніх часток.
При віддаленні від розглянутої частки А на відстань порядку 10 атомних відстаней закономірне розташування часток порушується. Таким чином, рідкий стан характеризується закономірним розташуванням часток у невеликих об’ємах і неупорядкованим – по всьому об’єму. Таку структурну влас-тивість рідкого стану виражають термінами “ближ-ній порядок” і “дальній порядок” і говорять, що в рідинах і в розплавах є ближній порядок і відсут-ній дальній порядок. |
Рис. 28. Розташування часток у рідині |