
- •М.П. Завгородній, м.М. Корнет, о.А. Бражко, л.О. Омельянчик біоорганічна хімія.
- •Частина 1
- •Тема 1. Класифікація і номенклатура біоорганічних сполук
- •1.5 Визначте родоначального структуру у формулі сполуки, яку використовують для синтезу антибіотика левоміцетину.
- •Доповніть фразу.
- •Тема 2. Хімічний зв’язок та взаємний вплив атомів в біОорганічних сполуках
- •2.1. Електронна будова елементів-органогенів
- •Атомні орбіталі
- •2.1.2 Гібридизація орбіталей
- •Ковалентні зв'язки
- •2.2.2 Донорно-акцепторні зв'язки
- •2.2.3 Водневі зв'язки
- •2.3. Спряження і ароматичність
- •2.3.1 Системи з відкритим ланцюгом спряження
- •2.3.2 Системи із замкнутою системою спряження
- •2.3.3 Електроні ефекти
- •Тема 3. Стереоізомерія біоорганічних сполук
- •Тема 4. Спирти. Феноли
- •4.1 Спирти
- •Лабораторна робота
- •4.2 Феноли і нафтоли
- •Лабораторна робота
- •Тема 5. Карбонільні сполуки (альдегіди і кетони)
- •Лабораторна робота
- •Тема 6. Карбонові кислоти.
- •6.1 Карбонові кислоти
- •Лабораторна робота
- •6.2 Фенолкислоти
- •Лабораторна робота
- •Тема 7. Ефіри та аміди карбонових кислот
- •7.1. Етери (прості ефіри)
- •Лабораторна робота
- •7.2 Естери (складні ефіри)
- •Лабораторна робота
- •7.3 Аміди кислот
- •Лабораторна робота
- •Навчальне видання
- •Боорганічна хімія.
- •Чатина 1
2.2.2 Донорно-акцепторні зв'язки
Перекривання двох одноелектронних АО - не єдиний шлях утворення ковалентного зв'язку. Ковалентний зв'язок може утворюватися при взаємодії заповненої двохелектронної орбіталі одного атома (донора) з вакантною орбіталлю іншого атома (акцептора). Донорами служать сполуки, що містять або орбіталі з неподіленою парою електронів, або π-МО. Носіями неподілених пар електронів (п-електронів, від англ. - що не зв'язують) є атоми азоту, кисню, сірки, галогенів.

аміак метанол метаналь метілхлорид
Неподілені пари електронів відіграють важливу роль в прояві хімічних властивостей сполук. Зокрема, вони відповідальні за здатність сполук вступати в донорно-акцепторну взаємодію.
Ковалентний зв'язок, що утворюється за рахунок пари електронів одного з партнерів по зв'язку, називається донорно-акцепторним або координаційним.
Донор Акцептор
неподільна
пара електронів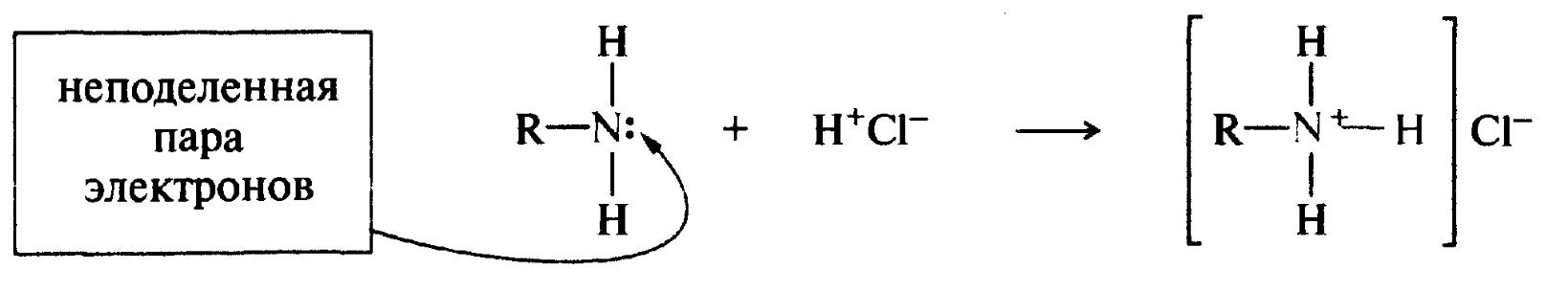
Первинний амін алкіламонійхлорид
Донорно-акцепторний зв'язок, що утворився, відрізняється тільки способом утворення; за властивостями вона однакова з іншими ковалентними зв'язками. Атом-донор при цьому переважає позитивний заряд.
Донорно-акцепторні зв'язки характерні для комплексних сполук, що називаються також донорно-акцепторними комплексами. Залежно від типу донора, тобто від того, які електрони усуспільнюються, комплекси класифікують як п- або π-комплекси.
Різновидом донорно-акцепторного зв'язку є біполярній (семиполярний) зв'язок, наприклад, в нітрогрупі.
Біполярний зв'язок
Нітросполука
Одночасно з утворенням ковалентного зв'язку за рахунок неподіленої пари електронів атома на зв'язаних атомів виникають протилежні по знаку заряди. Електростатичне поєднання ковалентної і іонної зв'язків дає біполярний зв'язок, характерною ознакою якого служить наявність протилежних зарядів на ковалентно зв'язаних атомах.
У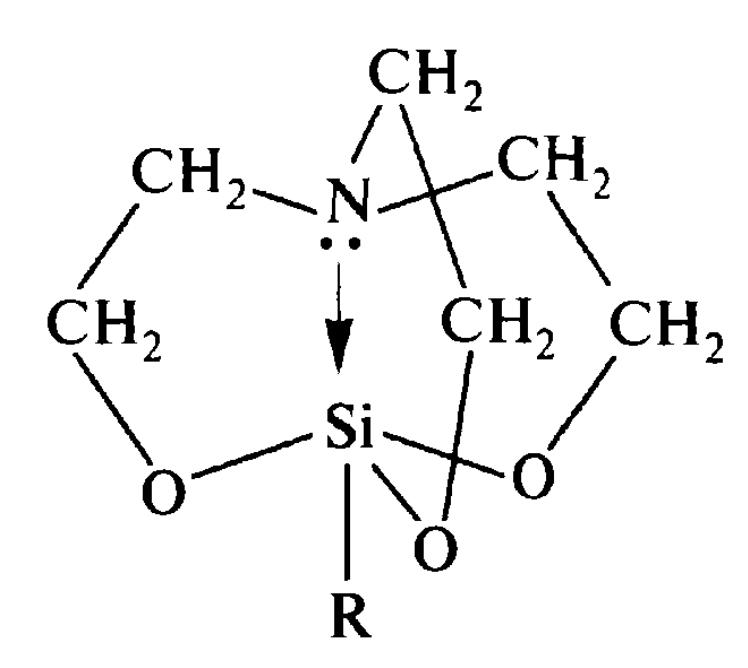 творення
донорно-акцепторного зв'язку може мати
місце і в тих випадках, коли донорний і
акцепторний атоми знаходяться усередині
однієї молекули і внаслідок особливостей
просторової будови зближені на відстань,
достатню для взаємодії між ними. Прикладом
сполук з таким внутрішньомолекулярним
координаційним зв'язком служать
сілатрани, що часто проявляють високу
біологічну активність.
творення
донорно-акцепторного зв'язку може мати
місце і в тих випадках, коли донорний і
акцепторний атоми знаходяться усередині
однієї молекули і внаслідок особливостей
просторової будови зближені на відстань,
достатню для взаємодії між ними. Прикладом
сполук з таким внутрішньомолекулярним
координаційним зв'язком служать
сілатрани, що часто проявляють високу
біологічну активність.
сілатрани
(R=Hal, Alk, Ar та ін.)
2.2.3 Водневі зв'язки
Атом водню, пов'язаний з сильно електронегативним елементом (азотом, киснем, фтором та ін.), здатний взаємодіяти з неподіленою парою електронів іншого досить електронегативного атома цій же або іншої молекули. В результаті виникає водневий зв'язок, що є різновидом донорно-акцепторного зв'язку. Графічно водневий зв'язок зазвичай позначається трьома точками.

Енергія водневого зв'язку невелика (10-4- кДж/моль) і в основному визначається електростатичною взаємодією.
Міжмолекулярні водневі зв'язки обумовлюють асоціацію органічних сполук, наприклад спиртів.
Міжмолекулярний
водневий зв'язок
Внутрішньомолекулярний
водневий зв'язок
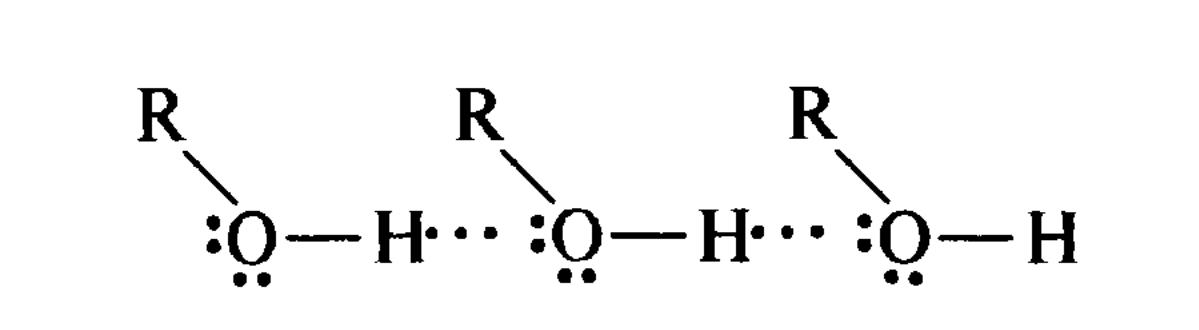
АСОЦІАЦІЯ МОЛЕКУЛ СПИРТУ
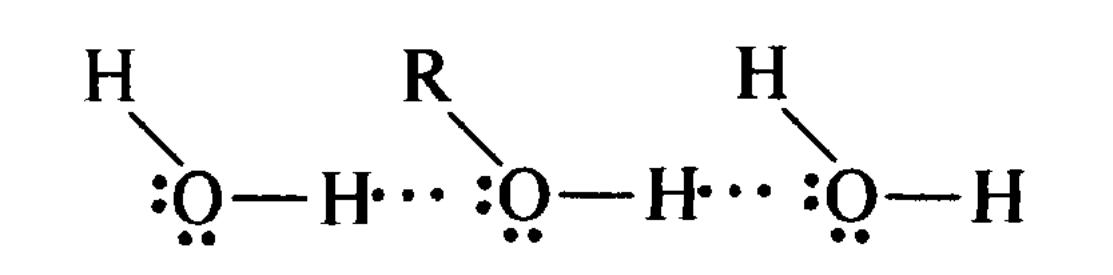
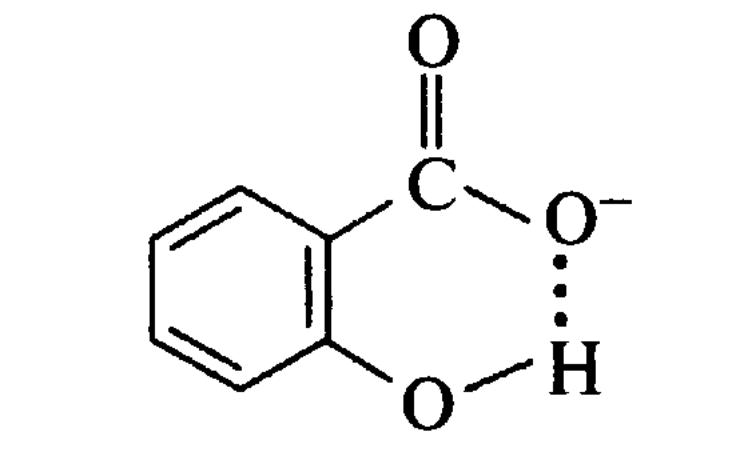
ГІДРАТАЦІЯ МОЛЕКУЛ СПИРТУ САЛІЦИЛАТ-ІОН
Водневі зв'язки впливають на фізичні (температури кипіння і плавлення, в'язкість, спектральні характеристики) і хімічні (кислотно-основні) властивості сполук. Так, температура кипіння етанолу С2Н5ОН (78,3°С) значно вища, ніж у того, що має однакову з ним молекулярну масу ефіру диметилу СН3ОСН3 (-24° С), що не асоціюється за рахунок міжмолекулярних водневих зв'язків. Органічні сполуки можуть взаємодіяти з розчинником, тобто сольватуватися, за рахунок міжмолекулярних водневих зв'язків. Наприклад, у водному розчині відбувається гідратація спиртів.
