
- •Классификация органических соединений. Сопряженные системы, электронные эффекты.
- •Классификация органических соединений.
- •Ковалентные связи.
- •Индуктивный эффект.
- •Сопряженные системы. Сопряжение.
- •Открытые сопряженные системы.
- •Типы сопряжения.
- •Замкнутые сопряженные системы.
- •Критерии ароматичности.
- •Ароматичность гетероциклов.
- •Мезомерный эффект
- •Виниловый спирт фенол
- •Электронодонорные (эд) и электроноакцепторные (эа) заместители.
Лекция № 1.
Классификация органических соединений. Сопряженные системы, электронные эффекты.
Биоорганическая химия изучает строение и свойства веществ, участвующих в процессах жизнедеятельности, связь их строения и свойств с биологической активностью. Это биополимеры: пептиды, белки, углеводы, нуклеиновые кислоты, это биорегуляторы: витамины, гормоны, лекарственные препараты.
Биоорганическая химия тесно связана с другими дисциплинами: биохимией, физиологией, биологией, фармакологией. Она является частью химического образования врача, т.к. в основе обмена веществ, процессов жизнедеятельности лежат органические реакции.
Знание химии позволяет познать молекулярную природу физиологических процессов, механизм действия ферментов, препаратов, механизм процессов зрения, памяти, дыхания.
Классификация органических соединений.
По строению углеродного скелета.
Ациклические (с открытой незамкнутой цепью):
А) алканы СН3 – СН2 – СН3
Б) алкены СН3 – СН = СН2
В) алкины СН3 – С ≡ СН
Ц
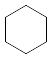 иклические
(с замкнутой цепью):
иклические
(с замкнутой цепью):
А![]() )
карбоциклические – циклоалканы
)
карбоциклические – циклоалканы
– ароматические
Б) гетероциклические – в цикл кроме атомов углерода входят атомы других элементов – гетероатомы (O,N,S).
![]()
![]()
![]()
![]()
По наличию функциональной группы.
Функциональная группа – это атом или группа атомов, определяющая принадлежность соединения к классу и его химические свойства.
Классы органических соединений.
Название |
Общая формула |
Функциональная группа |
Углеводороды |
R–H (CnH2n+2) |
––––––– |
Галогенопроизводные |
R–Cl |
––––––– |
Простые эфиры |
R–O–R |
––––––– |
Спирты |
R–OH |
–OH (гидрокси) |
Амины |
R–NH2 |
–NH2 (амино группа) |
|
R–NO2 |
–NО2 (нитро группа) |
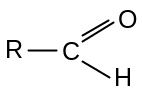
Альдегиды |
|
С=О (карбонильная) |
|
|
–С=О (карбонильная) |
|
|
–СООН (карбоксильная) |
|
|
–––––– |
Амиды |
|
–––––– |
Сульфокислоты |
R–SO3H |
–SO3H (сульфо) |
Тиоспирты |
R–SH |
–SH (тиогруппа, меркапто) |
Ковалентные связи.
Органическим соединениям характерны ковалентные связи.
Ковалентной связью называется химическая связь, образованная за счет обобществления электронов связываемых атомов. Существует два типа ковалентной связи: σ(сигма)– и π(пи)–связи.
σ–связь – одинарная ковалентная связь, образованная при перекрывании атомных орбиталей (АО) с максимумом перекрывания на прямой связывающей ядра атомов. Она возникает при перекрывании различных АО (s–, p–, sp3–)
σ σ σ
C – H C – C C – Cl
sp3 – s sp3 – sp3 sp3 – p
σ – связь очень прочная.
π–связь – ковалентная связь образованная при боковом перекрывании негибридных р–АО с максимумом перекрывания по обе стороны от прямой, связывающей ядра атомов. π–связь менее прочная, более реакционноспособная.
Ковалентная связь характеризуется следующими параметрами:
Энергия связи – энергия, необходимая на образование или разрыв связи.
Длина связи – расстояние между центрами ядер атомов. Длина связи С–С равна 0,154 нм, длина связи С=С равна 0,134 нм.
Полярность связи – неравномерное распределение электронной плотности связи.
Поляризуемость – подвижность электронов, их способность смещаться под действием внешнего поля. Электроны π–связи более подвижны, чем электроны σ–связи.
Реакционная способность соединений зависит от природы атомов в молекуле, природы связи между ними и от взаимного влияния атомов. Влияние атомов может передаваться по двум механизмам: индуктивному и мезомерному. Рассмотрим индуктивный эффект.

 Нитросоединения
Нитросоединения
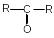
 Кетоны
Кетоны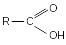 Кислоты
Кислоты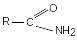 Сложные
эфиры
Сложные
эфиры