
- •Оглавление
- •Глава 1
- •Глава 2 этиология, патогенез и классификация
- •Глава 3
- •Глава 4 диагностика сахарного диабета
- •Диагностические критерии внутривенного теста на толерантность к глюкозе
- •Глава 5 диабетические ангиопатии
- •Глава 6 лечение сахарного диабета
- •Лечение инсулинзависимого диабета Диетотерапия
- •Инсулинотерапия
- •Лечение инсулиннезависимого диабета
- •Диетотерапия
- •Лечение пероральными сахароснижающими средствами
- •Глава 7
- •Гипогликемическое состояние и гипогликемическая кома
- •Лечение сахарного диабета во время хирургических вмешательств
- •Трудоспособность, трудоустройство и врачебно-трудовая экспертиза
Инсулинотерапия
Создание канадскими исследователями Бантингом и Бестом в 1921 г. лечебных препаратов инсулина, круто изменившее судьбу больных сахарным диабетом, является одним из самых замечательных достижений медицины XX века. Появилась возможность компенсировать абсолютную или относительную недостаточность инсулина введением экзогенного гормона. В настоящее время постоянно лечатся инсулином около 40--45% больных сахарным диабетом (по другим данным, 25-30%).
Сырьем для лекарственных препаратов инсулина являются поджелудочные железы некоторых животных, обычно крупного рогатого скота и свиней. Этим определяется одно из частых осложнений инсулинотерапии — появление антител к вводимому инсулину, отличающемуся по строению от человеческого и обладающему, следовательно, антигенными свойствами. Наиболее выражены антигенные свойства у бычьего инсулина, наименее — у свиного. Китовый инсулин с производства снят.
Инсулин принято дозировать в биологических единицах (путем тестирования его действия на кроликах) и в интернациональных массовых (1 ИЕ) или в единицах действия (ЕД). По современному международному стандарту, 1 мг препарата эквивалентен 24,5 ЕД, иначе говоря, 1 ЕД обеспечивается 0,04082 мг инсулина.
Все инсулиновые препараты выпускаются в специальных флаконах бесцветного стекла, закрытых резиновыми пробками с металлической окантовкой. При использовании пробки не снимают, а прокалывают иглой после обработки спиртом и набирают препарат в шприц. Флакон, выпускаемый нашей промышленностью, содержит 200 ЕД инсулина в 5 мл раствора. Это значит, что в каждом миллилитре содержится 40 ЕД инсулина. За рубежом выпускают флаконы по 5 и 10 мл, причем в 1 мл может быть 40, 80, 100 и 500 ЕД. Все это обозначено на флаконе и должно быть учтено врачом и объяснено больному. Срок хранения препаратов инсулина 2 года, инсулина Б — 3 года.
Комитетом экспертов ВОЗ по сахарному диабету (1981) внесено предложение об унификации выпуска препаратов инсулина с активностью 40 ЕД/мл.
Сахароснижающая лекарственная терапия ИЗСД осуществляется почти исключительно с помощью препаратов инсулина. Только в редких случаях удается перевести больного на прием пероральных средств, да и то на непродолжительное время. Это возможно у детей и подростков в самом начале заболевания. После компенсации метаболических нарушений с помощью инсулина из-за высокой остаточной активности сравнительно сохранных -клеток, возникает временная ремиссия заболевания (“всплеск” инсулинпродуцирующей способности поджелудочной железы). Однако затем инсулиновая недостаточность нарастает и инсулин на всю жизнь больного становится единственным средством лечения диабета.
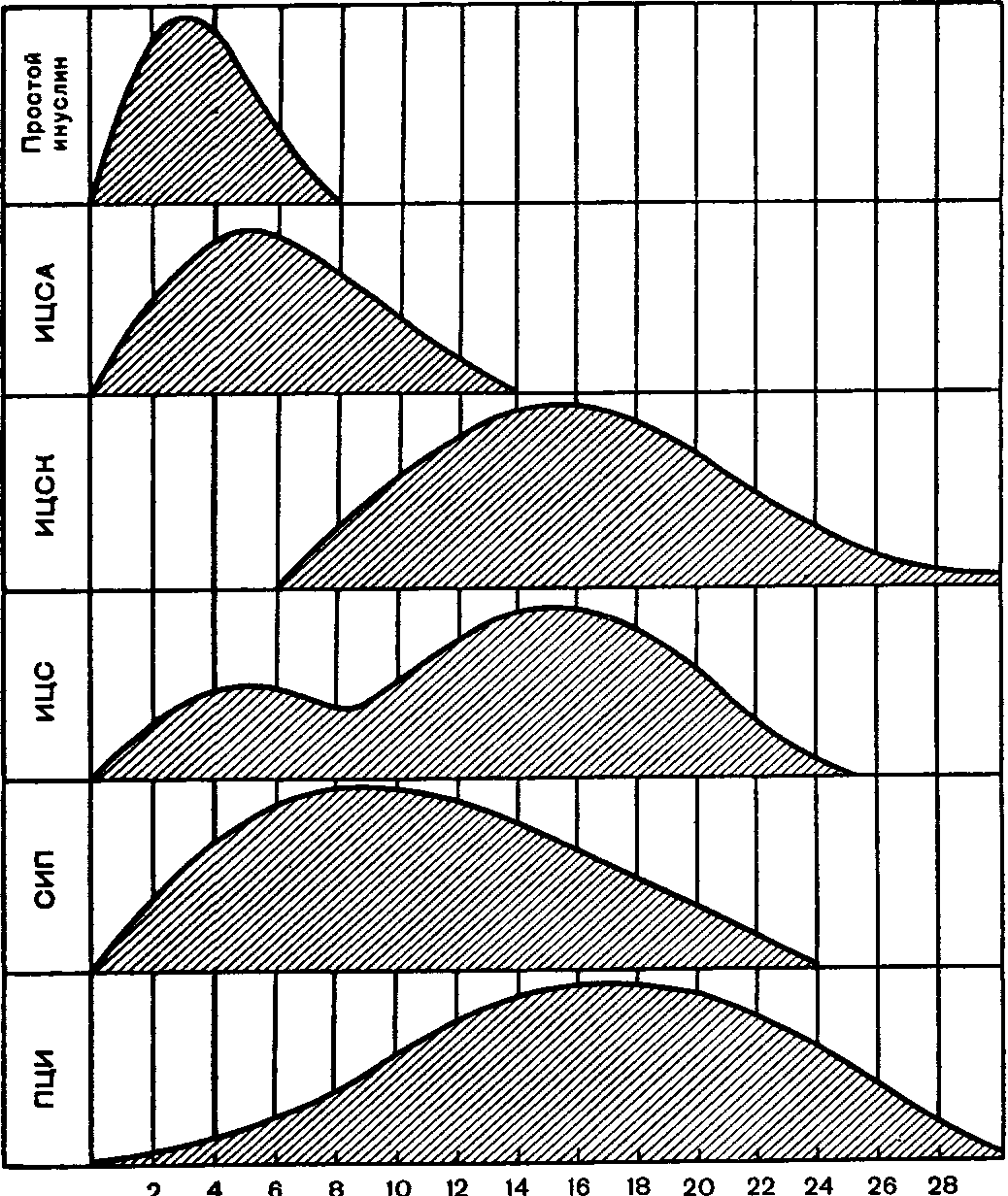
Современные препараты инсулина различаются в зависимости от сырья, технологического способа, которым достигается замедление их всасывания из места введения, и продолжительности действия (рис. 12). Всего в мире производится около 40 различных препаратов инсулина [Тихонова Е. П. и др., 1980]. В клинической практике препараты инсулина принято по длительности их действия делить на 3 группы (табл. 8).
Препараты инсулина короткого действия различаются по сырью, способу консервации, но достаточно близки по важнейшим фармакодинамическим и фармакокинетическим параметрам.
Инсулин для инъекций (в широкой врачебной практике его обычно называют простым, или обычным, инсули-лином) представляет собой кислый водный раствор кристаллического инсулина, получаемого из поджелудочных желез убойного скота с добавлением в качестве консерванта фенола. рН простого инсулина 3,0—3,5, что может обусловить болезненность подкожных инъекций. Действие препарата начинается через 15—30 мин после введения, достигает максимума через 2—3 ч, а затем постепенно снижается, продолжаясь в общей сложности 6—8 ч, редко больше. В настоящее время простой инсулин при постоянном лечении неосложненных случаев сахарного диабета используется обычно вместе с препаратами пролонгированного действия. Обычно препарат вводят подкожно, иногда внутримышечно. Не рекомендуется одномоментно вводить в одно место более 30 ЕД. Абсолютным и неотложным показанием к введению простого инсулина являются диабетический кетоацидоз, диабетическая кетоацидемическая, гиперосмолярная и лактаци-демическая прекома и кома. В таких случаях инсулин вводят внутривенно или внутримышечно и подкожно.
Время часы
Рис. 12. Временные параметры действия основных препаратов инсулина.
Таблица 8. Характеристика сахаросиижающего действия препаратов инсулина
Препарат инсулина |
Аналоги |
Гипоглихеммзирующее действие, ч |
||
|
|
начало |
максимум |
продолжительность |
Препараты короткого действия |
|
|
|
|
Инсулин для инъекций (простои инсулин) |
|
|
|
|
|
15-30 мин |
2-3 |
6-8 |
|
Суинсулин
|
Actrapid, |
15-20 мин |
2 |
6-7 |
Дания |
|
|
|
|
Моносуинсулин |
|
15—20 мин |
2 |
6-7 |
Препараты средней продолжительности действия' |
|
|
|
|
|
|
|
|
|
Суспензия цинк-инсулина аморфного, ИЦСА |
Insulinum |
|
|
|
senulente |
1-1 № |
4-6 |
12-14 |
|
|
(Дания) |
|
|
|
Суспензия инсулина-семилонг |
|
1-1 № |
4-6 |
12-14 |
Инсулин Б (ГДР) |
|
1-2 |
4-8 |
10-18 |
Препараты длительного действия. |
|
|
|
|
|
|
|
|
|
Протамин-цинк-инсулин, ГЩИ |
|
6-8 |
14-20 |
24-36 |
Суспензия инсулин-протамина, СИП |
Изофан- инсулин, NPH-инсулин |
|
|
|
1-1 и |
6-12 |
20-24 |
||
|
|
|
|
|
|
|
|
|
|
Суспензия цинк-инсулина, |
Insulinum lente (Индия, СФРЮ, Дания) |
1-2 |
10-16 |
24 |
ИЦС |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Суспензия инсулина-лонг |
|
l'A-2 |
10-16 |
24 |
Суспензия цинк-инсулина кристаллического, ИЦС К |
Insulinum ultralente (СФРЮ) |
|
|
|
6-8 |
12-18 |
30-36 |
||
|
|
|
|
|
|
|
|
|
|
Суспензия инсулина ультралонг |
|
6-8 |
12-18 |
30-36 |
|
|
|
||
Суинсулин— нейтральный (рН 7,0—7,5) водный раствор кристаллического инсулина, получаемого из поджелудочной железы свиней. Начало действия препарата через 15—20 мин после подкожного введения, максимум действия через 2 ч, продолжительность действия 6—7 ч. Обычно вводят подкожно, при диабетической коме внутривенно. Показания к назначению те же, что и для простого инсулина. Суинсулин используют чаще при резистентности к другим препаратам инсулина. Суинсулин оказался также эффективным при лечении липодистрофий, обусловленных применением обычного инсулина. Наконец, из-за большей близости химической структуры к инсулину человека суинсулин реже вызывает аллергические реакции, и его удается с успехом применять при общей или местной аллергической реакции на инсулин крупного рогатого скота. Отечественный суинсулин— аналог препарата Actrapid фирмы Novo (Дания).
Препараты инсулина средней продолжительности действия. Суспензия цинк-инсулина аморфного (инсулин-цинк-суспензия аморфный, ИЦСА) — суспензия инсулина с хлоридом цинка в буферном растворе нейтральной реакции (рН 7,1—7,5). Аморфные частицы инсулина медленно всасываются. Начало сахароснижающего эффекта через 1—1'/а ч после инъекции, максимум действия через 4—6 ч, продолжительность действия 12—16 ч. Таким образом, одна утренняя инъекция ИЦСА может заменить 2 инъекции простого инсулина (утреннюю и дневную). Препарат вводят обычно 2 раза в сутки в сочетании с простым инсулином или 1 раз вместе с ИЦС или ИЦСК. ИЦСА, как и другие препараты инсулина пролонгированного действия, нельзя вводить внутривенно. По действию ИЦСА близка к зарубежному (Дания, Югославия) препарату Insulinum semilente.
Инсулин Б (фирма Берлин-Хеми, ГДР)—кислый (рН 3—4) раствор кристаллического инсулина, пролонгированное действие которого обеспечивается добавлением амино-хинкарбамида гидрохлорида. Во флаконе содержится 10 мл препарата. Начало действия через 1—2 ч после введения, максимум через 4—8 ч, длительность 10—18 ч. Вводится только подкожно в 2 инъекции в сутки.
Препараты инсулина длительного действия. Протамин-цинк-инсулин (ПЦИ) — первый в истории диабетологии препарат инсулина пролонгированного действия. Его получают, добавляя к кристаллическому инсулину раствор прота-мина сульфата, цинка хлорида и фосфата натрия (рН 6,9—7,3). Начало сахароснижающего эффекта через 6—8 ч после инъекции, максимум через 14—20 ч, продолжительность 24—36 ч. Таким образом, действие препарата при его утреннем введении распространяется на вторую половину дня, вечернее, ночное и предутреннее время. Этим определяется необходимость для снижения уровня сахара крови в первую половину дня одновременно с ПЦИ вводить простой инсулин.
ПЦИ и простой инсулин нельзя смешивать в одном шприце. Дело в том, что ПЦИ содержит избыток протамина, с которым может связываться обычный инсулин, и тогда временные параметры действия введенной смеси становятся мало прогнозируемыми. Обычно тот и другой инсулин последовательно набирают в шприц и вводят через одну иглу, но в разные места подкожной клетчатки. Следует отметить, что аллергические реакции на ПЦИ могут быть связаны не только с непереносимостью инсулина, но и с гиперчувствитель-ностью к протамину как чужеродному белку. В настоящее время ПЦИ почти полностью вытеснен из эндокринологической практики новыми препаратами пролонгированного действия.
Суспензия инсулин-протамина (СИП) содержит меньше, чем ПЦИ, протамина, но больше цинка;
рН 7,0—7,3. По действию СИП близка к зарубежным препаратам изофан-инсулину и NPH-инсулину (нейтральный про-тамин Хагедорна). Сахароснижающее действие СИП начинается через 1—V/2 ч после введения, достигает максимума через 6—12 ч, продолжается 20-24 ч. При необходимости СИП можно смешивать в одном шприце с простым инсулином и тотчас после смешивания вводить под кожу, обычно 1 или 2 раза в сутки.
Суспензия цинк-инсулина кристаллического (инсулин-цинк-суспензия кристаллический, ИЦСК) — препарат, близкий к зарубежному препарату Insulinum ultralente. Инсулин в суспензии находится в виде крупных кристаллов, нерастворимых в воде, медленно всасывающихся; рН 7,1—7,4. Начало сахароснижающего эффекта через 6—8 ч, максимум через 12—18 ч, продолжительность до 36 ч. Назначают при высокой гликемии в комбинации с простым инсулином, с ИЦСА и вводят один (обычно утром), редко 2 раза в сутки.
Суспензия цинк-инсулина (инсулин-цинк-суспензия, ИЦС) состоит из 30% ИЦСА и 70% ИЦСК. Близка к зарубежному препарату Insulinum lente; pH 7,1-7,4. Действие препарата начинается через l—11/2ч после введения, первый пик действия наступает через 5—7 ч, второй, более значительный, через 10—16 ч. Общая продолжительность действия 24 ч и более. ИЦС является базисным препаратом, который вводят 1—2 раза в сутки в сочетании с простым инсулином, а также с ИЦСА.
Одна из важнейших проблем инсулинотерапии сахарного диабета—более или менее выраженный, но всегда неизбежный при длительном лечении иммунный ответ больного организма на введение чужеродного белка. Как подчеркивают эксперты ВОЗ по сахарному диабету (1981), “различия между инсулинами из поджелудочных желез различных животных не определяют их антидиабетического действия, но могут обусловливать разные иммунные ответы у больных диабетом”.
Монопиковые инсулииы. В последние 10—15 лет создан ряд технологии лучшей очистки промышленного инсулина от крупномолекулярных иммуноактивных примесей. С помощью гель-хроматографической очистки удалось получить так называемый монопиковый инсулин (т. е. дающий один пик на хроматограмме) 98% чистоты. Еще чище монокомпонентный инсулин, получаемый с помощью хроматографии на ДЕАЕ-целлюлозе. Она освобождает препарат от 99% макромолеку-лярных примесей.
Высокоочищенные препараты инсулина значительно реже вызывают аллергические реакции, а также липоатрофии, но, к сожалению, меньше влияют на развитие инсулинорезистент-ности. Поскольку в развитии диабетической микроангиопатии иммунным механизмам придается все большее значение, важно выяснить, как лечение монокомпонентными инсулинами влияет на их возникновение и эволюцию.
В настоящее время прошли клиническое испытание и разрешены для клинического применения в нашей стране монопиковые инсулины моносуинсулин, суспензия инсулина-семилонг, суспензия инсулина-лонг и суспензия инсулина-ультралонг.
Моносуинсулин (М-инсулин) имеет начало, максимум и продолжительность действия такие же, как у суинсулина. Может иметь нейтральную или кислую реакцию в зависимости от сырья и технологии.
Суспензии инсулина-семилонг, лонг и ультралонг по своему составу и параметрам гипогликемизирующего эффекта не отличаются от инсулинов отечественного производства группы ИЦС (соответственно ИЦСА, ИЦС и ИЦСК).
По первым результатам клинического применения [Пляц О. М. и др., 1984] монопиковые препараты инсулина ускоряют компенсацию диабета, снижают суточную потребность в гормоне. В некоторых случаях удается уменьшить инсулинорезистентность, устранить лабильность диабета, снизить титр антител к инсулину. Монопиковые препараты инсулина обладают статистически достоверно меньшими аллергизирующими свойствами, по некоторым данным, дают хороший лечебный эффект при инсулиновой липодистрофии
Препараты инсулина выдают больным в районной поликлинике бесплатно (так же как и пероральные сахаро-снижающие препараты) Хранить их следует в холодильнике при температуре 3—5°С, в том отделе, где обычно хранятся овощи и фрукты, ни в коем случае не допуская замораживания Нельзя вводить инсулин холодным, необходимо подогревать флакон в ладонях до температуры тела Пролонгированные препараты перед тем, как набирать в шприц, перемешивают встряхиванием Обычно инъекции инсулина больной делает себе сам. Для этого во время госпитализации, когда впервые назначают инсулин, больного обучают проведению инъекций (стерилизация шприца и игл, набор необходимой дозы в шприц и т. д.). Больному разъясняют принцип лечения вплоть до профилактики осложнений инсулинотерапии и в первую очередь предупреждения и купированния гипогликемии. Детям до 10 лет, лицам с резко сниженным зрением, физически немощным или умственно неполноценным больным инъекции делают родственники, а при отсутствии такой возможности—медицинская сестра поликлиники. Сами больные вводят себе инсулин подкожно в переднюю или наружную поверхность бедра, в подкожную клетчатку живота. Если инъекцию выполняет другой человек, то можно вводить препарат в плечи, в подлопаточную область, ягодицы. Очень важно, чтобы место введения инсулина менялось при каждом уколе. С самого начала больного следует ориентировать на строжайшее соблюдение правил асептики.
Тактика инсулинотерапии. Определить величину инсулиновой недостаточности и рассчитать потребность больного в экзогенном инсулине невозможно. Дозу препарата подбирают в значительной мере эмпирически. Дело осложняется еще и тем, что реакция разных больных на одну и ту же дозу одного и того же препарата инсулина различна (время начала, максимума и общая продолжительность действия инсулина). Наконец, даже у одного и того же больного чувствительность к инсулину в разные периоды заболевания может быть различной.
К этому нужно добавить, что врача, особенно впервые назначающего инсулин, всегда волнует не только чувствительность больного к сахароснижающему действию препарата, но и опасность аллергической реакции В разное время были предложены специальные пробы чувствительности больного к инсулину и вероятности аллергической реакции. Однако от проб на чувствительность к инсулину, пришлось отказаться ввиду их малой информативности. Проба на аллергию к инсулину проводится тогда, когда в анамнезе больного имеется сывороточная болезнь или поливалентная лекарственная аллергия, при отчетливых признаках аллергических заболеваний. Однако и в этих условиях результаты пробы не всегда однозначны.
Тест на аллергию к инсулину выполняют путем внутри-кожного введения в сгибательную поверхность предплечья 0,5—1 ЕД инсулина. Если в течение часа на месте инъекции не появляется гиперемии, отечности, зуда, то можно вводить лечебную дозу инсулина. В противном случае проводят десенсибилизирующие мероприятия.
Инсулинотерапия каждого больного должна быть максимально индивидуализированной. Дозы инсулина и режим его введения определяются в значительной мере образом жизни больного, стереотипом питания, физической активностью. Как уже говорилось, режим приема пищи, распределение энергетической ценности суточного рациона, сахарная ценность каждой порции пищи должны быть строго одинаковыми. Это возможно только тогда, когда больной и его родственники сознательно сотрудничают с врачом. В идеале больной должен ежедневно рассчитывать энергетическую и сахарную ценность как суточного рациона, так и каждого приема пищи, разнообразя при этом меню при одинаковом ежедневном количестве белков, жиров и углеводов в пище.
Физическая активность больного также должна быть настолько стереотипной, насколько это возможно. Это в равной мере относится к физическим нагрузкам на работе, в быту и к спортивным занятиям. Максимум нагрузки должен приходиться на часы, следующие за посталиментар-ной гипергликемией. В этом случае физические упражнения на фоне инсулинотерапии способствуют снижению уровня гликемии, стабилизации диабета, при точном дозировании не создают риска гипогликемических состояний. Только соблюдение всех этих условий позволяет подобрать такой режим инсулинотерапии, который обеспечивает компенсацию диабета
В крови здорового человека постоянно имеется определенный базальный уровень инсулина. Бета-клетки поджелудочной железы дискретно высвобождают в кровь в ответ на каждое повышение гликемии определенные порции инсулина, необходимые для того, чтобы обеспечить утилизацию тканями глюкозы Искусственно воспроизвести этот механизм с помощью подкожного введения препаратов инсулина практически невозможно, не обращаясь к слож-ным и дорогостоящим компьютерным системам Вместе с тем для удовлетворительной компенсации метаболических нарушении совершенно необходимо, чтобы в любой момент инсулинемия максимально соответствовала гликемии
Долгое время была общепринятой практика однократного подкожного введения больному всей суточной дозы инсулина пролонгированного и короткого действия. Это было удобно и больному, и его родственникам, и поликлинике, если инъекции делала медицинская сестра. Подбирая дозы препаратов инсулина короткого, среднего и длительного действия, надеялись добиться такого уровня инсулинемии, который обеспечивал бы нормогликемию как на высоте алиментарной нагрузки, так и в перерывах между приемами пищи, в том числе ночью. Эта цель в большинстве случаев оказывалась недостижимой. Как видно на рис. 8, всякий прием пищи приводит к повышению содержания сахара в крови. В ответ на гипергликемию у здорового человека высвобождается повьпиенное количество инсулина, обеспечивающее должную инсулинемию. У больного диабетом “погасить” посталиментарный подъем гликемии можно только тогда, когда каждому приему пищи будет предшествовать инъекция быстродействующего препарата инсулина. При однократном введении препаратов разной продолжительности действия инсулинемия обычно оказывается или недостаточной, чтобы предотвратить посталиментарную гипергликемию, или слишком значительной, создающей риск развития гипогликемии в интервале между приемами пищи
В настоящее время вводят комбинации различных препаратов инсулина (пролонгированного и короткого действия) в несколько инъекций, точно соотнося время введения гормона с периодами посталиментарной гипергликемии. Как специально отмечает Комитет экспертов ВОЗ по сахарному диабету (1981), “хороший контроль уровня глюкозы в крови обычно лучше достигается с помощью не одной, а нескольких ежедневных инъекций—обычно двух, а иногда и трех”
При подборе дозы инсулина необходимо учитывать давность заболевания, исходную гликемию, а также предшествующий опыт лечения (если таковой имеется). Существует представление о средней потребности больных ИЗСД в инсулине в зависимости от продолжительности и некоторых особенностей заболевания. На первом году болезни она обычно не превышает 0,5 ЕД/(кг • сут), а после компенсации метабочических нарушений снижается в среднем до 0,4 ЕД/(кг-сут) У беременных (при беременности до 20 нед) потребность в инсулине 0,6 ЕД/(кг • сут). В дальнейшем потребность в инсулине повышается до 0,7— 0,8 ЕД/(кг • сут), но у лиц с массой тела свыше 60 кг она обычно не более 40 ЕД/сут [Касаткина Э П., 1986]. При кетоацидозе потребность в инсулине может возрастать до 1 ЕД /(кг. сут).
Лицам с давно установленным диагнозом, особенно получающим препараты инсулина в одной инъекции, нередко приходится уменьшать дозу инсулина. Так, J. Ofefsky и R. Sherwin (1985) рекомендуют при синдроме хронической передозировки инсулина (см. ниже) у больных, получающих 0,7—0,9 ЕД/(кг-сут), снижать дозу до 0,7 ЕД/(кг-сут). При отсутствии признаков этого синдрома и дозе инсулина 0,9 ЕД/(кг-сут) и выше ее уменьшают на 20-25%.
В стационаре удобно начинать инсулинотерапию больного впервые выявленным ИЗСД с простого инсулина (хотя это не обязательно) и затем, после определения дозы, необходимой для компенсации, перевести больного на лечение комбинацией препаратов инсулина с различной продолжительностью действия. Если у пациента выявлен кетоацидоз или другие серьезные нарушения обмена, мы придерживаемся тактики, изложенной в главе 7. Сначала назначают сугубо ориентировочные дозы инсулина, которые наверняка не вызовут гипогликемического состояния.
Простой инсулин больньпл без симптомов кетоацидоза назначают в 3 инъекциях: перед завтраком, обедом и ужином. Соотношение доз 2:2:1, иногда 2:3:1. Начальные утренняя и дневная дозы в зависимости от гликемии варьируют в пределах 6—16 ЕД, вечерняя — 4—10 ЕД. Больного предупреждают о том, что он должен есть через 20— 30 мин (после начала действия препарата) и через 2—3 ч (максимум его действия) после каждой инъекции инсулина. Дальнейшее уточнение дозы проводится под контролем гли-кемического профиля (определение сахара крови каждые 3—4 ч). При невозможности многократного в течение суток исследования уровня сахара крови ориентиром может быть его количество в 4 порциях мочи. Измеряют объем мочи и подсчитывают глюкозурию в граммах. Первую порцию мочи собирают между утренним и дневным введением инсулина, вторую — между дневным и вечерним, третью — после вечерней инъекции до ночного сна, четвертую — в течение ночи. Сахар в определенной порции мочи является показанием к повышению дозы инсулина в предшествующей инъекции. Если необходимо, назначают 2 дополнительные инъекции инсулина в небольших дозах (обычно в 6—7 ч и в 22 ч).
По мере компенсации обменных нарушений (устранение глюкозурии, снижение гликемии) чувствительность больного к препаратам инсулина повышается. Дозы инсулина приходится снижать, причем тем больше, чем выше была начальная компенсирующая доза.
После достижения компенсации диабета с помощью простого инсулина больного переводят на лечение комбинацией препаратов простого и пролонгированного действия. Иногда, особенно в поликлинических условиях, лечение начинают сразу же с комбинации препаратов разной продолжительности действия, вводимых в 2 инъекции.
Предпочтительность такого лекарственного режима связана с тем, что препараты инсулина пролонгированного (среднего, длительного) действия создают базальный уровень инсулинемии, а инсулины короткого и быстрого действия (простой инсулин, суинсулин), назначение которых приурочивается к основным приемам пищи (завтрак, обед, ужин), не позволяют посталиментарной гипергликемии подниматься выше допустимого предела. Соотношение доз препаратов дневного и ночного действия 2:1.
Препараты пролонгированного действия ИЦС, ИЦСА и ИЦСК можно смешивать в шприце в различных соотношениях. ИЦС представляет собой смесь ИЦСА и ИЦСК в стандартном отношении 3:7 и поэтому при утреннем введении максимально активен ночью. Преимущественно ночной активностью характеризуются также ИЦСК, СИП и ПЦИ. Напротив, ИЦСА и Б-инсулин обеспечивают инсулинемию в течение первых полусуток после введения.
При переводе больного с лечения простым инсулином на терапию любым из препаратов пролонгированного действия следует учесть возможность повышенной чувствительности к вновь назначенному виду инсулина и связанную с этим вероятность развития гипогликемического состояния (к тому же из-за нейтральной реакции пролонгированные инсулины практически не разрушаются в месте введения). Сначала доза нового препарата должна быть на 20% ниже дозы препарата, применявшегося ранее. Это же правило распространяется и на те случаи, когда один препарат пролонгированного действия заменяется другим.
Назначая одновременно различные препараты инсулина, следует помнить, что нельзя вводить в одном шприце и в одно и то же место подкожной клетчатки препараты, замедление резорбции которых достигается разными про лонгаторами (например, кристаллами цинка в ИЦС и протамином в ПЦИ), и препараты кислой и нейтральной реакции (кислую реакцию имеют простой инсулин и инсу лин Б, нейтральную — суинсулин, СИП, ПЦИ, препараты группы ИЦС).
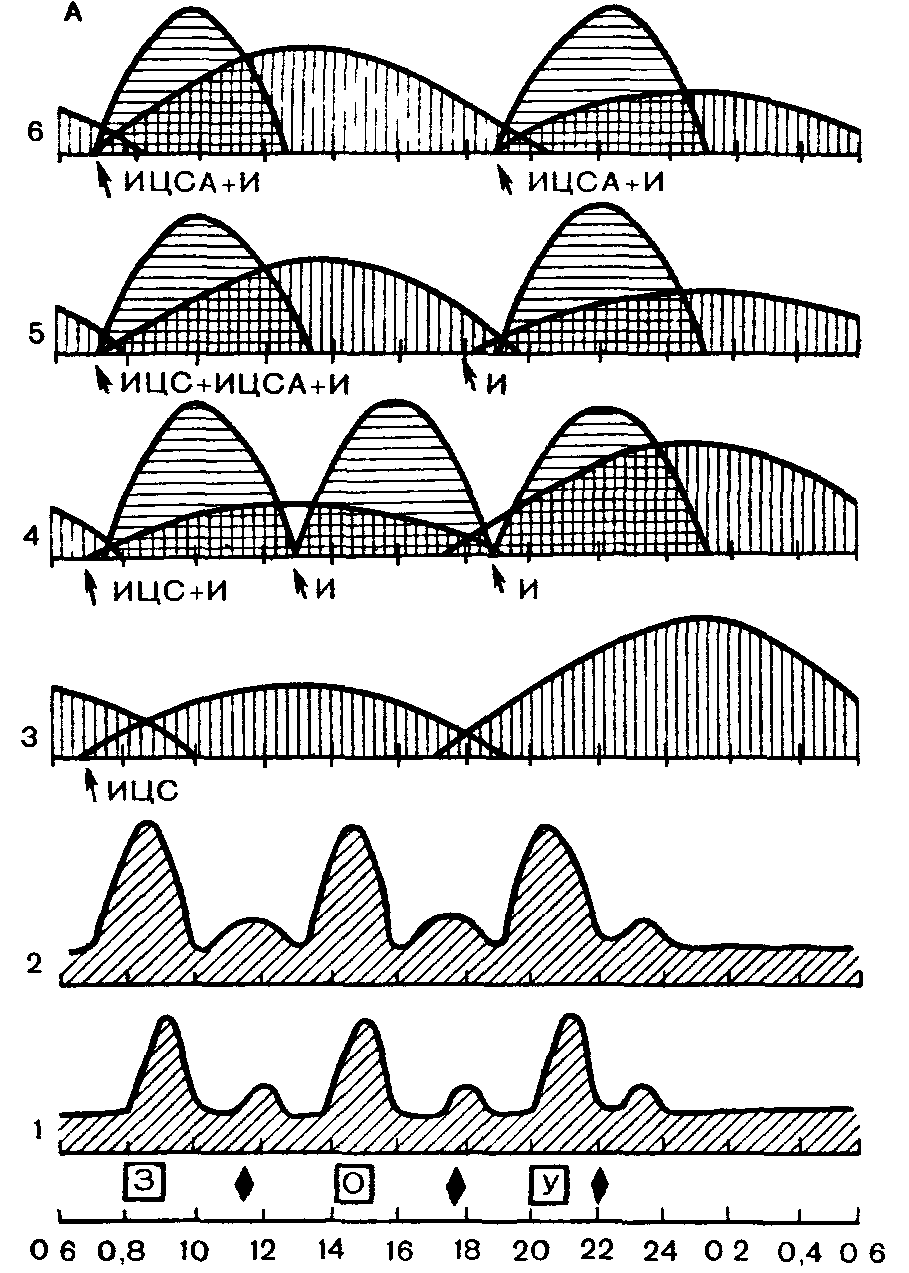
Время суток часы
Рис. 13. Суточные колебания гликемии и инсулинемии у здоровых лиц при обычном питании и у больных сахарным диабетом при различных вариантах инсулинотерапии (по Э. П. Касаткиной, 1986).
Квадраты обозначают основные приемы пищи (завтрак, обед, ужин), темные ромбы — закуску, стрелки — инъекции инсулина. А • 1 — колебания гликемии при традиционном режиме питания у здоровых, 2 — колебания инсулинемии у здоровых людей; 3 — колебания инсулинемии у больных диабетом при одноразовом введении препарата инсулина суточного действия (типа ИЦС), 4 — колебания инсулинемии у больных диабетом при трехразовом введении инсулина (ИЦС + 3 инъекции инсулина короткого действия), 5 — колебания инсулинемии при двухразовом введении инсулина (ИЦС + ИЦСА + 2 инъекции инсулина короткого действия); 6 — колебания инсулинемии при двухразовом введении инсулина (ИЦСА + И).
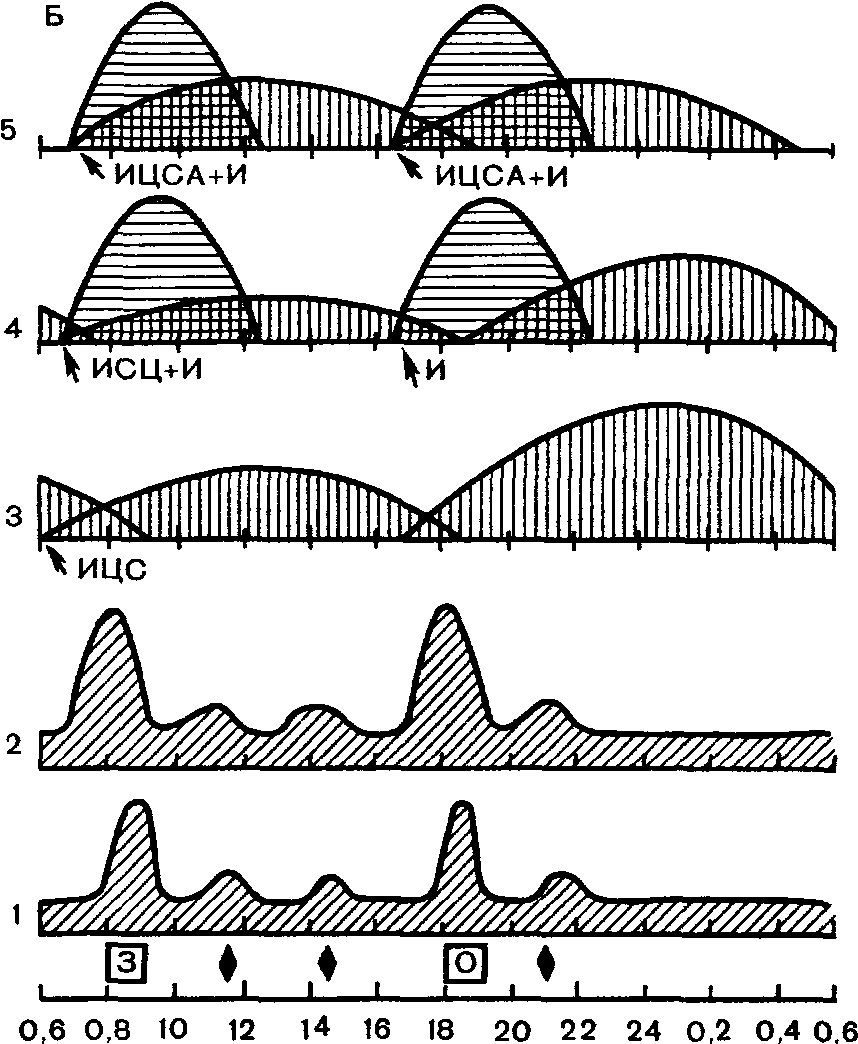
Б 1 — колебания гликемии при двухразовом приеме основных количеств пищи (завтрак, поздний обед) и 3 закусках у здоровых, 2 — колебания инсулинемии при таком же режиме питания у здоровых людей; 3 - колебания инсулинемии у больных диабетом при одноразовом введении инсулина суточного действия, 4 — колебания инсулинемии при двухразовом введении инсулина (ИЦС + 2 инъекции короткого действия), 5 — колебания инсулинемии при двухразовом введении комбинации препаратов ИЦСА + И
В практике лечения ИЗСД можно применять следующие режимы инсулинотерапии (рис. 13, 14).
1. Введение утром ИЦС и простого инсулина перед каждым из трех основных приемов пищи (завтрак, обед, ужин). Этот режим, очень неудобный для работающего пациента, показан при лабильном диабете, в период декомпенсации заболевания, а также детям дошкольного возраста [Касаткина Э. П., 1986].
2. Перед завтраком ИЦС, ИЦСА и простой инсулин, перед ужином—простой инсулин. Усвоение углеводов, поступивших с пищей в обед, обеспечивает действие ИЦСА.
3. Перед завтраком и перед ужином вводят ИЦСА и простой инсулин.
4. Перед завтраком и ужином инсулин Б и простой инсулин.
5. Перед завтраком и ужином ИЦС или СИП и простой инсулин.
6. Перед каждым приемом пищи (3 инъекции) вводят простой инсулин, а перед сном ИЦС или СИП (в расчете на то, что преимущественно “ночное” сахароснижающее действие ИЦС или СИП будет осуществляться в течение следующего дня).
7. Утром ИЦС или СИП и простой инсулин, перед ужином простой инсулин и на ночь (в 22 ч) ИЦС или СИП.
8. Перед каждым приемом пищи простой инсулин, перед завтраком ИЦСК. Иногда ИЦСК назначают и перед ужином.
Если двукратное введение препаратов инсулина почему-либо невозможно или нежелательно и суточная доза должна вводиться в одной инъекции, то можно рекомендовать следующие режимы:
1. Утром ИЦС, ИЦСА и простой инсулин.
2. Утром ИЦСА, ИЦСК и простой инсулин.
Во всех схемах терапии простой инсулин можно заменить суинсулином.
В стационаре инсулинотерапия контролируется по глике-мическому профилю, в поликлинике на протяжении недели делают 3—4 выборочных исследования гликемии перед разными приемами пищи, а также через 1 или 2 ч после еды. Можно пользоваться индикаторными полосками глюкозан (СССР), декстронал или декстростикс для ориентировочного определения гликемии.
Суточную глюкозурию каждый больной может определять ежедневно сам. Определяют сахар в моче, собранной между двумя инъекциями инсулина, после второй инъекции до сна, в течение ночи, а также в ранние утренние часы. Отсутствие глюкозурии в последней (четвертой) порции мочи иногда может быть предвестником утренней гипогликемии, а высокая глюкозурия — свидетельством так называемого феномена зари—высокого глюконеогенеза в период между 4 и 7 ч утра.
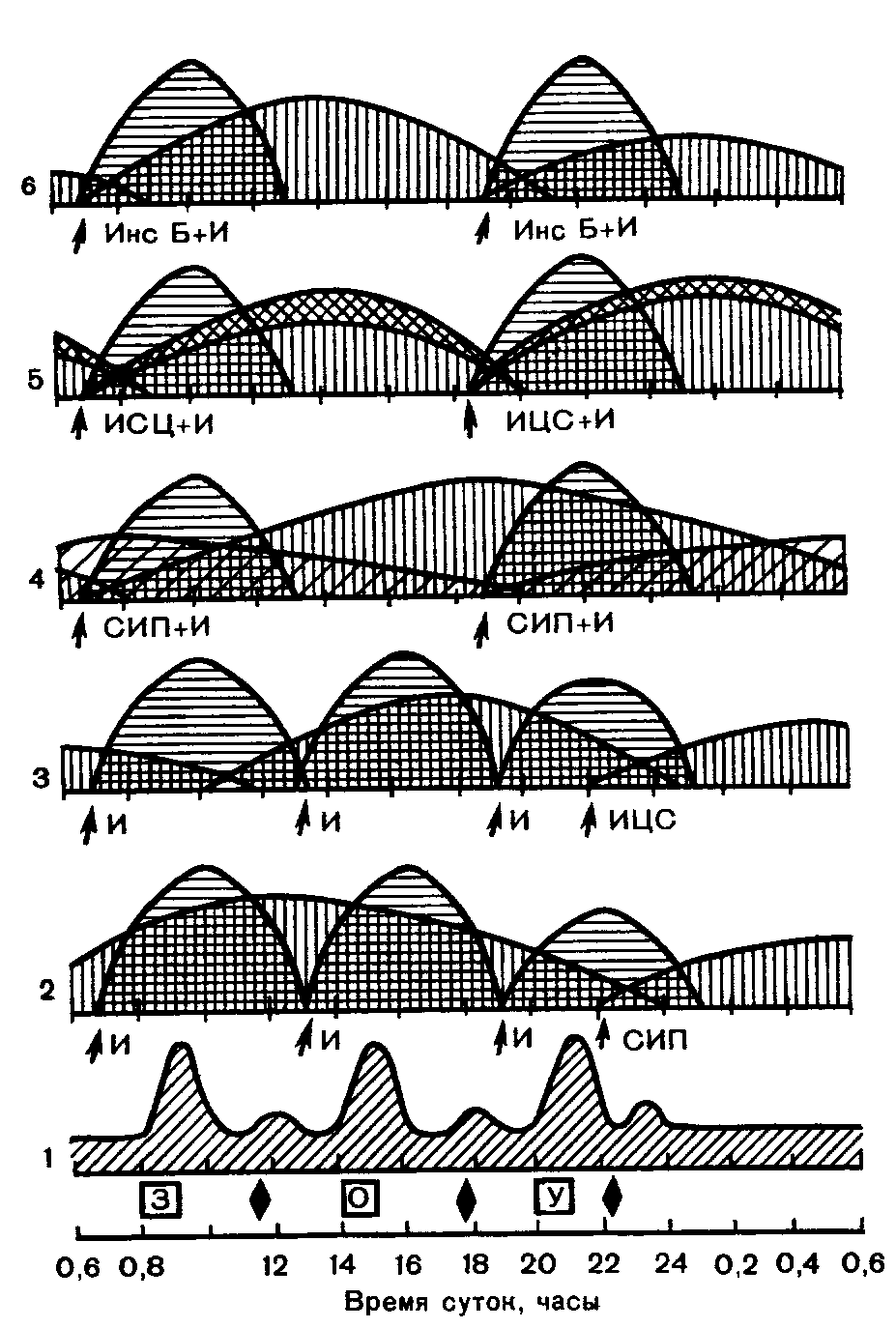
Рве. 14. Суточные колебания инсулинемии у больных сахарным диабетом при некоторых режимах инсулинотерапии. Условные обозначения те же,
что на рис. 13 A.I— колебания гликемии у здорового человека при традиционном режиме питания, 2 — колебания инсулинемии при троекратном введении инсулина короткого действия и инъекции СИП на ночь (в 22 ч), 3 — колебания инсулинемии при троекратном введении инсулина короткого действия и инъекции ИЦС на ночь (в 22 ч), 4 — колебания инсу-линемни при двукратном введении комбинации СИП + И, 5 — колебания инсулинемии при двукратном введении комбинации ИЦС + И, 6 — колебания инсулинемии при двукратном введении комбинации Б-инсулин + И, Б 7 — колебания инсулинемии при двукратном введении инсулина короткого действия и введении ИЦС утром и на ночь, 8 — колебания инсулинемии при двукратном введении инсулина короткого
Приведем пример подбора инсулинотерапии больному 23 лет с массой тела 70 кг, поступившему в терапевтическое отделение по поводу впервые выявленного диабета с гликемией 18,6 ммоль/л и отрицательной реакцией мочи на ацетон. В день поступления назначено Дробное введение суинсулина: перед завтраком 12 ЕД, перед обедом 12 ЕД и перед ужином 8 ЕД. После снижения утренней гликемии до 11,8 ммоль/л назначено: утром 10 ЕД ИЦС и 8 ЕД суинсулина, днем 8 ЕД и вечером 6 ЕД суинсулина. После снижения гликемии до 6,4 ммоль/л суточная доза инсулина снижена: утром—8 ЕД ИЦС и 6 ЕД суинсулина, днем-6 ЕД и вечером 4 ЕД суинсулина. Затем больной переведен на 2 инъекции: перед завтраком - ИЦС 6 ЕД, ИЦСА 6 ЕД, суинсулин 4 ЕД, перед ужином суинсулина 6 ЕД.
Как показывает клинический опыт, нерациональное использование всех возможностей современной инсулинотерапии часто приводит к лечебным ошибкам, итогом которых является отсутствие у больного стойкой компенсации со значительными повышениями гликемии в определенное время суток, высокой глюкозурией, частыми гипогликемическими состояниями, наклонностью к кетоацидотическим эпизодам. Иногда это приводит к ложному заключению о лабильном течении диабета.
Е П Тихонова и соавт. (1980) проанализировали ошибки инсулинотерапии у 1486 больных, госпитализированных в клинику в связи с неэффективностью лечения различными препаратами инсулина по месту жительства. Эти ошибки, относящиеся к практике лечения ИЗСД, сводятся к следующему Во-первых, часто не достигается соответствие между инсулинемией и гликемией на протяжении суток.
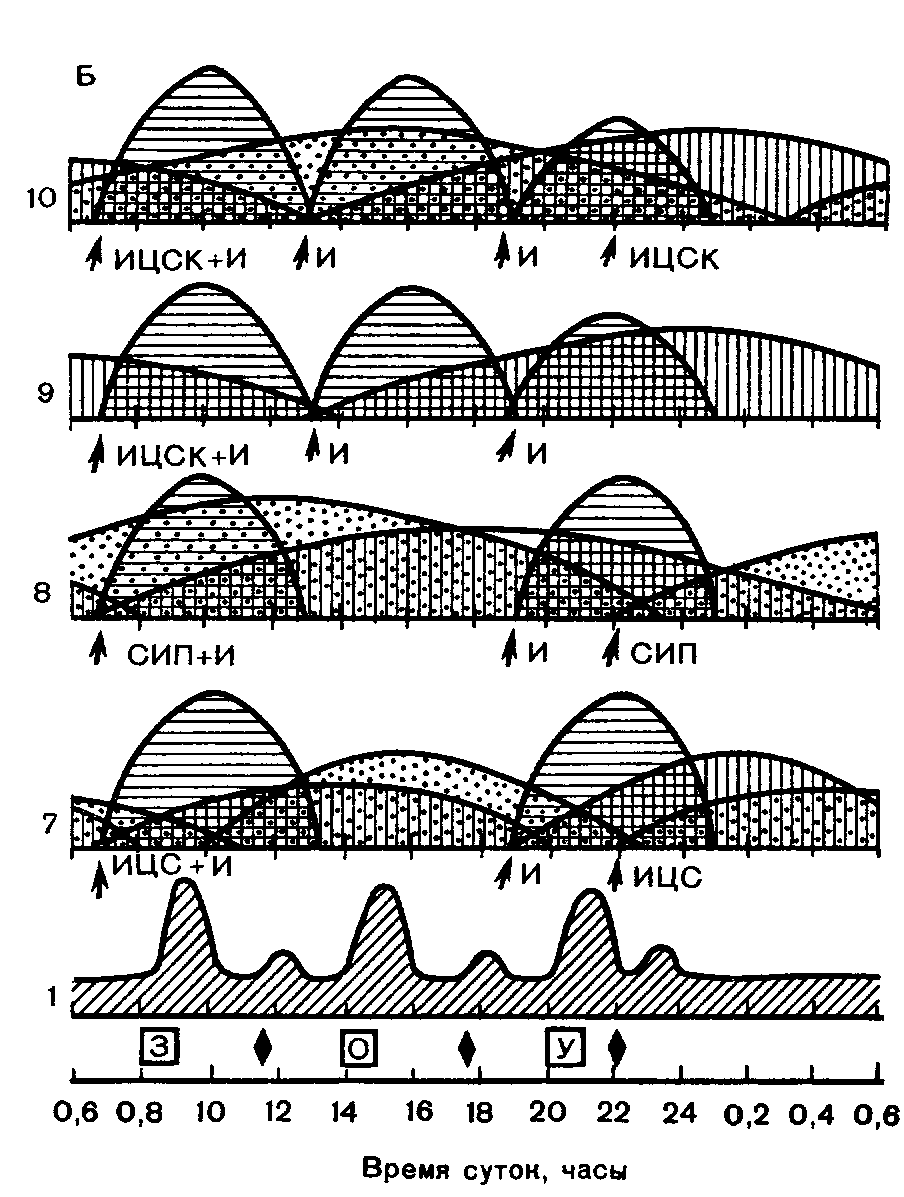
действия и введении СИП утром и на ночь, 9 — колебания инсулинемии при троекратном введении инсулина короткого действия и утреннем введении ИЦСК, 10 — колебания инсулинемии при троекратном введении инсулина короткого действия и введении ИЦСК утром и на ночь.
Во-вторых, причина неэффективности лечения нередко кроется в несоблюдении больным предписанного режима питания. Это выражается в превышении допустимой энергетической ценности пищи, произвольном изменении количества потребляемых углеводов, отсутствии четко фиксированного времени приема пищи, беспорядочном распределении углеводосодержащих продуктов в суточном рационе. Значение этого в плохой компенсации диабета подчеркивают и другие авторы, указывающие, что большая часть больных в течение всей жизни практически находятся на “свободной диете” [Касаткина Э. П., 1986]. К сожалению, обучение больных диабетом самоконтролю, рациональному образу жизни, основам диететики занимает недостаточное место в санитарно-просветительной работе.
В-третьих, до сих пор врачи пытаются во что бы то ни стало добиться компенсации диабета путем однократного введения всей суточной дозы инсулина, причем она нередко достигает 80—100 ЕД и более. Как уже подчеркивалось, только дву-, а при необходимости и троекратное введение инсулина в течение суток позволяет избежать значительных колебаний уровня сахара крови от нормо- и даже гипогликемии до гипергликемии. Конечно, такой режим терапии неудобен, а иногда очень обременителен для больного. В связи с этим переориентация больных диабетом на постоянное дробное введение препаратов инсулина требует большой разъяснительной работы, терпения и настойчивости.
В последнее время неоправданное завышение доз инсулина, препятствующее достижению компенсации, связывают с развитием синдрома хронической передозировки инсулина, или синдрома Сомоджи.
Стремление добиться нормогликемии и аглюкозурии нередко приводит к развитию у больного ИЗСД гипогли-кемических состоянии Диагностика нетипичной гипогликемии представляет иногда значительные трудности. Нерезко выраженная гипогликемия, особенно у больных с вегетативной и соматической нейропатией, может проявляться головной болью, снижением настроения вплоть до выраженной депрессии, нарушением работоспособности, внезапными нарушениями зрения, повышенным аппетитом, немотивированным негативизмом в поведении и т. д. Ночная гипогликемия, возникающая в связи с передозировкой препарата с ночным пиком активности, проявляется беспокойством во время сна, кошмарными сновидениями, шумным дыханием, обильным потоотделением. Утром больной просыпается с трудом, с головной болью, усталый, в подавленном настроении.
На снижение уровня сахара крови формируется защитная реакция с активацией симпатико-адреналовой, гипо-таламо-гипофизарно-надпочечниковой систем и высвобождением контринсулярных гормонов адреналина, глюкагона, кортизола, СТГ. В результате содержание глюкозы в крови увеличивается.
Таким образом, после перенесенной ночью гипогликемии, оставшейся нераспознанной, утром у больного обнаруживаются гипергликемия, глюкозурия, иногда ацетонурия. Ориентируясь на эти данные, врач принимает формально логичное, но по существу глубоко ошибочное решение увеличить дозу инсулина. Создается своеобразный порочный круг. Казалось бы, обоснованное наращивание дозы инсулина должно привести к нормализации гликемии, а вместо этого оно еще более дезорганизует регуляцию метаболических процессов: периоды гипогликемии в течение суток чередуются с периодами высокой гипергликемии Появляются устойчивая кетонурия, гиперлипидемия, усиливается гепатостеатоз, диабет приобретает лабильное течение, в связи с перееданием увеличивается масса тела больного Так формируется синдром хронической передозировки инсулина. Определенную роль в лабильности диабета играет нарушение функции печени, обусловленное жировой дистрофией гепатоцитов, снижением содержания в них гликогена Печеночный гликонеогенез при инсулинозависи-мом диабете резко повышен в связи с низкой инсули-немией в воротной вене. Способность печени к стабилизации гликемии при этом существенно ограничивается.
Синдром хронической передозировки инсулина диагностируется на основании тщательного анализа самочувствия больного, а также колебаний гликемии и глюкозурии в течение суток. Особенно внимательным нужно быть при выявлении скрытых гипогликемических состояний. На возможность хронической передозировки инсулина могут указывать постоянно повышенный аппетит с нарастанием массы тела несмотря на декомпенсацию заболевания, увеличение печени, отсутствие видимой причины для стойкой декомпенсации диабета и постоянной наклонности к ацетонурии, увеличение суточной потребности в инсулине до 0,75—0,8 ЕД/кг и больше.
Выявление синдрома передозировки инсулина обязывает к снижению его дозы (прежде всего препаратов ночного действия), переходу на дву-, троекратное введение гормона в течение дня. В среднем дозу инсулина при синдроме Сомоджи снижают на 10—20%, а иногда и больше. Так, в наблюдениях Э. П. Касаткиной, Ю. И. Демидовой (1985), у детей с ИЗСД, получавших инсулин в дозе 0,8 ЕД/(кг-сут), его суммарная доза была снижена на 27,5%, а при исходной дозе—более 1 ЕД/(кг-сут) на 46,5%.
Осложнения инсулинотерапии. К ним относятся гипо-гликемические состояния вплоть до гипогликемической комы (см. главу 7), аллергия к инсулину, инсулинрезистентность, инсулиновые липодистрофии подкожной клетчатки, инсули-новые отеки. Профилактика и лечение этих осложнений представляют значительные сложности.
Термин “инсулинрезистентность” употребляют в двух значениях. В узком смысле слова это потребность больного в экзогенном инсулине более 100 ЕД/сут при отсутствии кетоацидоза, инфекции и сопутствующих эндокринных заболеваний с избыточной выработкой контринсулярных гормонов. В более широком и чаще употребимом значении о резистентности к инсулину говорят тогда, когда суточная доза инсулина превышает обычный дебит нормально функционирующей поджелудочной железы. Так, инсулинрезистентность может сопровождать диабетический кетоацидоз, интеркуррентные инфекционные заболевания, стрессовые ситуации. Из этих представлений, в частности, исходит наиболее принятая в эндокринологических (в том числе отечественных) клиниках классификация инсулинрезистентности, предложенная Jallow, Berson (I960). В соответствии с ней выделяют легкую (80— 125 ЕД/сут), среднюю (125—200 ЕД/сут) и тяжелую (более 200 ЕД/сут) инсулинрезистентность.
Причины истинной инсулинрезистентности разнообразны и не всегда могут быть выяснены с абсолютной достоверностью. Обычно она развивается в течение нескольких недель или месяцев инсулинотерапии, но может обнаружиться немедленно, при первых же попытках применить препараты инсулина. Это связывают с определенной иммунной настроенностью организма, но точный механизм развития инсулинрезистентности неизвестен.
Наиболее очевидная причина инсулинрезистентности — гормональные контринсулярные влияния, реально существующие при таких заболеваниях, как диффузный токсический зоб, феохромоцитома, акромегалия, болезнь и синдром Иценко — Кушинга, Иногда инсулинрезистентность развивается при беременности как следствие гиперпродукции плацентарного лактогена и т. д. У больных сахарным диабетом, как показали работы А. С. Ефимова и соавт. (1983), избыточная активность гормональных контринсулярных факторов как причина резистентности к инсулину в большинстве случаев отсутствует.
Чаще, по современным представлениям, снижение чувствительности к препаратам инсулина обусловлено выработкой нейтрализующих антител к чужеродному белку. Любопытно, что при этом нейтрализация сахароснижающего влияния инсулина редко сочетается с клиническими аллергическими проявлениями. Антителообразование можно считать явлением почти закономерным при инсулинотера-пии. Антитела обнаруживаются уже после нескольких инъекций гормона, и их титр постепенно нарастает. Неясно, однако, почему этот процесс у разных больных имеет разную выраженность, почему в одних ситуациях он ведет к значительному снижению чувствительности к препаратам инсулина, а в других нет.
Считается, что вырабатываются антитела не столько к самой молекуле инсулина, сколько к другим компонентам лекарственного средства: компоненту А (содержащему белковые примеси из клеток поджелудочной железы}, компоненту В, включающему значительные количества проинсулина, и компоненту С, который, кроме чистого инсулина, включает примеси дериватов проинсулина, в которых С-пептид не полностью отделен от А- и В-цепи [Петридес П. и др., 1980]. Все это послужило основанием для создания монопиковых и монокомпонентных препаратов, а также синтеза человеческого инсулина.
Описаны редкие формы диабета, при которых инсулинрезистентность имеет еще более сложный генез. Так, например, известен сахарный диабет, ассоциирующийся со своеобразным поражением слизистых оболочек и кожи — acanthosis nigricans. При одном варианте этого генетического синдрома выявлено снижение числа рецепторов к инсулину в периферических тканях (тип А), при другом (тип В) обнаружено образование антител к этим рецепторам. Высокой инсулинрезистентностью характеризуется так называемый липоатрофический сахарный диабет.
Как показывает практика, чувствительность к инсулину может снижаться при тяжелых паренхиматозных заболеваниях печени. Наложение портокавального анастомоза при внутрипеченочном блоке портального кровотока нередко позволяет снизить компенсирующую дозу инсулина.
Наконец, сама декомпенсация диабета, даже без кетоаци-доза, сопровождается снижением чувствительности к инсулину. Восстановление компенсации обычно позволяет несколько снизить первоначальные дозы инсулина. Еще в 20-е годы В. Г. Баранов обратил внимание на то, что легкие гипогликемические состояния обеспечивают еще большую чувствительность к инсулину.
Выбор средства для преодоления инсулинрезистентности зависит от ее генеза, конечно в той мере, в какой удается его установить. Лучшим способом является перевод больного на высокоочищенный (монопиковый, монокомпонентный) свиной инсулин. Иногда высокую потребность в инсулине удается снизить, заменив свиным инсулином часть общей дозы препаратов, добавив к лечению, например, 8—12 ЕД суинсулина в 1—2 инъекциях.
Некоторые авторы рекомендуют заменить подкожное введение инсулина внутривенным в расчете на быстрое связывание избытка циркулирующих в крови антител. Остальная часть вводимой при этом дозы дает быстрый компенсирующий эффект. При очевидной зависимости низкой чувствительности к инсулину от сопутствующей эндокринной патологии (гипофизарный, стероидный диабет и т. д.) или очаговой латентной инфекции (хронический пиелонефрит, хронический гайморит и т. п.) проводится соответствующая терапия.
При иммунных механизмах инсулинрезистентности (особенно подтвержденных высокими титрами антител к инсулину) целесообразна иммуносупрессивная терапия с помощью глюкокортикоидных гормонов. Испробовали различные режимы такого лечения как по суточной дозировке преднизолона, так и по продолжительности лечения. По одним данным, достаточно 10—15 мг/сут в течение 10 дней (иногда 2—3 нед). Другие авторы предпочитают назначать 60—80 мг/сут не более чем на 10 дней. Во избежание инфекционных осложнений одновременно назначают антибиотики. Применение таких средств, как имуран (азатиоприн) не выявило существенных их преимуществ перед глюкокортикоидами. Изучаются возможности плазма-(Ьереза и гемосорбции для корреции инсулинрезистентности.
Аллергические реакции на инсулин в большинстве случаев связаны с присутствием в препаратах инсулина белковых примесей со значительной антигенной активностью. Антигенные свойства монокомпонентных инсулинов менее выражены по сравнению с другими препаратами инсулина.
Антителообразование происходит практически у всех больных, получающих препараты инсулина, но их титр очень различен. Антитела относятся по преимуществу к классу IgG. Интенсивность антителообразования зависит от сырья (при применении бычьего инсулина она значительнее, чем при использовании свиного), а также технологических особенностей изготовления лекарства. Чаще наблюдаются аллергические реакции на ПЦИ, реже—на простой инсулин, еще реже—на ИЦС. Образование антител к инсулину контролируется генетически, что частично объясняет различную переносимость одного и того же препарата разными больными. По наблюдениям А. В. Древаля (1974), антителообразование интенсивнее при тяжелом диабете и при микроангиопатии, а также при использовании препаратов пролонгированного действия.
Клинически принято различать местные (локальные) и общие (генерализованные) немедленные и замедленные аллергические реакции на инсулин. Локальная реакция возникает в месте введения инсулина, чаще через 1—2 нед после начала лечения, обычно немедленно (в течение первого часа) после инъекции, изредка спустя 6—24 ч. Она выражается в гиперемии и отечности участка кожи диаметром 1—5 см (иногда больше), сопровождаемых жжением, зудом или болью. Иногда реакция проявляется папулезной сыпью, инфильтратом в подкожной клетчатке в месте инъекции, очень редко бывает асептический некроз ткани по типу феномена Артюса. Общая реакция может иметь вид уртикарной зудящей сьши, ангионевротического отека, бронхоспазма, желудочно-кишечных расстройств, полиартрита (чаще полиартралгии), изменений в системе кроветворения (тромбоцитопеническая пурпура, эозинофилия, увеличение лимфатических узлов), наконец, анафилактического шока. Генерализованная аллергическая реакция в большинстве случаев возникает на фоне нарастающей местной реакции на инсулин. К счастью, аллергия становится генерализован-ной относительно нечасто—приблизительно у 0,1% больных, лечащихся инсулином.
Аллергическую реакцию кожи не всегда легко отличить от неаллергического воспаления, связанного с механической травмой (неумелое выполнение инъекций) или химическим раздражением (использование игл и шприцев, хранимых в спирте, введение неподогретых растворов инсулина). В таких случаях проводят аллергическую диагностическую пробу.
Иногда аллергию к инсулину удается устранить без специального лечения: достаточно сменить препарат инсулина (ПЦИ на ИЦС, ИЦС на СИП и т.д.), его серию или использовать тот же препарат, выпускаемый другой фирмой (например, вместо ИЦС — Insulinum lente датского или югославского производства). При возникновении аллергии к инсулину, получаемому из поджелудочных желез крупного рогатого скота, эффективна его замена свиным инсулином, особенно монокомпонентным. Для подавления аллергических реакций используют также антигистаминные средства, при тяжелой генерализованной аллергии — глюкокортикоидные препараты. Если возможно, то инсулинотерапию заменяют пероральными сахароснижающими препаратами.
Принципиально важен вопрос: допустимо ли продолжение инсулинотерапии при местной, и тем более общей аллергической реакции на инсулин? Считается, что если лечение инсулином показано больному, то при наличии только кожной реакции оно может быть продолжено, но под строгим врачебным контролем в стационаре. Приблизительно в Уз таких случаев происходит спонтанная гипосенсиби-лизация, и изменения кожи самостоятельно проходят. Если местные проявления аллергии сохраняются, несмотря на указанные мероприятия, то больному проводят гипосенсиби-лизацию к инсулину. Так же поступают при общей аллергической реакции, за исключением тех случаев, где инсули-нотерапия должна быть продолжена по жизненным показаниям—диабетическая прекома или кома [Древаль А. В., 1979].
Специфическую гипосенсибилизацию (десенсибилизацию) можно проводить быстро или медленно. Первый вариант применяют тогда, когда инсулинотерапию нельзя отменить более чем на 2—3 сут. Используют различные схемы быстрой гипосенсибилизации. По одной из них начинают с введения Уюоо ЕД инсулина. В течение первых суток вводят последовательно 1/1000, 1/500, 1/250 и 1/125 ЕД, на вторые сутки -1/100, 1/50, 1/25 и 1/12 ЕД, на третьи сутки -1/5, 1/2, 1 и 2 ЕД. На четвертые сутки дозу инсулина постепенно доводят до терапевтически эффективной. В клинике
ИЭЭиХГ АМН СССР быструю гипосенсибилизацию начинают с дозы 0,02—0,04 ЕД, увеличивая ее в 2 раза через каждые 2—3 ч. Если очередная доза вызывала местную аллергическую реакцию, то несколько раз повторяют введение предыдущей дозы.
Если жизненных показаний к инсулинотерапии нет, то гипосенсибилизацию ведут медленно. Дозу инсулина, начиная с у) ооо-Vi оооо ЕД, доводят до терапевтической в течение 10 дней — 2—3 мес.
Иногда через несколько месяцев после успешной гипо-сенсибилизации при продолжающейся инсулинотерапии аллергическая реакция на инсулин (обычно местная) возникает снова. В таких случаях рекомендуется провести 2—3 повторных курса гипосенсибилизации.
Липодистрофии— очаговые нарушения липогенеза и липолиза, возникающие в подкожной жировой клетчатке в местах инъекций инсулина. Чаще наблюдается липоатро-фия, т. е. участки рассасывания подкожной жировой ткани различного размера, от небольшого углубления до ямки диаметром до 10—12 см. Значительно реже бывает избыточное жирообразование, напоминающее липоматоз с фиброзным изменением подкожной клетчатки.
Липодистрофии возникают в различные сроки от начала инсулинотерапии (от 1 мес до нескольких лет), при введении разных доз практически любого препарата инсулина, полученного из поджелудочных желез крупного рогатого скота, но чаще ПЦИ. Причины их развития до сих пор неясны. В настоящее время развитие Липодистрофии объясняют аутоиммунными процессами в местах инъекций. Существует также предположение о роли нейродистрофических изменений в тканях, что подтверждается существованием так называемой реципрокной Липодистрофии. Считают, что липодистрофия является следствием длительной травмати-зации периферических нервных волокон при инъекциях. При этом, по-видимому, имеет значение не только механическое, но и химическое и термическое раздражение (кислая реакция некоторых препаратов инсулина, влияние консервантов, липолитический эффект примеси панкреатической липазы, попадание в подкожную клетчатку спирта, которым обрабатывается кожа, реакция антиген — антитело, раздражающее действие охлажденного препарата). Развитию липоатрофий способствует частое введение инсулина в одно и то же место, нарушение правил выполнения инъекций. Поразительно, что иногда липоатрофия возникает на значительном удалении от места инъекций. Трудно объяснить и то, что липоатрофические изменения при одних и тех же условиях инсулинотерапии возникают не у всех, а у меньшей части больных. Однажды возникнув, липоатрофические дефекты могут прогрессировать, регрессировать, а в исключительных случаях подвергаются спонтанному обратному развитию.
Лучшим средством лечения является введение в липоатрофические участки суинсулина. Инъекции делают ежедневно, свиной инсулин вводят в дозе 4—10 ЕД. Уменьшение тканевого дефекта становится очевидным уже после 4— 5 инъекций, а через 2--4 мес ямки почти полностью заполняются жировой тканью. В большей части случаев удается добиться полной ликвидации липоатрофий или их уменьшения [Клячко В. Р., Тиркина Т. Н., 1963]. Еще лучшие результаты (80% улучшений) дает применение монопикового инсулина.
В. В. Талантов (1982) предложил в пограничные участки липоатрофий вводить в одном шприце с лечебной дозой инсулина приблизительно равный объем 0,5% раствора новокаина. Смесь, подогретую до температуры тела, вводят медленно ежедневно, а при ограниченных дефектах подкожного жирового слоя 1 раз в 2—3 дня. По данным автора, эффект наступает через неделю и достигает максимума в сроки от 2—3 нед до 2—4 мес после начала лечения.
Хотя инсулиновая липодистрофия знаменует собой в основном чисто косметический дефект, больные диабетом, как правило, бывают психологически тяжело травмированы этим осложнением. В связи с этим профилактика липоди-строфий должна занимать должное место в лечении больных. Больной должен пользоваться только острой иглой, стерилизуя ее кипячением, перед инъекцией надо дождаться испарения спирта с обработанного им участка кожи, содержимое шприца подогревать до температуры кожи, вводить лекарство медленно. Игла должна быть направлена строго перпендикулярно поверхности кожи и войти в ткани не менее чем на 1/2 -3/4 толщины подкожного жирового слоя. Совершенно обязательно постоянно менять места инъекций, между инъекциями в одно и то же место должно пройти около 2 мес.
Инсулиновые отеки относятся к преходящим, не имеющим серьезного прогностического значения явлениям, возникающим в начале инсулинотерапии у больных диабетом, ранее плохо контролируемым. Ф. Фелиг (1985) объясняет их задержкой инсулином натрия, а также восстановлением нормального объема внеклеточной жидкости по мере снижения глюкозурии и осмотического диуреза. Отеки проходят самостоятельно и специального лечения не требуют.
