
- •660025, Г. Красноярск, ул. Вавилова, 66 а
- •1.1.Распространение в природе и получение
- •1.2 Физические свойства
- •Химические свойства
- •Соединения s – металлов
- •1.6.Применение
- •Элементы іііа – группы
- •Распространение в природе и получение
- •Физические свойства
- •Химические свойства
- •Соединения металлов
- •2.1.4. Применение
- •Глава 3. Химия переходных металлов
- •В периоде с ростом z восстановительные свойства металлов уменьшаются, достигая минимума у элементов iв группы (табл.3.1.). Тяжелые металлы viiiв и iв групп за свою инертность названы благородными.
- •3.1. Элементы 1в группы
- •3.1.1. Распространение в природе и получение
- •3.1.2.Физические свойства
- •3.1.3. Химические свойства
- •3.1.4. Соединения металлов
- •3.1.5.Применение
- •3.2. Элементы подгруппы II a
- •3.2.1.Распространение в природе и получение
- •3.2.2.Физические свойства
- •3.2.3. Химические свойства По химическим свойствам Zn и его аналоги менее активны, чем подгруппа Са. В ряду от Zn к Hg-химическая активность металлов уменьшается (см. Табл.3.3.).
- •3.2.4. Соединения металлов
- •3.2.5. Применение
- •3.3. Элементы подгруппы iiia
- •3.3.1. Способы получения
- •3.3.2.Физические и химические свойства
- •3.3.3. Соединения металлов
- •3.3.4. Применение
- •3.4. Элементы подгруппы ivb
- •3.4.1.Распространение в природе и получение
- •3.4.2.Физические свойства
- •3.4.3. Химические свойства
- •3.4.4. Соединения металлов
- •3.4.5. Применение
- •3.5. Элементы подгруппы vb
- •3.5.1.Распространение в природе и получение
- •3.5.1.Физические свойства
- •3.5.2. Химические свойства
- •3.5.4. Cоединения металлов
- •3.5.5.Применение
- •3.6. Элементы подгруппы viв
- •3.6.1. Распространение в природе и получение
- •В промышленности чистый хром получают из хромистого железняка:
- •Вольфрам, молибден получают из соответствующих оксидов, например:
- •3.6.2.Физические свойства
- •3.6.3. Химические свойства
- •3.6.4. Соединения металлов
- •3.6.5. Применение
- •3.8. Элементы подгруппы VII b
- •3.8.1. Распространение в природе и получение
- •3.8.2.Физические свойства
- •3.8.4. Химические свойства
- •3.8.5.Соединения металлов
- •3.8.6. Применение
- •3.9.2. Физические свойства
- •3.9.3. Химические свойства
- •3.9.4.Соединения металлов
- •3.9.5. Применение
- •3.9. Элементы VIII в группы (платиновые металлы)
- •3.9.1. Распространение в природе и получение
- •В виде соединений находятся в Си- Ni сульфидных рудах.
- •3.9.2. Физические свойства
- •3.9.3. Химические свойства
- •3.9.4.Соединения металлов
- •3.9.5.Применение
- •Глава 4. Лантаноиды и актиноиды
- •4.1. Электронные конфигурации атомов лантаноидов и актиноидов и их свойства.
- •4. 1.1.Монотонно изменяющиеся
- •4.1.2.Периодически изменяющиеся свойства
- •4.2.Распространение f - элементов в природе и получение
- •4.3.Разделение смеси соединений лантаноидов (актиноидов)
- •4.3.1.Ионообменная хроматография
- •4. 3.2.Жидкостная экстракция
- •4.3.3.Разделение по изменению степени окисления
- •4.4.Физические свойства
- •4.5.Химические свойства
- •4.6.Соединения f-металлов
- •4.7.Применение
Элементы іііа – группы
К металлам ІІІА группы относятся алюминий (Al), галлий (Ga), индий (Jn), таллий (Tl). Атомы этих элементов имеют по три валентных электрона (ns2 np1). В невозбужденном состоянии неспарен только один р- электрон, в возбужденном – три электрона. Соответственно эти элементы могут проявлять степени окисления +1 и +3, однако с увеличением радиуса атома участие s2 – электронов в образовании связей уменьшается. Особенно инертна электронная пара 6s2 (Tl 6s2 6p1), поэтому таллий в соединениях обычно проявляет степень окисления +1.
A
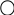

 l
Ga
Jn
Tl
l
Ga
Jn
Tl
+3 +3 +3 +1, +3

Распространение в природе и получение
В свободном состоянии элементы ІІІА – группы в природе не встречаются. Наиболее распространенным из них является алюминий (8 масс.%), он занимает третье место по распространенности после кислорода и кремния и первое место среди металлов. Алюминий образует в природе многочисленные алюмосиликаты, часто очень сложного состава – K(AlSi3O8) – ортоклаз, Al4(OH)8(Si4O10) – каолин, (Na,K)(AlSiO4)- нефелин, K[Al3(OH)6(SiO4)2] – алунит. При выветривании алюмосиликатов образуются бокситы – Al2O3*nН2О. Около 50% мировых запасов бокситов сосредоточено в Австралии, 26% - в Африке.
У нас в стране отсутствуют высококачественные бокситы, поэтому алюминиевая промышленность стала использовать нефелины и алуниты. Галлий, индий и таллий – редкие и рассеянные элементы. Они встречаются в виде примесей к природным соединениям Zn, Pb, Fe, Cu и Al. Известен минерал галит CuGaS2.
Основой для производства Al является искусственно получаемый продукт – глинозем, технология производства которого целиком определяется используемым сырьем – бокситовым или нефелиновым.
Бокситы обычно вскрывают раствором едкого натра по методу Байера при 200 – 220 0С, комплексную переработку нефелинов осуществляют спеканием с содой или известняком при t ~ 1200 0С. Сейчас разработаны и внедрены смешанные технологии, например, последовательная технология Байер – спекание, по которой из исходного низкокачественного боксита по схеме Байера извлекают Al(ОН)3, а осадок, содержащий Fe и Si (красный шлам), перерабатывают методом спекания. Широко используется в мире параллельная схема, по которой часть боксита направляют на байеровскую ветку, а высококремнистый боксит спекают с содой или известняком.
Одна из принципиальных схем:
Al2O3 NaAlO2
Fe2O3 + Na2CO3
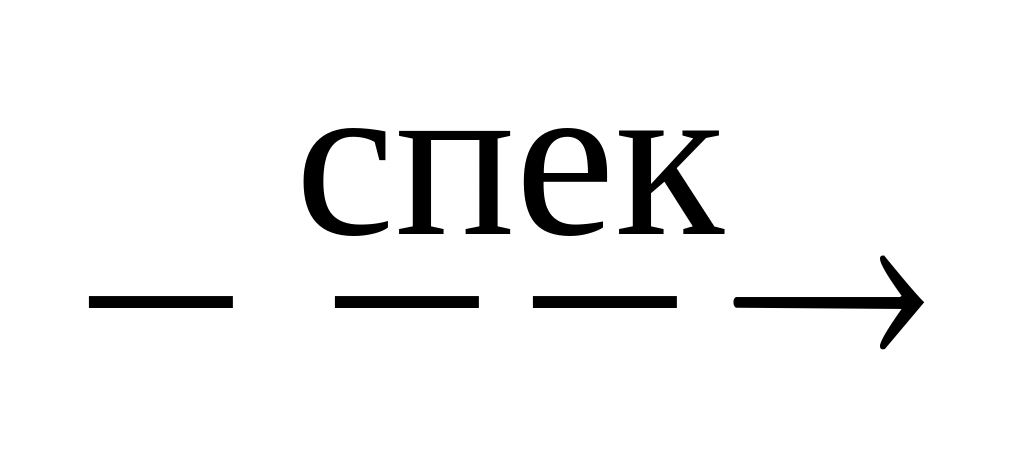 2
NaFeO2
+ CO2
2
NaFeO2
+ CO2
SiO2 Na2SiO3
Выщелачивание спека водой
NaFeO2 + 2 H2O = Fe(OH)3 + NaOН
Обработка известковым молоком в автоклаве
Na2SiO3 + Ca(OH)2 = CaSiO3 + 2NaOH
После отделения путем фильтрации Fe и Si осаждают из раствора Al(ОН)3:
2NaAlO2 + CO2 + H2O
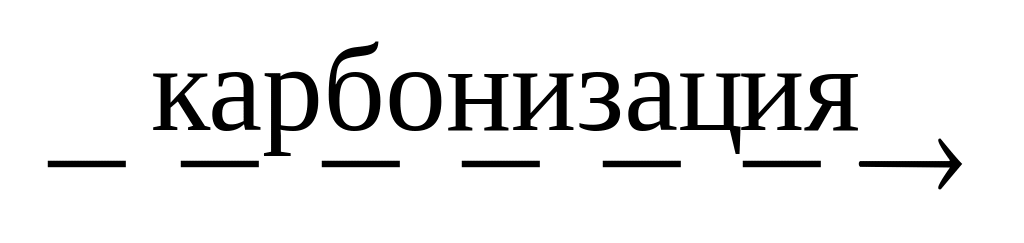 2Al(OH)3
+ Na2CO3
2Al(OH)3
+ Na2CO3
2Al(OH)3
![]() Al2O3
+ 3 H2O
Al2O3
+ 3 H2O
выход 50 – 60%
Алюминий получают электролизом расплава глинозема Al2О3 в криолите Na3AlF6, с содержанием глинозема 6 – 8% при температуре 9500С.
Для увеличения электропроводности и снижения температуры плавления (tпл. Al2О3 = 2050 0С) к расплаву добавляют соли AlF3, CaF2, MgF2. При этом сам жидкий алюминий является катодом и собирается на дне ванны, в то время как угольный анод, вертикально опущенный в расплав, выгорает до смеси оксидов углерода. Сила тока в электролизере достигает 80 – 150кА при напряжении 4 – 5В. Сложные реакции, протекающие на электродах, можно представить следующим образом:
Al2O3 Al3+ + AlO33-
катод (-) Al3+ + 3е- → Al
анод (+) AlO33- + 3С – 6е- → Al3+ + 3СО
Производство Al – энергетически емкий процесс. Добавление к электролиту LiF, LiCl позволяет повысить производительность электролизеров, снизить расход электроэнергии, анодной массы, понизить температуру расплава электролита.
Галлий получают из бокситов при производстве алюминия в виде Ga(OH)3, индий и таллий из руд цветных металлов (Zn, Pb, Cu, Fe). Их отходы выщелачивают кислотами, затем экстрагируют и выделяют цементацией или электролизом.
2JnCl3 + 3Zn = 3ZnCl2 + 2Jn
Tl2SO4 + Zn = 3ZnSO4 + 2Tl
Галлий выделяют электролизом из Ga(OH)3 в расплаве NaOH (при соотношении 1: 6), Jn – при электролизе расплава JnCl3.
