
- •660025, Г. Красноярск, ул. Вавилова, 66 а
- •1.1.Распространение в природе и получение
- •1.2 Физические свойства
- •Химические свойства
- •Соединения s – металлов
- •1.6.Применение
- •Элементы іііа – группы
- •Распространение в природе и получение
- •Физические свойства
- •Химические свойства
- •Соединения металлов
- •2.1.4. Применение
- •Глава 3. Химия переходных металлов
- •В периоде с ростом z восстановительные свойства металлов уменьшаются, достигая минимума у элементов iв группы (табл.3.1.). Тяжелые металлы viiiв и iв групп за свою инертность названы благородными.
- •3.1. Элементы 1в группы
- •3.1.1. Распространение в природе и получение
- •3.1.2.Физические свойства
- •3.1.3. Химические свойства
- •3.1.4. Соединения металлов
- •3.1.5.Применение
- •3.2. Элементы подгруппы II a
- •3.2.1.Распространение в природе и получение
- •3.2.2.Физические свойства
- •3.2.3. Химические свойства По химическим свойствам Zn и его аналоги менее активны, чем подгруппа Са. В ряду от Zn к Hg-химическая активность металлов уменьшается (см. Табл.3.3.).
- •3.2.4. Соединения металлов
- •3.2.5. Применение
- •3.3. Элементы подгруппы iiia
- •3.3.1. Способы получения
- •3.3.2.Физические и химические свойства
- •3.3.3. Соединения металлов
- •3.3.4. Применение
- •3.4. Элементы подгруппы ivb
- •3.4.1.Распространение в природе и получение
- •3.4.2.Физические свойства
- •3.4.3. Химические свойства
- •3.4.4. Соединения металлов
- •3.4.5. Применение
- •3.5. Элементы подгруппы vb
- •3.5.1.Распространение в природе и получение
- •3.5.1.Физические свойства
- •3.5.2. Химические свойства
- •3.5.4. Cоединения металлов
- •3.5.5.Применение
- •3.6. Элементы подгруппы viв
- •3.6.1. Распространение в природе и получение
- •В промышленности чистый хром получают из хромистого железняка:
- •Вольфрам, молибден получают из соответствующих оксидов, например:
- •3.6.2.Физические свойства
- •3.6.3. Химические свойства
- •3.6.4. Соединения металлов
- •3.6.5. Применение
- •3.8. Элементы подгруппы VII b
- •3.8.1. Распространение в природе и получение
- •3.8.2.Физические свойства
- •3.8.4. Химические свойства
- •3.8.5.Соединения металлов
- •3.8.6. Применение
- •3.9.2. Физические свойства
- •3.9.3. Химические свойства
- •3.9.4.Соединения металлов
- •3.9.5. Применение
- •3.9. Элементы VIII в группы (платиновые металлы)
- •3.9.1. Распространение в природе и получение
- •В виде соединений находятся в Си- Ni сульфидных рудах.
- •3.9.2. Физические свойства
- •3.9.3. Химические свойства
- •3.9.4.Соединения металлов
- •3.9.5.Применение
- •Глава 4. Лантаноиды и актиноиды
- •4.1. Электронные конфигурации атомов лантаноидов и актиноидов и их свойства.
- •4. 1.1.Монотонно изменяющиеся
- •4.1.2.Периодически изменяющиеся свойства
- •4.2.Распространение f - элементов в природе и получение
- •4.3.Разделение смеси соединений лантаноидов (актиноидов)
- •4.3.1.Ионообменная хроматография
- •4. 3.2.Жидкостная экстракция
- •4.3.3.Разделение по изменению степени окисления
- •4.4.Физические свойства
- •4.5.Химические свойства
- •4.6.Соединения f-металлов
- •4.7.Применение
3.6. Элементы подгруппы viв
Побочную подгруппу VI группы периодической системы составляют хром Cr, молибден Mo, вольфрам W. Электронная конфигурация их валентного слоя nS2(n-1)d4, однако у Cr и Mo наблюдается “проскок электрона”:Cr 4s1 3d5; Mo -5s1 4d5. Устойчивые степени окисления: Cr +2, ( +3), +6, Mo (+6) возможна +4, +3, W ( +6), редко +5.
Являясь типичными d- металлами Cr, Mo, W образуют комплексные соединения с координационными числами 6 и 4, известны комплексы для Мо и W с к.ч. = 8.
3.6.1. Распространение в природе и получение
Все три представителя VI B-группы относятся к довольно распространенным элементам. Хром по распространенности превосходит, например, кобальт и никель. В природе встречаются исключительно в связанном состоянии и образуют самостоятельные месторождения, а также входят в состав полиметаллических руд. Самым распространенным минералом хрома является Fe(CrO2)2 или FeO Cr2O3- хромистый железняк,
или Cr2O3 хромовая охра, молибдена MoS2 молибденит (молибденовый блеск), вольфрами, CaWO4 шеелит, (Fe, Mn)WO4 вольфрамит, WO3 вольфрамовая охра, WS2 вольфрамовый блеск.
В промышленности чистый хром получают из хромистого железняка:
Окислительной плавкой с карбонатом натрия:
4FeOCr2O3 + 8Na2CO3 + O2 =2Fe2O3 + 8Na2CrO4 + 8CO2
2. Хромат восстанавливают углеродом:
2Na2CrO4+ 3C = Сr2O3 + 2Na2O + 3CO
3. Алюмотермия оксида хрома (III): Сr2O3 + 3А1 = 3Сr + А12O3
Вольфрам, молибден получают из соответствующих оксидов, например:
CaWO4 + 2 HCI = H2WO4 + CaCI2
H2WO4
![]() WO3
+ 3 Н2О
WO3
+ 3 Н2О
МоО3
+ Н2
![]() Мо + 3 Н2О
Мо + 3 Н2О
Чистота металлов составляет 98%. Чистые металлы получают электролизом расплава (K3MoCI6) или сернокислого раствора Сr2 (SO4)3 .. Чистота полученных таким способом металлов 99,5 %.
3.6.2.Физические свойства
Металлы Cr, Mo, W- в компактном состоянии блестящие серо-белые металлы, парамагнитные. Их относят к тяжелым и тугоплавким металлам (см.табл.3.8 .). Вольфрам является одним из тугоплавких металлов.
Таблица 3.8.
Основные характеристики элементов подгруппы хрома
-
металл
R ат., нм
Плотность, г/см3
J ион., эВ
T пл.., 0C
Tкип.,0C
Содержание в земной коре, %
Относительная электроотрицательность по Полингу
Cr
0,127
7,29
6,77
1875
2680
2102
1,6
Mo
0,139
10,22
7,10
2620
4630
3104
1,8
W
0,140
19,35
7,98
3395
5680
1104
1,7
В чистом виде легко поддаются механической обработке, однако технический Cr – очень тверд, а чистый Cr – пластичен.
3.6.3. Химические свойства
Химическая активность подгруппы хрома уменьшается от Cr к W. В обычных условиях эти металлы довольно инертны, т.к. покрыты оксидной пленкой.
Отношение к неметаллам подгруппы хрома можно представить в виде схемы:
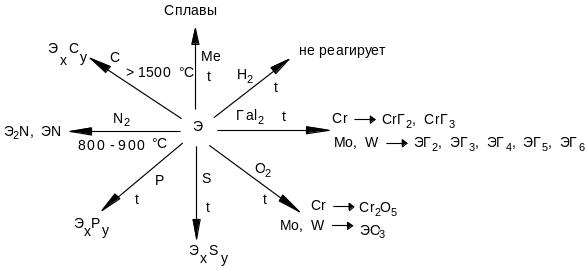
При нагревании взаимодействуют почти со всеми неметаллами, с образованием: оксидов Сr2O3; MoO6; хлоридов СrCI3; WCI6. Чистый хром может поглощать водород, а молибден и особенно вольфрам водород практически не растворяют.
Известны: нитриды - CrN; Mo2N; WN2; карбиды -Cr3C2; Mj2C; WC; бориды -WB; сульфиды -Cr2S3; MoS2; WS3 и др. Это нестехиометричные, тугоплавкие твердые соединения, устойчивы к действию химических реагентов. Кроме того, они реагируют с большинством металллов с образованием твердых растворов или интерметаллических соединений.
Отношение к кислотам Взаимодействие Cr, Мо и W с агрессивными средами определяется как химической активностью металла, так и степенью пассивации его поверхности оксидными пленками. Наиболее сильно пассивирует Cr. В обычном состоянии он пассивирует в Н2О и HNO3. если эту пленку разрушить химически или термически, то металлы легко реагируют с сильными кислотами и их смесями. Это можно представить схемой:
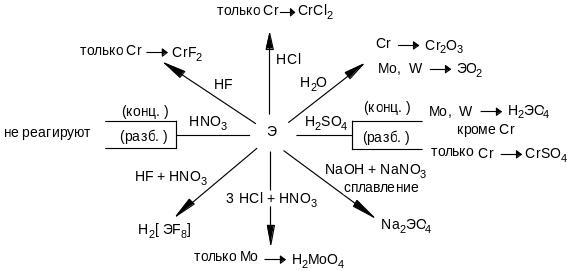
Cr–металл средней активности (-0,74в), в ряду напряжений он расположен между цинком и железом, а Мо и W возле Н ,т.е. малоактивны:
Элемент Э2+ /Э Э+3/Э
Cr 0,913 0,744
Мо 0,200
W 0,15
Хром растворяется в разбавленных кислотах (HCI и H2SO4), с образованием солей хрома (П). При нагревании он взаимодействует с водой, например:
2Cr
+ 3Н2О
![]() Cr2O3
+ 3H2
Cr2O3
+ 3H2
При обычных условиях концентрированные кислоты (HNO3, H2SO4) пассивируют Cr u W, а при нагревании металлы растворяется. Хром образует соли (III), молибден и вольфрам оксиды или кислоты в высшей степени окисления, например:
Cr + 6 HNO3(конц) = Cr (NO3)3 + 3NO2 + 3H2O
W + 6HNO3 = WO3 + 6NO2 + 3H2O, (Mo)
Mo + 3H2SO4 H2MoO4 + 3SO2 + 2H2O
Лучшим растворителем для Мо и W является горячая смесь кислот:
Мо + 8HF + 6HNO3= H2MoF8 + 6NO2 + 6Н2О
и расплавы щелочей в присутствии окислителей: например:
Cr + NаCIO3 + 2NaOH = Na2CrO4 + NaCI + H2O
При этом образуются хроматы, молибдаты и вольфраматы.
