
- •660025, Г. Красноярск, ул. Вавилова, 66 а
- •1.1.Распространение в природе и получение
- •1.2 Физические свойства
- •Химические свойства
- •Соединения s – металлов
- •1.6.Применение
- •Элементы іііа – группы
- •Распространение в природе и получение
- •Физические свойства
- •Химические свойства
- •Соединения металлов
- •2.1.4. Применение
- •Глава 3. Химия переходных металлов
- •В периоде с ростом z восстановительные свойства металлов уменьшаются, достигая минимума у элементов iв группы (табл.3.1.). Тяжелые металлы viiiв и iв групп за свою инертность названы благородными.
- •3.1. Элементы 1в группы
- •3.1.1. Распространение в природе и получение
- •3.1.2.Физические свойства
- •3.1.3. Химические свойства
- •3.1.4. Соединения металлов
- •3.1.5.Применение
- •3.2. Элементы подгруппы II a
- •3.2.1.Распространение в природе и получение
- •3.2.2.Физические свойства
- •3.2.3. Химические свойства По химическим свойствам Zn и его аналоги менее активны, чем подгруппа Са. В ряду от Zn к Hg-химическая активность металлов уменьшается (см. Табл.3.3.).
- •3.2.4. Соединения металлов
- •3.2.5. Применение
- •3.3. Элементы подгруппы iiia
- •3.3.1. Способы получения
- •3.3.2.Физические и химические свойства
- •3.3.3. Соединения металлов
- •3.3.4. Применение
- •3.4. Элементы подгруппы ivb
- •3.4.1.Распространение в природе и получение
- •3.4.2.Физические свойства
- •3.4.3. Химические свойства
- •3.4.4. Соединения металлов
- •3.4.5. Применение
- •3.5. Элементы подгруппы vb
- •3.5.1.Распространение в природе и получение
- •3.5.1.Физические свойства
- •3.5.2. Химические свойства
- •3.5.4. Cоединения металлов
- •3.5.5.Применение
- •3.6. Элементы подгруппы viв
- •3.6.1. Распространение в природе и получение
- •В промышленности чистый хром получают из хромистого железняка:
- •Вольфрам, молибден получают из соответствующих оксидов, например:
- •3.6.2.Физические свойства
- •3.6.3. Химические свойства
- •3.6.4. Соединения металлов
- •3.6.5. Применение
- •3.8. Элементы подгруппы VII b
- •3.8.1. Распространение в природе и получение
- •3.8.2.Физические свойства
- •3.8.4. Химические свойства
- •3.8.5.Соединения металлов
- •3.8.6. Применение
- •3.9.2. Физические свойства
- •3.9.3. Химические свойства
- •3.9.4.Соединения металлов
- •3.9.5. Применение
- •3.9. Элементы VIII в группы (платиновые металлы)
- •3.9.1. Распространение в природе и получение
- •В виде соединений находятся в Си- Ni сульфидных рудах.
- •3.9.2. Физические свойства
- •3.9.3. Химические свойства
- •3.9.4.Соединения металлов
- •3.9.5.Применение
- •Глава 4. Лантаноиды и актиноиды
- •4.1. Электронные конфигурации атомов лантаноидов и актиноидов и их свойства.
- •4. 1.1.Монотонно изменяющиеся
- •4.1.2.Периодически изменяющиеся свойства
- •4.2.Распространение f - элементов в природе и получение
- •4.3.Разделение смеси соединений лантаноидов (актиноидов)
- •4.3.1.Ионообменная хроматография
- •4. 3.2.Жидкостная экстракция
- •4.3.3.Разделение по изменению степени окисления
- •4.4.Физические свойства
- •4.5.Химические свойства
- •4.6.Соединения f-металлов
- •4.7.Применение
3.9.2. Физические свойства
Железо, кобальт и никель представляют собой блестящие белые металлы с сероватым(Fe, Со) или серебристым (Ni) оттенком. Они тугоплавкие и тяжелые металлы, обладающие превосходными механическими свойствами и образующие множество сплавов.
Железо обладает хорошей пластичностью и ферромагнитными свойствами (намагничивается и сохраняет свои магнитные свойства по прекращению действия магнитного поля) Имеет четыре изотопа: 54,56 ( основной), 57;58; есть и радиоактивные 55;59. Кобальт более тверд и хрупок.
Таблица 3.11.
Некоторые свойства элементов подгруппы железа
Металл |
R ат., нм |
Плотность, г/см3 |
J ион., эВ |
Стандартный электродный потенциал процесса, В
|
T пл.., 0C |
Tкип.,0C |
Содержание в земной коре, масс.% |
Относительная электроотрицательность по Полингу |
|
Э2+ |
Э+3 |
||||||||
Fe |
0,126 |
7,9 |
7,89 |
-0,44 |
-0,036 |
1539 |
2740 |
4,65 |
1,8 |
Сo |
0,125 |
8,8 |
7,87 |
-0,28 |
0,4 |
1439 |
2255 |
4103 |
1,8 |
Ni |
0,124 |
8,9 |
7,64 |
-0,25 |
- |
1455 |
1728 |
4108 |
1,8 |
.
3.9.3. Химические свойства
Значение стандартных электродных потенциалов этих металлов позволяет отнести их к металлам средней активности. Причем активность в ряду уменьшается.
Отношение к неметаллам. В обычных условиях Со и Ni устойчивы к О2 влажного воздуха а Fe ржавеет:
4 Fe +3О2 + Н2О = 2 Fe2О3n Н2О
При температуре красного каления сгорает, превращаясь в железную окалину Fe3О4.
При нагревании все металлы взаимодействуют с парами Н2О, кислорода, галогенами, серой, углеродом, CO:
3Fe +4Н2О = Fe3О4 + Н2↑ или Co + Н2О = CoO + Н2
3Fe + C = Fe3C
Ni + CI2 = NiCI2
цементит
Схематично взаимодействие металлов подгруппы железа с неметаллами можно представить схемой:
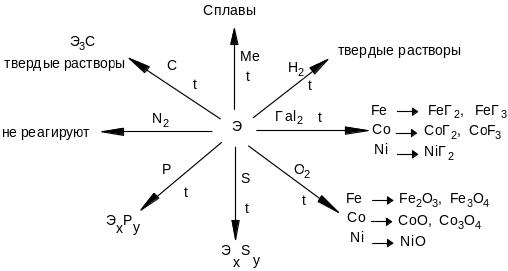
Водород эти металлы растворяет, образуя гидриды состава: МеН, МеН2, МеН3 и МеН4. Наибольшей растворяющей способностью обладает никель, чем объясняется его высокая каталитическая активность в реакциях гидрирования.
С азотом эти металлы непосредственно не реагируют, но косвенным путем можно получить металлоподобные Fe4N; Fe2N. Со2N.
С углеродом образуют металлоподобные карбиды: Ме3С, Ме2С, а с фосфором- Ме3Р2.
Все металлы образуют карбонилы: Ni(CO)4, Fe(CO)5 ,Co(CO)4 или Со2(СО)8, обладающие диамагнитными свойствами.
Отношение к кислотам. В кислотах H2SO4 (разб), НС1, HNO3(разб.) Fe и Со растворяются при обычной температуре, а Ni – при нагревании с образованием солей Ме (II):
Fe + H2SO4 = FeSO4 + H2
5Со + 12HNO3 = 5Со(NO3)2 + N2 + 6H2O
В кислотах – окислителях конц. HNO3 и H2SO4 все металлы пассивируют, но при нагревании растворяются с образованием солей Fe (III), а Со и Ni (II), например:
Fe + 4HNO3 Fe (NO3)3 + NO↑ + 2H2O
Со + 2H2SO4 = СоSO4+ SO2 +2H2О
Царская водка растворяет все металлы:
3 Ni + 2HNO3 +6НС1 NiС12 +2 NO + 4H2O
Схематично отношение металлов семейства железа к кислотам можно представить так:
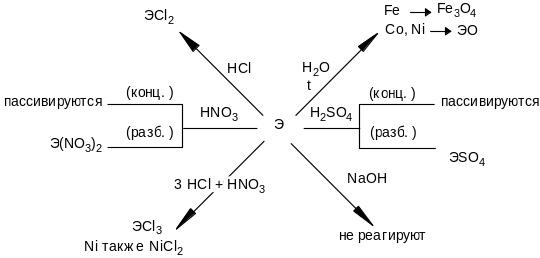
Со щелочами Fe Со и Ni не реагируют.
