
- •660025, Г. Красноярск, ул. Вавилова, 66 а
- •1.1.Распространение в природе и получение
- •1.2 Физические свойства
- •Химические свойства
- •Соединения s – металлов
- •1.6.Применение
- •Элементы іііа – группы
- •Распространение в природе и получение
- •Физические свойства
- •Химические свойства
- •Соединения металлов
- •2.1.4. Применение
- •Глава 3. Химия переходных металлов
- •В периоде с ростом z восстановительные свойства металлов уменьшаются, достигая минимума у элементов iв группы (табл.3.1.). Тяжелые металлы viiiв и iв групп за свою инертность названы благородными.
- •3.1. Элементы 1в группы
- •3.1.1. Распространение в природе и получение
- •3.1.2.Физические свойства
- •3.1.3. Химические свойства
- •3.1.4. Соединения металлов
- •3.1.5.Применение
- •3.2. Элементы подгруппы II a
- •3.2.1.Распространение в природе и получение
- •3.2.2.Физические свойства
- •3.2.3. Химические свойства По химическим свойствам Zn и его аналоги менее активны, чем подгруппа Са. В ряду от Zn к Hg-химическая активность металлов уменьшается (см. Табл.3.3.).
- •3.2.4. Соединения металлов
- •3.2.5. Применение
- •3.3. Элементы подгруппы iiia
- •3.3.1. Способы получения
- •3.3.2.Физические и химические свойства
- •3.3.3. Соединения металлов
- •3.3.4. Применение
- •3.4. Элементы подгруппы ivb
- •3.4.1.Распространение в природе и получение
- •3.4.2.Физические свойства
- •3.4.3. Химические свойства
- •3.4.4. Соединения металлов
- •3.4.5. Применение
- •3.5. Элементы подгруппы vb
- •3.5.1.Распространение в природе и получение
- •3.5.1.Физические свойства
- •3.5.2. Химические свойства
- •3.5.4. Cоединения металлов
- •3.5.5.Применение
- •3.6. Элементы подгруппы viв
- •3.6.1. Распространение в природе и получение
- •В промышленности чистый хром получают из хромистого железняка:
- •Вольфрам, молибден получают из соответствующих оксидов, например:
- •3.6.2.Физические свойства
- •3.6.3. Химические свойства
- •3.6.4. Соединения металлов
- •3.6.5. Применение
- •3.8. Элементы подгруппы VII b
- •3.8.1. Распространение в природе и получение
- •3.8.2.Физические свойства
- •3.8.4. Химические свойства
- •3.8.5.Соединения металлов
- •3.8.6. Применение
- •3.9.2. Физические свойства
- •3.9.3. Химические свойства
- •3.9.4.Соединения металлов
- •3.9.5. Применение
- •3.9. Элементы VIII в группы (платиновые металлы)
- •3.9.1. Распространение в природе и получение
- •В виде соединений находятся в Си- Ni сульфидных рудах.
- •3.9.2. Физические свойства
- •3.9.3. Химические свойства
- •3.9.4.Соединения металлов
- •3.9.5.Применение
- •Глава 4. Лантаноиды и актиноиды
- •4.1. Электронные конфигурации атомов лантаноидов и актиноидов и их свойства.
- •4. 1.1.Монотонно изменяющиеся
- •4.1.2.Периодически изменяющиеся свойства
- •4.2.Распространение f - элементов в природе и получение
- •4.3.Разделение смеси соединений лантаноидов (актиноидов)
- •4.3.1.Ионообменная хроматография
- •4. 3.2.Жидкостная экстракция
- •4.3.3.Разделение по изменению степени окисления
- •4.4.Физические свойства
- •4.5.Химические свойства
- •4.6.Соединения f-металлов
- •4.7.Применение
3.4.5. Применение
Титан и его сплавы отличаются высокой прочностью, легкостью, тугоплавкостью, химической стойкостью при обычной температуре (эти сплавы используются главным образом в самолетостроении и ракетостроении). Высокая прочность титана и его исключительная инертность по отношению к плазме крови и веществам, вырабатываемым организмом человека, делают его незаменимым материалом для протезирования (протезы костей, арматура искусственных сердечных клапанов и др.).
При высокой температуре титан очень активно соединяется с галогенами, кислородом, серой, азотом и углеродом, поэтому его применяют для удаления газов из расплавленного металла и получения однородного литья, а также в вакуумной технике (для получения глубокого вакуума). Оксид титана ТiО2 применяется в качестве катализатора во многих органических синтезах. Белила на основе ТiО2 (так называемые титановые белила) характеризуются высокой прочностью, кислотостойкостью и в отличие от свинцовых белил не ядовиты и не темнеют на воздухе под действием H2S.
Цирконий является конструкционным материалом для атомных реакторов, так как он почти не захватывает медленные (тепловые) нейтроны и обладает высокой стойкостью против коррозии и механической прочностью при высоких температурах. Гафний, наоборот, весьма активно поглощает нейтроны, благодаря чему используется в регулирующих и защитных устройствах атомных реакторов. Оксиды этих металлов применяются при изготовлении тугоплавких стекол и жаропрочной лабораторной аппаратуры.
Вопросы и упражнения
Составьте формулу внешнего валентного слоя элементов подгруппы титана.
Определите характерные степени окисления титана, циркония и гафния.
Кто из металлов этой подгруппы растворим в растворах щелочей? Составьте уравнения реакции.
Как изменяются восстановительные свойства металлов в подгруппе титана сверху вниз.
Получение оксидов металла в высшей степени окисления.
Амфотерность соединений титана.
Оксосоли. Получение. Их устойчивость.
Получение кислот (
 титановая,
титановая,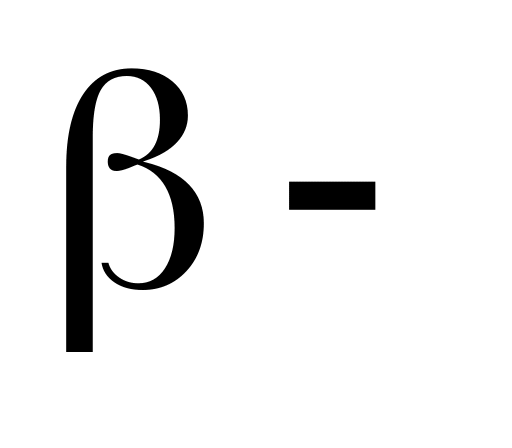 титановая).
Свойства кислот. Почему они растворимы
в растворах HF,
H2SO4.
Составьте соответствующие уравнения
реакций.
титановая).
Свойства кислот. Почему они растворимы
в растворах HF,
H2SO4.
Составьте соответствующие уравнения
реакций.Составьте уравнение реакции:Ti2(SO4)3 + KMnO4 + H2O=….
10. Составьте уравнения реакции протекающей в солянокислой среде между хлоридом титана (+3) и перхлоратом калия.
3.5. Элементы подгруппы vb
Побочную подгруппу V группы периодической системы составляют V, Nb, Ta. Общая электронная формула этой подгруппы: nS2(n-1)d3. Однако для атома Nb наблюдается "провал электрона", т.е. внешний валентный слой 5S24d3 5S14d4. Характерные с.о. для V (+2),+3, (+4), +5; Nb (+5) ; Ta (+5). Координационное числа: V 4,6; Nb,Ta 6,7,8.
3.5.1.Распространение в природе и получение
Соединения ванадия широко распространенны в природе, но они очень рассеянны и не образуют значительных скоплений (см. табл.3.6.). Ниобий и тантал встречаются всегда вместе, содержание их в земной коре еще меньше. Основные минералы: ванадит 3Pb3(VO4)2PbCL2, колумбит-(Fe,Mn)NbO3TaO3, лопарит (Nа,Са)NbO3TaO3, танталит Fe(TaO3)2.
Главным источником ванадия являются железные руды, в которых его содержание составляет 0,1-0,2 %. Поэтому в доменном процессе ванадий значительно переходит в чугун. В производстве стали из ванадистого чугуна получают шлаки, содержащие ортованадат натрия NаVO3:
4FeVO4 + 4NaCL + O2 = 4NaVO3 + 2Fe2O3 + 2CL2
Действуя на ванадат натрия разбавленной серной кислотой выделяют оксид ванадия V2О5. Из оксида ванадий восстанавливают алюминием.
Металлы подгруппы ванадия получают:
металлотермическим восстановлением (Са, AL) оксидов:
3V2O5
+ 10AL
![]() 6 V
+ 5AL2O3
6 V
+ 5AL2O3
металлотермическим восстановлением галогенидов или комплексных фторидов:
NbCI5 + 5Nа 2 Nb + 5 NaCI
K2TaF7 + 5Nа Ta + 5 NaF + 2 KF
электролизом Ме2О5 в расплаве K2МеF7
алюмотермическим восстановлением смеси оксидов этих металлов с оксидами Fе. Получают сплавы феррованадий, ферротантал, которые используют как легирующие добавки к сталям.
