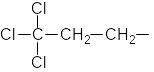- •25.09.01. Предельные углеводороды
- •Лабораторная работа 3. Ароматические углеводороды (арены)
- •Лабораторная работа № 8 Высокомолекулярные соединения
- •Работа №1. Синтез полистирола
- •Электронная теория строения органических соединений.
- •Реакционная способность органических соединений.
- •Вопросы для самопроверки
- •Семинар 2
- •Вопросы для самопроверки
- •Алкины.
- •Вопросы для самопроверки
Электронная теория строения органических соединений.
Электронное строение атома углерода в основном и возбужденном состояниях.
Теория гибридизации атомных орбиталей. Типы гибридных орбиталей, их сравнение (энергия, форма), электроотрицательность атомов в разных гибридных состояниях.
Химическая связь. Ковалентная связь. Способы образования связи (координация и коллигация). Простые и кратные связи. Сравнение свойств - и -связей (энергия, направленность, полярность, поляризуемость).
Электронные эффекты в органических молекулах. Понятие электроотрицательности. Относительные электроотрицательности элементов-органогенов и некоторых функциональных групп по Полингу; электроотрицательные и электроположительные элементы и группы атомов. Полярные и неполярные связи.
Понятие индуктивного эффекта. Природа эффекта, знаки эффекта, графическая символика. Особенности передачи, аддитивный характер индуктивного эффекта.
Сопряженные системы. Виды сопряжения (p,- сопряжение и ,-сопряжение). Элементы теории резонанса. Каноническая форма и резонансный гибрид, графическая символика. Понятие об энергии сопряжения. Мезомерный эффект (эффект сопряжения). Знаки эффекта, особенности передачи. Полярный и неполярный резонанс.
Сверхсопряжение (гиперконъюгация, ,-сопряжение).
Пространственные (стерические, объемные) эффекты в органических молекулах.
Реакционная способность органических соединений.
Общие принципы. Понятие реакционной способности; реагенты и субстраты. Радикальные реагенты (радикалы), гомолитический разрыв связи (гомолиз). Электрофильные и нуклеофильные реагенты, гетеролитический разрыв связи (гетеролиз).
Классификация реакций по результату превращения: замещение, присоединение, отщепление (элиминирование). Классификация органических реакций по типу реагента: радикальные, электрофильные, нуклеофильные. Девять основных типов органических реакций.
Карбокатионы, особенности строения, относительная устойчивость, индуктивная и резонансная стабилизация карбокатионов. Карбанионы: строение, относительная устойчивость, стабилизация. Свободные радиакалы: особенности строения, устойчивость (время жизни), индуктивная и резонансная стабилизация.
Вопросы для самопроверки
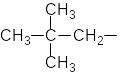
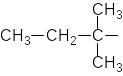
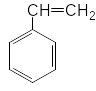
1. Какие из приведенных соединений относятся к органическим?
По какому принципу Вы производили отбор?
2. Перечислите основные постулаты А.М. Бутлерова и проиллюстрируйте на примерах.
3. Какие Вам известны валентные состояния атомов: а) углерода, б) азота, в) кислорода, г) серы, д) фосфора.
4. Приведите примеры неорганических соединений, в которых атомы углерода, кислорода, азота, фосфора и серы находятся в различных валентных состояниях. Определите степени окисления этих атомов.
5. Приведите примеры структурных формул органических соединений с пятью атомами углерода линейного и циклического строения:
а) без гетероатома в цепи (цикле);
б) с атомом кислорода в цепи (в цикле);
в) с двумя атомами азота в цепи (цикле).
6. Перечислите основные классы органических соединений. Определите степени окисления атомов углерода в следующих соединениях:
CH4; CF4; CH3OH; HCOH; CH3COOH; HCN; CH3NH2; CH3NO2
7. Дайте определение понятия "функциональная группа". Какие Вам известны моно- и полифункциональные соединения?
8. Составьте структурные формулы изомеров, имеющих общую формулу С5H12O. Рассмотрите на этом примере виды структурной изомерии.
Сколько геометрических изомеров у
СН3СН=СНСН=СНСН3?
10.Какие из перечисленных ниже соединений будут иметь стереоизомеры: 2-метилбутановая кислота, 3-метилбутановая кислота?
11. Составьте электронные формулы атомов, входящих в состав органических соединений С, О, N, Cl.
12. Какова гибридизация центральных атомов в следующих соединениях: С2Н6, С2Н4, NH3, BF3, SO2, SO3?
13. Сравните основные характеристики - и -связей между атомами углерода: длина связи, энергия связи, поляризуемость, способ образования, реакционная способность.
14. Расположите элементы в ряд по увеличению электроотрицательности: N,F,P,O,I,H,Cl,S,Br,B,Na,Ca,Al,Mg.
15. Расставьте заряды на элементах, входящих в состав следующих молекул: HCN, HCOOH, Na2CO3, CH3COONa, C4H9Li, HOCl, C3H7MgBr, HCl, POCl3, SOCl2.
16. Расположите углеводородные радикалы в порядке возрастания индуктивного эффекта:
а) СН3, С3Н7, С5Н11, С4Н9, С2Н5;
б)
|
|
|
|
|
|
|||
|
|
|
|
|||||
в)
|
|
|
|
|
|
г)
|
|
|
|
17. Составьте возможные канонические формы и резонансные гибриды для следующих соединений:
|
|
|
|
|
|
|
|
|
18. В каких из предложенных соединений имеются подвижные атомы водорода в углеводородном радикале?
|
|
|
||
|
|
|
|
|