
1. Реакции электрофильного присоединения (ае).
Наиболее часто используются реакции присоединения воды. продуктами реакции являются спирты

С =С+
НОН Н+
Н-С-С-ОН
=С+
НОН Н+
Н-С-С-ОН
Реакция проходит в сильно кислой среде, ион Н+ является атакующим электрофилом.
Механизм реакции:
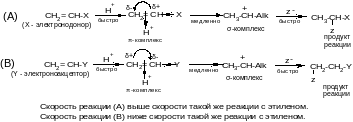
Правило Марковникова:
При присоединении воды или галогеноводорода к алкенам водород присоединяется к наиболее гидрогенизированному атому углерода.
Правило Марковникова соблюдается для углеводородов и для тех производных, которые имеют у двойной связи электронодонорный заместитель. Например:
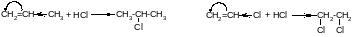
Для соединений, имеющих у двойной связи электроноакцепторный заместитель, реакция идет против правила Марковникова.
Например:
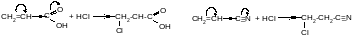
2)Ароматические углеводороды (арены) – это соединения, имеющие циклическую сопряженную ароматическую систему, что определяет их общие признаки в структуре и химических свойствах.
БЕНЗОИДНЫЕ АРЕНЫ

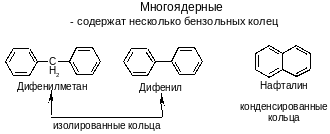
НЕБЕНЗОИДНЫЕ АРЕНЫ
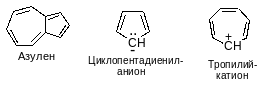
Физические свойства ароматических углеводородов
Бензол – жидкость с т.кип. 80о; производные бензола – более высоко кипящие жидкости или низкоплавкие твердые вещества.
Многоядерные арены – низкоплавкие твердые вещества. Все ароматические углеводороды имеют характерный запах.
1. Реакции электрофильного замещения (SЕ)
Механизм реакций SR:
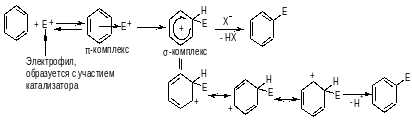
Влияние заместителей на скорость и направление реакцийSЕ.
Различные заместители меняют электронную плотность в бензольном кольце: увеличивают или уменьшают, причем она становится не одинаковой на различных атомах углерода. Это изменяет скорость реакций SЕ и делает её неодинаковой для различных положений цикла.
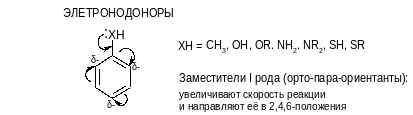
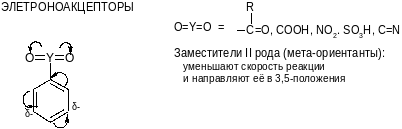
Особое положение занимают галогены: за счет +М-эффекта они ориентируют реакцию в орто- и пара-положения (как заместители I рода), но их –I-эффект по величине превышает мезомерный, общая электронная плотность в кольца снижается и скорость реакции SE уменьшается.
Ориентация в дизамещенных бензола
1. Согласованная ориентация:
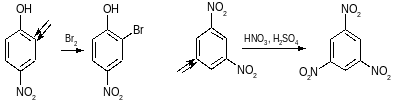
2. При несогласованной ориентации учитываются:
а) влияние более сильно активирующей группы
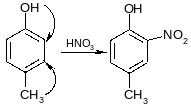
б) пространственные затруднения
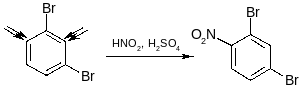
Виды реакций электрофильного замещения
1. Галогенирование
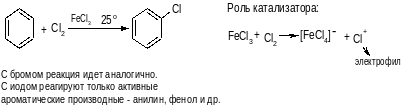
2. Нитрование
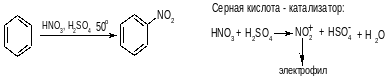
3. Сульфирование
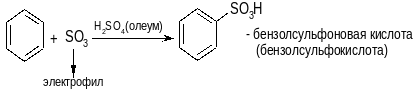
Реакции Фриделя-Крафтса
4. Алкилирование
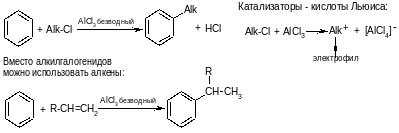
5. Ацилирование
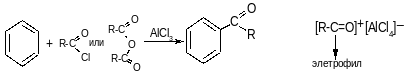
2. Реакции бензола с разрушением ароматической системы
Окисление
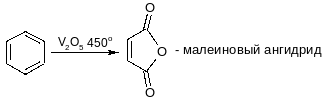
Восстановление (гидрирование)
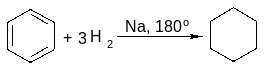
Радикальное хлорирование
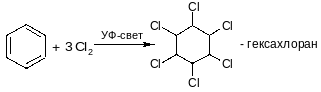
3. Реакции боковых цепей алкилбензолов
Радикальное замещение
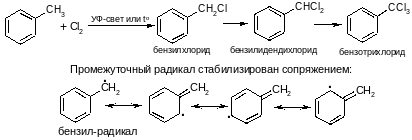
другие алкилбензолы хлорируются в α-положение:
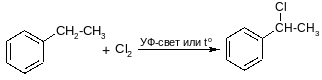
Окисление
Все моноалкилбензолы при окислении KMnO4 в щелочной среде дают бензойную кислоту:
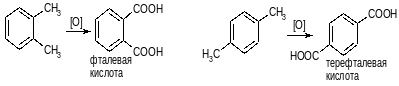
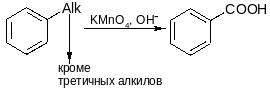 аналогично:
аналогично:
. Реакции многоядерных аренов
Реакции дифениламина
Бензольные кольца дифениламина изолированы, и по реакционной способности он подобен алкилбензолам (толуол):
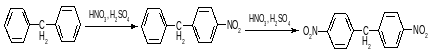
Реакции дифенила Бензольные кольца дифенила сопряжены и почти копланарны. Реакции SE идут поочередно в оба цикла:
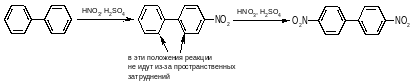
Реакции нафталина
Электрофильное замещение

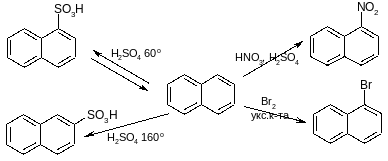
Гидрирование

Окисление

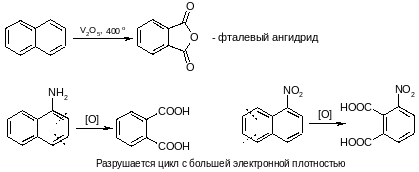 Бензол
широко используется в промышленной
органической химии в кач растворителя
и сырья для синтеза красителей, полимеров.
Толуол в производстве взрывчатых
веществ, красителей.
Бензол
широко используется в промышленной
органической химии в кач растворителя
и сырья для синтеза красителей, полимеров.
Толуол в производстве взрывчатых
веществ, красителей.
№36
1. Реакции электрофильного замещения (SE) на примере нитрования ароматических углеводородов.
2. Липиды фосфолипидов.
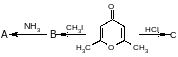
1. Реакции электрофильного замещения (SЕ)
Механизм реакций SR:
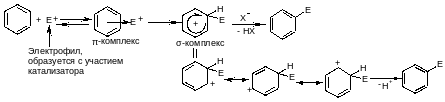
Влияние заместителей на скорость и направление реакций SЕ.
Различные заместители меняют электронную плотность в бензольном кольце: увеличивают или уменьшают, причем она становится не одинаковой на различных атомах углерода. Это изменяет скорость реакций SЕ и делает её неодинаковой для различных положений цикла.
Особое положение занимают галогены: за счет +М-эффекта они ориентируют реакцию в орто- и пара-положения (как заместители I рода), но их –I-эффект по величине превышает мезомерный, общая электронная плотность в кольца снижается и скорость реакции SE уменьшается.
Ориентация в дизамещенных бензола
1. Согласованная ориентация:

2. При несогласованной ориентации учитываются:
а) влияние более сильно активирующей группы

б) пространственные затруднения
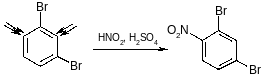
2. Нитрование
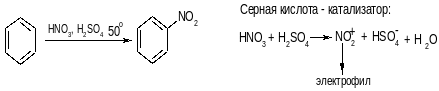
2)липиды– это большая группа природных веществ разнообразных по химическому строению и объединенных общим физико-химическим свойством: они нерастворимы в воде и хорошо растворимы в неполярных органических растворителях
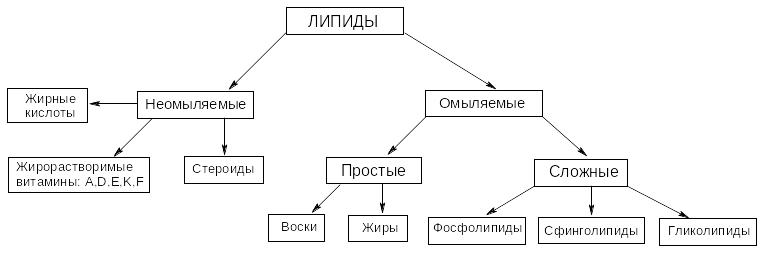
Жирными кислотами называются монокарбоновые кислоты с длинной углеродной цепью.
а) Насыщенные жирные кислоты б) Ненасыщенные жк
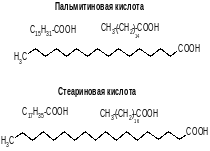

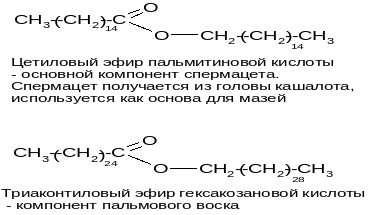
Воски – это сложные эфиры высших жирных кислот и
высших одноатомный спиртов.
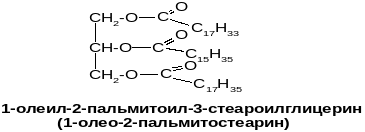
Жиры и масла
Триглицериды – это сложные эфиры глицерина и жирных кислот.
Структура и хим свойства фосфолипидов
Ф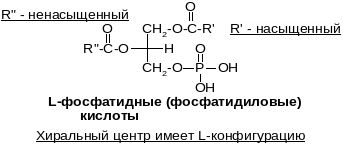 осфолипиды
– это производные фосфатидных
кислот
осфолипиды
– это производные фосфатидных
кислот
Молекулы фосфолипидов содержат 4 сложно-эфирные связи, которые разрываются при кислот-ном или щелочном гидролизе. При этом образуются глицерин, две жирных кислоты, аминоспирт и фосфорная кислота:

№37
1. Ре-ии элек замещения (SE) на примере алкилирования аром ув (реакция Фриделя-Крафтса)..
2. Терпены:
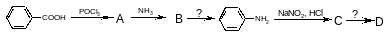
2) . Реакции электрофильного замещения (SЕ)
Механизм реакций SR:

Влияние заместителей на скорость и направление реакций SЕ.
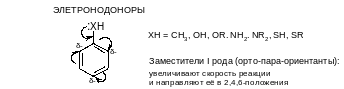
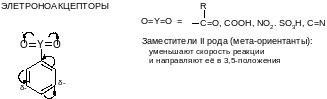
Особое положение занимают галогены: за счет +М-эффекта они ориентируют реакцию в орто- и пара-положения (как заместители I рода), но их –I-эффект по величине превышает мезомерный, общая электронная плотность в кольца снижается и скорость реакции SE уменьшается.
Реакции Фриделя-Крафтса
Алкилирование

