
- •Вопрос 1
- •Вопрос 2
- •Вопрос 3
- •Вопрос 4
- •Вопрос 5
- •Вопрос 6
- •Вопрос 7
- •Вопрос 8
- •Вопрос 9 Соотношение неопределённостей Гейзенберга
- •Вопрос 10 .Волновая функция и ее статистический смысл
- •Вопрос 11 Стационарное уравнение Шрёдингера
- •Вопрос 12
- •Вопрос 14 Прохождение частицы сквозь потенциальный барьер, туннельный эффект
- •Вопрос 15 Квантовый гармонический осциллятор
- •Вопрос 16 Решение уравнения Шрёдингера
- •Вопрос 17 Квантование энергии электрона в атоме
- •Линейчатый спектр атома водорода
- •1. Орбитальный механический момент импульса электрона
- •Вопрос 19
- •Вопрос 20
- •Структура периодической системы
- •Значение периодической системы
- •Вопрос 21 Поглощение, спонтанное и вынужденное излучения
- •Эйнштейна коэффициенты
- •Вопрос 22
- •Принцип действия лазера
- •Вопрос 23
- •1. Классическая теория теплоёмкости. Модель независимых осцилляторов
- •Вопрос 26
- •Вопрос 27
- •Вопрос 28
- •§ 77. Периодическая система элементов Менделеева
- •Вопрос 29
- •Вопрос 30
- •13.Температурная зависимость электропроводимости п/п-ов.
- •Вопрос 32
- •Масса и энергия связи ядра
- •Вопрос 33
- •Гамма-лучи
- •Бета-лучи
- •Альфа-частицы
- •Законы сохранения в ядерных реакциях
- •Закон сохранения энергии
- •Закон сохранения импульса
- •Закон сохранения момента импульса
- •Другие законы сохранения
- •Вопрос 35
- •Вопрос 36
Вопрос 28
Распределение электронов в атоме по энергетическим уровням
Каждый электрон в атоме движется в первом приближении в центрально-симметричном некулоновском поле. Состояние электрона в этом случае определяется тремя квантовыми числами: n и m, физический смысл которых был выяснен.
Таким образом, состояние каждого электрона в атоме характеризуется четырьмя квантовыми числами:
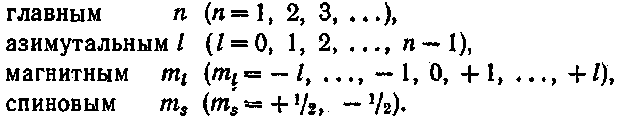
Энергия состояния зависит в основном от чисел п и д. Кроме того, имеется слабая зависимость энергии от чисел ml и тs поскольку их значения связаны с взаимной ориентацией моментов, от которой зависит величина взаимодействия между орбитальным и собственным магнитными моментами электрона. За некоторыми исключениями, энергия состояния сильнее возрастает с увеличением числа n, чем с увеличением l. Поэтому, как правило, состояние с большим «обладает, независимо от значения l, большей энергией,
В нормальном (невозбужденном) состоянии атома электроны должны располагаться на самых низких доступных для них энергетических уровнях. Поэтому,казалось бы, в любом атоме в нормальном состоянии все электроны должны находиться в состоянии Is (я — 1, / = 0), а основные термы всех атомов должны быть типа 5-термов (L — Q). Опыт, однако, показывает, что это не так.
Объяснение наблюдаемых типов термов заключается в следующем. Согласно одному из законов квантовой механики, называемому принципом Паули1), в одном и том же атоме (или в какой-либо квантовой системе) не может быть двух электронов, обладающих одинаковой совокупностью четырех квантовых чисел. Иными словами, в одном и том же состоянии не могут находиться одновременно два электрона.
Данному п соответствуют, как мы уже знаем, п2 состояний, отличающихся значениями / и т\ (см. § 69). Квантовое число ms может принимать два значения: ±7г. Поэтому в состояниях с данным значением п могут находиться в атоме не более 2/г2 электронов:
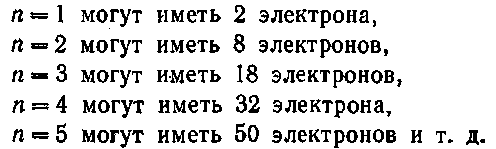
Совокупность электронов, имеющих одинаковые п и /, образует оболс-чку. Совокупность оболочек с одинаковым п образует группу или слой. В соответствии с значением п слоям дают обозначения, заимствованные из спектроскопии рентгеновских лучей:
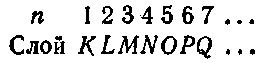
Подразделение возможных состояний электрона в атоме на оболочки и слои показано в табл. 5, в которой вместо обозначений та = ±7г применены символы: fj. Оболочки, как указано в таблице, могут обозначаться двумя способами (например, L\ либо 2s).
Для
полностью заполненной оболочки
характерно равенство нулю суммарного
орбитального и спинового моментов (L
=
0; S = 0). Следовательно, момент количества
движения такой оболочки равен нулю (У
= 0.) Убедимся в этом на примере З^-оболочки.
Спины всех десяти электронов, входящих
в эту оболочку, попарно компенсируют
друг друга, вследствие чего S = 0. Квантовое
число проекции результирующего
орбитального момента Ml
этой
оболочки на ось z
имеет
единственное значение
![]() .
Следовательно, L
также
равно нулю.
.
Следовательно, L
также
равно нулю.
Таким образом, при определении L и S атома заполненные оболочки можно не принимать во внимание.
