
- •1. Сформулировать представление о функциях крови, качественном и количественном составе плазмы в норме и при патологии
- •2. Дать представление о кислотно- щелочном равновесии, принципах его регуляции, механизмах компенсации и симптоматике нарушений кщс.
- •Т ранспортные белки
- •Бикарбонатная буферная система является открытой системой
- •Гемоглобин является самым важным небикарбонатным буфером.
- •Регуляция концентрации протонов
Бикарбонатная буферная система является открытой системой
Наиболее активной буферной системой внеклеточного пространства является бикарбонатная буферная система. Этот буфер представляет смесь недиссоциированной угольной кислоты и ее аниона.
![]()
Недиссоциированная угольная кислота находится в равновесии с количеством CO2, поэтому обычно понятие концентрация угольной кислоты и концентрация CO2 используется с одинаковым смыслом.
Уравнение Гендерсона- Гассельбальха для бикарбонатной системы
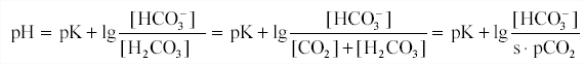
В норме рН =7,4; s*pCO2= 1,2 мМ; pCO2=40 мм рт. ст.; [HCO3-]= 24 мМ . Отсюда s= 0,03 K=7,95*10-7 и pK=6,1.
Взаимоотношения между соотношением [HCO3]/[H2CO3] и рН показаны в табл.3.По значению рK возможности такой буферной системы в регуляции рН очень невелики. Однако взаимодействие системы с газовой фазой легких делает бикарбонатную систему открытой системой, что придает ей почти неограниченные возможности по регуляции рН, а высокая концентрация компонентов в плазме делает эту буферную систему главной буферной системой внеклеточного пространства..
Табл 3.Соотношение НСО3 к СО2 и значение рН и концентрации протонов
Соотношение НСО3/СО2 |
8:1 |
10:1 |
12.5:1 |
16:1 |
20:1 |
25:1 |
32:1 |
40:1 |
50:1 |
Значение рН |
7.0 |
7.1 |
7.2 |
7.3 |
7.4 |
7.5 |
7.6 |
7.7 |
7.8 |
Концентрация протонов (нмоль/л) |
100 |
80 |
64 |
50 |
40 |
32 |
25 |
20 |
16 |
Гемоглобин является самым важным небикарбонатным буфером.
Среди небикарбонатных буферных систем, доля которых в общей концентрации составляет 50 % , гемоглобин занимает преимущественное положение благодаря высокой концентрации в крови (160 г/л крови) и функции имидазольных групп . Так как значение рК дезоксигенированного гемоглобина (8.25) выше, чем оксигенированного гемоглобина (6.95), дезоксигемоглобин представляет более слабую кислоту и лучший буфер. Наиболее благоприятным значением рК среди всех буферных систем (лучшая буферная область рН=рК±1) обладает фосфатная буферная система (6.80), однако в связи с небольшой концентрацией (1ммоль/л) она составляет лишь 1% общей буферной емкости. Внутри клеток фосфат находится в довольно высоких концентрациях ( 100-150 ммоль/л) однако он представлен органическими соединениями. Буферная емкость в значительной мере зависит от соответствия рК буферной системы внутриклеточному значению рН (6.8-6.9). Так как изоэлектрическая точка белков плазмы крови лежит в кислой среде (4.9-6.4 ) они переходят в анионное состояние при рН 7.4, и их буферная емкость составляет около 5 ммоль/л, хотя они присутствуют в довольно высокой концентрации.
Еще одна возможная буферная система – аммиак / ион аммония в связи с очень низкой концентрацией (40мкмоль/л) и неблагоприятным значением рК (9.4) имеет небольшое значение для буферных систем внеклеточного пространства.
Из данных таблиц видно, что внеклеточное пространство как закрытая система имело бы буферную емкость около 24 ммоль/л /рH, однако как открытая система она обладает в три раза более высокой емкостью причем на долю бикарбонатной системы приходится 3/4 емкости всех буферных систем. Если учитывать компенсаторные возможности регуляции дыханием парциального давления диоксида углерода, хотя строго говоря и не подпадающую под понятие буфер, общая емкость и процентная доля CO2-бикарбонатной системы будет еще более значимой.
Все упомянутые буферные системы, как составные части общего буферного раствора, находятся в равновесии друг с другом: слабая углекислота реагирует с основаниями небикарбонатной системы:
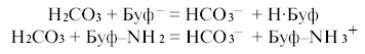
и наоборот, бикарбонат реагирует с недиссоциированной формой небикарбонатной буферной системы
![]()
