
- •Институт металлургии и химии
- •Кафедра химии лабораторный практикум
- •Часть 3
- •Физико-химические методы анализа
- •Фотоколориметрия Краткие теоретические сведения
- •Определение массовой доли р2о5 в фосфорной кислоте
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Построение калибровочного графика
- •Построение калибровочного графика
- •4.2. Анализ фосфорной кислоты
- •5. Обработка экспериментальных данных
- •Экспериментальные и расчетные данные
- •Фотоколориметрическое определение водорастворимого р2о5 в диаммофоске (дафк)
- •2. Сущность метода
- •4. Алгоритм определения
- •4.2. Анализ дафк
- •5. Обработка результатов
- •Экспериментальные и расчетные данные
- •Определение азота аммонийных солей в водных растворах
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Построение калибровочного графика
- •Построение калибровочного графика
- •4.2. Проведение анализа
- •5. Обработка результатов
- •Экспериментальные и расчетные данные
- •Определение железа (III) в водных растворах
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Построение калибровочного графика
- •Построение калибровочного графика
- •4.2. Проведение анализа
- •5. Обработка результатов
- •Экспериментальные и расчетные данные
- •Контрольные вопросы к разделу «фотоколориметрия»
- •1. В чем сущность фотометрического метода анализа?
- •2. Сформулируйте основной закон светопоглощения.
- •3. Что такое абсорбционность (оптическая плотность)? От чего она зависит?
- •Хроматографический анализ Краткие теоретические сведения
- •Ионообменная хроматография Краткие теоретические сведения
- •Определение содержания меди (II) в растворе методом ионообменной хроматографии
- •Сущность метода
- •Приборы и реактивы
- •Алгоритм определения
- •Экспериментальные данные
- •Обработка результатов
- •Экспериментальные и расчетные данные
- •Разделение цинка (II) и никеля (II) с помощью анионита
- •2. Сущность метода
- •Приборы и реактивы
- •Алгоритм определения
- •5.1. Методика разделения
- •5.2. Определение никеля
- •5.3. Определение цинка
- •Обработка результатов
- •Определение никеля
- •Определение цинка
- •Контрольные вопросы к разделу «хроматография»
- •Высокочастотное титрование Краткие теоретические сведения
- •Определение содержания железа (III) в растворе методом высокочастотного титрования
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм определения
- •Зависимость силы тока от объема титранта
- •5. Обработка результатов
- •Экспериментальные и расчетные данные
- •Контрольные вопросы к разделу «высокочастотное титрование»
- •Литература
- •Содержание
- •1 62600, Череповец, пр. Луначарского, 5
Ионообменная хроматография Краткие теоретические сведения
Ионообменная хроматография основана на обратимом стехиометрическом обмене ионов, находящихся в растворе, на ионы, входящие в состав ионообменника. Ионообменниками или ионитами называют твердые, малорастворимые, органические или неорганические высокомолекулярные кислоты, основания и их соли.
В зависимости от знака заряда функциональных групп ионообменные смолы являются катионитами или анионитами. Катиониты содержат кислотные функциональные группы [– SO3‾, – CO2‾, – PO32‾, – N(CH2CO2‾)2], поэтому каркас катионита, несущий фиксированные отрицательные заряды, заряжен отрицательно. Отрицательные заряды каркаса, компенсируются положительными зарядами противоионов, так что в целом катионит остается электронейтральным. Противоионы, в данном случае катионы, в отличие от функциональных групп каркаса, обладают подвижностью и могут переходить в раствор в обмен на эквивалентное количество ионов из раствора. Этот обмен приводит к установлению подвижного равновесия между ионами, находящимися в фазе смолы, и ионами в растворе. Химические формулы катионообменников схематически можно изобразить следующим образом: RSO3H; RSO3Na или R–H, R–Na. В первом случае катионообменник находится в Н+–форме, во втором – в Na+-форме; R – полимерная матрица. Тогда процесс ионного обмена записывают как обычную химическую гетерогенную реакцию:
R – H + Na+ ↔ R – Na + Н+
То есть в растворе появятся ионы водорода, а эквивалентное количество ионов Na+ будет поглощено катионитом. Функциональными группами каркаса анионитов являются четвертичные –NR3‾, третичные –NR2H+, первичные –NH2+, аммониевые, пиридиновые и другие основания, а в качестве подвижных противоионов выступают анионы. Амфотерные иониты или амфолиты, способны осуществлять одновременный обмен катионов и анионов. Анионообменники схематично можно изобразить так: RNH3OH или RNH3Cl (или R–ОН, R–Cl). В первом случае анионообменник находится в ОН‾-форме, во втором – в Cl–-форме.
Анионообменную реакцию можно записать следующим образом:
R-ОН + Cl– ↔ RCl+ОН–
Важной характеристикой ионообменника является его обменная емкость – свойство ионообменника поглощать определенное количество ионов из раствора. Обменную емкость выражают количеством моль-эквивалентов обменивающегося иона на единицу массы или объема смолы (моль экв/г или моль экв/мл).
На процесс ионного обмена оказывают влияние природа ионообменника и ионов раствора, а также ряд экспериментальных факторов: параметры колонн, размер зерен ионообменника, скорость пропускания раствора, состав подвижной фазы, температура и др.
В зависимости от цели эксперимента применяемый теплообменник обрабатывают растворами кислот, щелочей, солей для превращения в определенную форму (например, RН, RОН или их солевые формы RNа, RCl, RNH4). Обработанный ионообменник регенерирует, возвращая его в исходное состояние. Так, при десорбции катионов растворами кислот происходит регенерация обменника:
(RSO3)nН + nН+ ↔ nRSO3Н + Мn+
Синтетические высокополимерные ионообменные смолы делятся на четыре группы ионитов:
1) сильнокислотные катиониты: КУ-1, КУ-2, КУ-23, СДВ-3. Способны к обмену в кислой, нейтральной и щелочной среде;
2) слабокислотные катиониты, содержащие карбоксильные группы: КБ-2, КБ-4, КФУ, СГ-1. Способны к обмену ионов при рН > 7;
3) сильноосновные
аниониты, содержащие четвертичные
аммониевые или пиридиновые группы:
АВ-17, АВ-18, АВ-19, АВ-31
7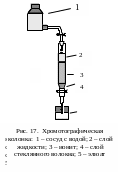 ДЭ-10П.
Способны к обмену ионов в кислой,
нейтральной и щелочной среде;
ДЭ-10П.
Способны к обмену ионов в кислой,
нейтральной и щелочной среде;
4
5
а
Для ионообменной хроматографии в количественном анализе применяют стеклянные колонки (рис. 17).
Р а б о т а 17
