
- •Бийский технологический институт (филиал) г.В. Багров, г.И. Севодина, о.Ю. Кравцова общая химическая технология
- •Содержание
- •Введение
- •Цель работы
- •Краткие теоретические сведения
- •Математическое описание процесса
- •Алгоритм решения
- •Задание
- •Контрольные вопросы
- •Лабораторная работа № 2. Исследование процесса восстановления двуокиси углерода углем
- •2.1 Цель работы
- •2.2 Краткие теоретические сведения
- •2.3 Описание кинетики процесса
- •2.4 Задание
- •2.5 Контрольные вопросы
- •Лабораторная работа № 3. Сравнение эффективности работы изотермических реакторов
- •3.1 Цель работы
- •3.2 Краткие теоретические сведения
- •3.3 Математическое описание изотермических реакторов
- •3.4 Задание
- •3.5 Контрольные вопросы
- •Лабораторная работа № 4. Исследование влияния условий проведения газофазной реакции на объем реактора
- •4.1 Цель работы
- •4.2 Краткие теоретические сведения
- •4.3 Математическое описание кинетики процесса
- •4.4 Задание
- •4.5 Контрольные вопросы
- •Лабораторная работа № 5. Расчет неизотермических реакторов
- •5.1 Цель работы
- •5.2 Краткие теоретические сведения
- •5.3 Задание
- •5.4 Контрольные вопросы
- •Лабораторная работа № 6. Реакторы с неидеальной структурой потока
- •6.1 Цель работы
- •6.2 Краткие теоретические сведения
- •6.3 Задание
- •6.4 Контрольные вопросы
- •Лабораторная работа № 7. Обогащение минерального сырья. Флотация
- •7.1 Цель работы
- •7.2 Краткие теоретические сведения
- •7.3 Описание лабораторной установки
- •7.4 Методика проведения работы
- •7.5 Обработка данных
- •7.6 Контрольные вопросы
- •Лабораторная работа № 8. Жесткость воды и еЕ определение. Методы снижения жесткости воды
- •8.1 Цель работы
- •8.2 Краткие теоретические сведения
- •8.3 Описание лабораторной установки
- •8.4 Определение жесткости воды
- •8.5 Обработка данных
- •8.6 Контрольные вопросы
- •Литература
- •А2 Программа № 2
- •А3 Программа № 3
- •А4 Программа № 4
- •А5 Программа № 5
- •А6 Программа № 6
- •А7 Программа № 7
- •А8 Программа № 8
- •А9 Программа № 9
2.5 Контрольные вопросы
1. Зачем проводится газификация топлива?
2. Какие реакции называются гетерогенными?
3. Какие области протекания гетерогенного процесса вы знаете?
4. Что такое лимитирующая стадия?
5. Как определяется лимитирующая стадия гетерогенного процесса?
6. Роль температуры и давления в проведении процесса восстановления двуокиси углерода.
7. Какие способы повышения степени превращения реагента применяются в промышленных условиях?
Лабораторная работа № 3. Сравнение эффективности работы изотермических реакторов
3.1 Цель работы
3.1.1 Использование кинетических закономерностей химической реакции для сравнения эффективности работы реакторов.
3.1.2 Изучение влияния гидродинамического режима в реакторе на показатели процесса.
3.2 Краткие теоретические сведения
Основными факторами сравнения химических реакторов, определяющими выбор типа аппарата, является кинетика химической реакции, отношение порядков основной и побочных реакций, а также распределение времени пребывания реагентов, концентраций и температур в реакционном объеме. Эти факторы в различных типах реакторов могут по-разному влиять на степень превращения реагентов, выход, селективность и, следовательно, на себестоимость получаемого продукта. Величина удельной производительности реактора, являющаяся одной из важнейших его характеристик, непосредственно связана также с кинетикой химического процесса и типом аппарата. Общее правило, устанавливающее связь между селективностью процесса и его аппаратурным оформлением: если зависимость между степенью превращения и селективностью падает, то следует выбирать реактор смешения периодического действия или реактор вытеснения, а для реакций с возрастающей зависимостью – реактор смешения непрерывного действия [3].
Оценку эффективности реактора по тому или иному технологическому критерию обычно проводят по двум крайним моделям: идеального смешения (РИС) и идеального вытеснения (РИВ), отражающим гидродинамические характеристики потоков [7]. В реальных аппаратах структура потока отвечает промежуточному варианту модели. Предпочтение отдается такой конструкции аппарата, которая приближена к идеальному аппарату с наилучшими показателями технологических критериев.
3.3 Математическое описание изотермических реакторов
В данной работе рассмотрены три варианта конструктивного оформления процесса химического превращения: РИС, РИВ и каскад РИС на примере двух химических реакций:
![]() (3.1)
(3.1)
![]()
(3.2)
Реакция (3.1) является простой необратимой, реакция (3.2) – параллельной. В обоих случаях целевым продуктом является компонент R. Для определения технологических критериев необходимо составить уравнения математического описания всех указанных типов реакторов с учетом кинетики реакции. Рассмотрим модели непрерывных реакторов для проведения реакции (3.1).
3.3.1 Реактор идеального вытеснения (РИВ)
Для изотермического реактора математическое описание представляет собой систему уравнений материального баланса по компонентам:

(3.3)
3.3.2 Реактор идеального смешения (РИС)
Уравнения материального баланса в стационарных условиях представляют собой систему вида:
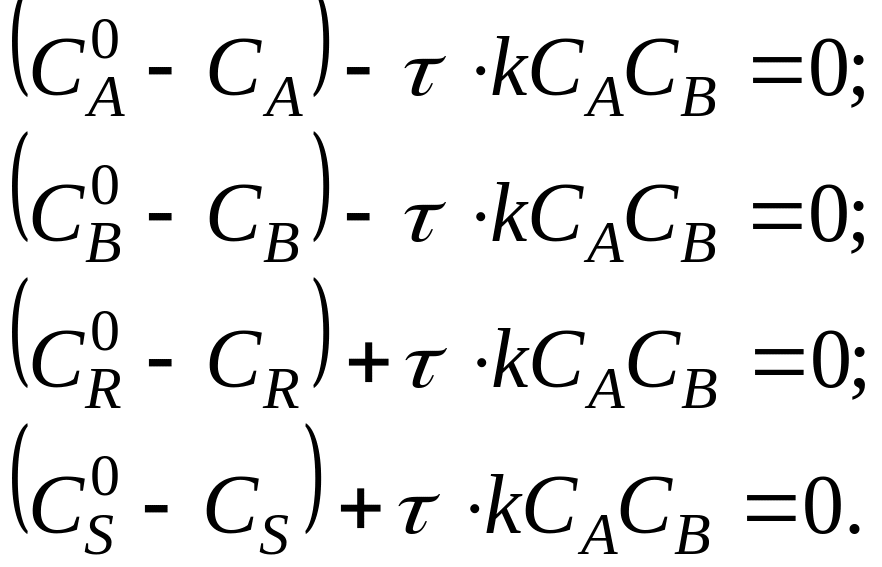
(3.4)
3.3.3 Каскад реакторов идеального смешения (РИС- m)
Параметром этой модели является число ячеек m. Система уравнений материального баланса по компонентам для j-ячейки имеет вид:
 (3.5)
(3.5)
В системы уравнений (3.3),
(3.4), (3.5) входят:
– время пребывания в реакторе, c;![]() – время пребывания в j-й
ячейке, с;
– время пребывания в j-й
ячейке, с;
![]() начальные концентрации
компонентов, моль/м3;
Са,
Св,
CR,
CS
– текущие значения
концентраций, моль/м3;
k
– константа скорости реакции, м3
/(моль с).
начальные концентрации
компонентов, моль/м3;
Са,
Св,
CR,
CS
– текущие значения
концентраций, моль/м3;
k
– константа скорости реакции, м3
/(моль с).
В результате решения систем уравнений (3.3)-(3.5) можно рассчитать концентрации всех компонентов, а затем и технологические критерии (программа № 4, Приложение А).
Ниже приведены системы уравнений материального баланса по компонентам для РИВ и РИС соответственно применительно для реакции (3.2).
 (3.6)
(3.6)
 (3.7)
(3.7)
В результате численного решения систем уравнений (3.6), (3.7) (программа № 5, Приложение А) получают значения концентраций компонентов на выходе из реактора и значения технологических критериев.
