
- •Бийский технологический институт (филиал) г.В. Багров, г.И. Севодина, о.Ю. Кравцова общая химическая технология
- •Содержание
- •Введение
- •Цель работы
- •Краткие теоретические сведения
- •Математическое описание процесса
- •Алгоритм решения
- •Задание
- •Контрольные вопросы
- •Лабораторная работа № 2. Исследование процесса восстановления двуокиси углерода углем
- •2.1 Цель работы
- •2.2 Краткие теоретические сведения
- •2.3 Описание кинетики процесса
- •2.4 Задание
- •2.5 Контрольные вопросы
- •Лабораторная работа № 3. Сравнение эффективности работы изотермических реакторов
- •3.1 Цель работы
- •3.2 Краткие теоретические сведения
- •3.3 Математическое описание изотермических реакторов
- •3.4 Задание
- •3.5 Контрольные вопросы
- •Лабораторная работа № 4. Исследование влияния условий проведения газофазной реакции на объем реактора
- •4.1 Цель работы
- •4.2 Краткие теоретические сведения
- •4.3 Математическое описание кинетики процесса
- •4.4 Задание
- •4.5 Контрольные вопросы
- •Лабораторная работа № 5. Расчет неизотермических реакторов
- •5.1 Цель работы
- •5.2 Краткие теоретические сведения
- •5.3 Задание
- •5.4 Контрольные вопросы
- •Лабораторная работа № 6. Реакторы с неидеальной структурой потока
- •6.1 Цель работы
- •6.2 Краткие теоретические сведения
- •6.3 Задание
- •6.4 Контрольные вопросы
- •Лабораторная работа № 7. Обогащение минерального сырья. Флотация
- •7.1 Цель работы
- •7.2 Краткие теоретические сведения
- •7.3 Описание лабораторной установки
- •7.4 Методика проведения работы
- •7.5 Обработка данных
- •7.6 Контрольные вопросы
- •Лабораторная работа № 8. Жесткость воды и еЕ определение. Методы снижения жесткости воды
- •8.1 Цель работы
- •8.2 Краткие теоретические сведения
- •8.3 Описание лабораторной установки
- •8.4 Определение жесткости воды
- •8.5 Обработка данных
- •8.6 Контрольные вопросы
- •Литература
- •А2 Программа № 2
- •А3 Программа № 3
- •А4 Программа № 4
- •А5 Программа № 5
- •А6 Программа № 6
- •А7 Программа № 7
- •А8 Программа № 8
- •А9 Программа № 9
8.2 Краткие теоретические сведения
Среди основных факторов, определяющих качество воды, выделяют ее жесткость и кислотность.
Жесткость воды обусловлена наличием в ней преимущественно катионов Са2+ (кальциевая жесткость воды) и Мg2+ (магниевая жесткость воды). Сумма концентраций Са2+ и Мg2+ называется общей жесткостью воды. Она складывается из карбонатной (временной, устранимой кипячением) и некарбонатной (постоянной) жесткости воды. Карбонатная вызвана присутствием в воде гидрокарбонатов Са и Mg. Некарбонатная – наличием сульфатов, хлоридов, силикатов, нитратов и фосфатов этих металлов.
В России жесткость воды определяют в [моль·экв/л]: карбонатная жесткость отвечает той части катионов Са2+ и Мg2+, которая эквивалентна содержащимся в воде анионам HCO3-, некарбонатная – анионам SO42-, NO3- и др. (1 моль·экв/л соответствует 20,04 мг/л катионов Са2+ или 12,16 мг/л катионов Мg2+). В других странах для выражения жесткости воды часто используют так называемые градусы жесткости. Например, 1 градус жесткости (немецкий), соответствующий содержанию 0,001 г СаО в 1 литре воды, равен 0,357 моль· экв/л.
Общую жесткость воды можно вычислить по формуле:
![]() .
.
Различают воду мягкую (общая жесткость до 2 моль·экв/литр), средней жесткости (от 2 до 10 моль·экв/л) и жесткую (более
10 моль·экв/литр).
Повышенная жесткость воды способствует усилению образования накипи в паровых котлах, отопительных приборах и бытовой металлической посуде, что значительно снижает интенсивность теплообмена, приводит к большому перерасходу топлива и перегреву металлических поверхностей.
Для устранения или уменьшения жесткости воды применяют специальные методы.
а) Термический метод (нагревание) умягчения воды основан на смещении равновесия в сторону образования карбонатов:
![]() .
.
Однако полностью карбонатную кальциевую жесткость устранить не удается, так как карбонаты кальция, хотя и незначительно (13 мг/л при 18 оС), но все же растворимы в воде.
![]()
Вначале образуется сравнительно хорошо растворимый (110 мг/л при температуре 18 оС) карбонат магния, который при продолжительном кипячении гидролизируется с образованием осадка малорастворимого (8,4 мг/л) гидроксида Mg:
![]() .
.
б) Реагентные методы умягчения воды основаны на обработке ее реагентами, анионы которых образуют с катионами Са2+ и Mg2+ малорастворимые соединения. Сущность известково-содового метода умягчения воды сводится к следующим основным процессам:
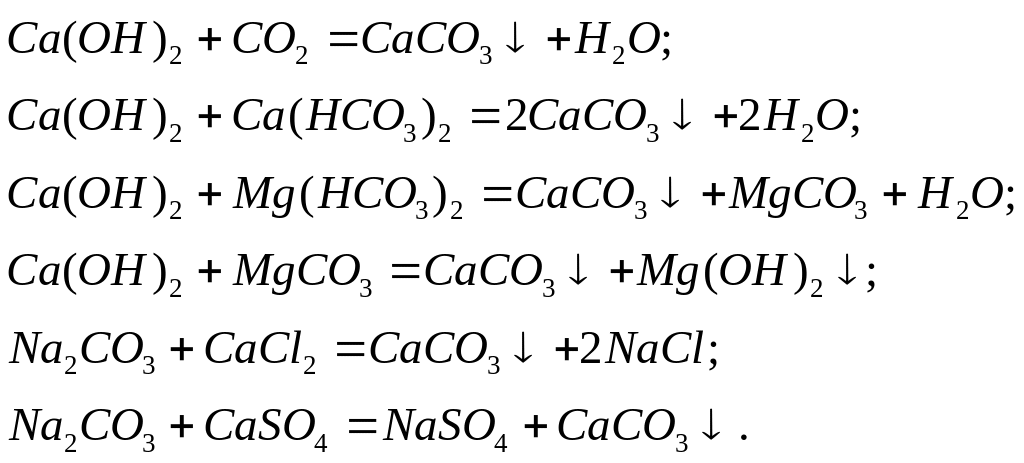
Умягчение воды известково-содовым методом применяют при высокой карбонатной и низкой некарбонатной жесткости воды.
Этим методом остаточная жесткость может быть доведена до 0,5–1,0 моль.экв/л.
При умягчении воды содо-натриевым методом ее обрабатывают содой и гидроксидом натрия:
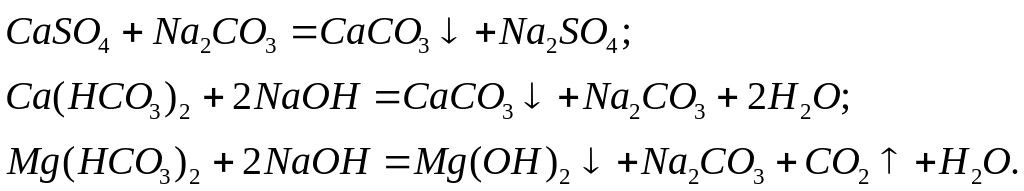
Поскольку сода образуется при взаимодействии NaOH c Ca(HCO3)2, требуемая доза ее значительно уменьшается. Содо-натриевый метод обычно применяется для умягчения воды, карбонатная жесткость которой немного дольше некарбонатной.
в) Фосфатный метод умягчения воды как самостоятельный не применяют в связи с высокой стоимостью реагентов. Фосфаты используют для доумягчения воды после ее обработки другими реагентами, например, известью и содой.
![]()
Процесс фосфатного доумягчения воды проводят обычно при температуре свыше 100 оС (термохимический метод). Остаточная жесткость при этом составляет 0,04–0,05 моль·экв/л.
г) Ионообменные методы используют для умягчения воды с преобладанием некарбонатной жесткости воды (Na+-катионирование) или карбонатной (Н+-катионирование).
