
- •Бийский технологический институт (филиал) г.В. Багров, г.И. Севодина, о.Ю. Кравцова общая химическая технология
- •Содержание
- •Введение
- •Цель работы
- •Краткие теоретические сведения
- •Математическое описание процесса
- •Алгоритм решения
- •Задание
- •Контрольные вопросы
- •Лабораторная работа № 2. Исследование процесса восстановления двуокиси углерода углем
- •2.1 Цель работы
- •2.2 Краткие теоретические сведения
- •2.3 Описание кинетики процесса
- •2.4 Задание
- •2.5 Контрольные вопросы
- •Лабораторная работа № 3. Сравнение эффективности работы изотермических реакторов
- •3.1 Цель работы
- •3.2 Краткие теоретические сведения
- •3.3 Математическое описание изотермических реакторов
- •3.4 Задание
- •3.5 Контрольные вопросы
- •Лабораторная работа № 4. Исследование влияния условий проведения газофазной реакции на объем реактора
- •4.1 Цель работы
- •4.2 Краткие теоретические сведения
- •4.3 Математическое описание кинетики процесса
- •4.4 Задание
- •4.5 Контрольные вопросы
- •Лабораторная работа № 5. Расчет неизотермических реакторов
- •5.1 Цель работы
- •5.2 Краткие теоретические сведения
- •5.3 Задание
- •5.4 Контрольные вопросы
- •Лабораторная работа № 6. Реакторы с неидеальной структурой потока
- •6.1 Цель работы
- •6.2 Краткие теоретические сведения
- •6.3 Задание
- •6.4 Контрольные вопросы
- •Лабораторная работа № 7. Обогащение минерального сырья. Флотация
- •7.1 Цель работы
- •7.2 Краткие теоретические сведения
- •7.3 Описание лабораторной установки
- •7.4 Методика проведения работы
- •7.5 Обработка данных
- •7.6 Контрольные вопросы
- •Лабораторная работа № 8. Жесткость воды и еЕ определение. Методы снижения жесткости воды
- •8.1 Цель работы
- •8.2 Краткие теоретические сведения
- •8.3 Описание лабораторной установки
- •8.4 Определение жесткости воды
- •8.5 Обработка данных
- •8.6 Контрольные вопросы
- •Литература
- •А2 Программа № 2
- •А3 Программа № 3
- •А4 Программа № 4
- •А5 Программа № 5
- •А6 Программа № 6
- •А7 Программа № 7
- •А8 Программа № 8
- •А9 Программа № 9
Введение
Одной из основных задач инженерного исследования химических процессов является установление закономерностей их протекания, необходимых для разработки и проектирования новых и анализа работы существующих технологий с целью их совершенствования.
Закономерности химических процессов могут быть установлены экспериментально либо расчетным путем. И в том, и в другом случае определяется влияние параметров процесса на его эффективность.
При обработке экспериментальных данных чрезвычайно важно получение количественных соотношений между параметрами процесса, т.е. математической модели процесса, включающей в себя уравнения кинетики, гидродинамики, распределение концентраций, температурных полей и т.д.
Подобная модель может быть использована для практических целей. Однако применение математических моделей химико-технологических процессов в большинстве случаев связано с использованием вычислительных машин.
В данном лабораторном практикуме по курсу общей химической технологии используются персональные компьютеры (ПК). В каждой лабораторной работе формулируется ее цель, приводится математическое описание процесса, метод решения и задания, предлагаемые студентам для выполнения.
Использование ПК в расчетных занятиях по курсу ОХТ расширяет класс решаемых задач, позволяя дать оперативный ответ на вопрос о том, что произойдет с реактором или процессом в целом при тех или других изменениях параметров.
ЛАБОРАТОРНАЯ РАБОТА №1.
ИССЛЕДОВАНИЕ ПРОЦЕССА ОКИСЛЕНИЯ
СЕРНИСТОГО АНГИДРИДА НА ВАНАДИЕВОМ
КАТАЛИЗАТОРЕ В ПРОТОЧНОМ ТРУБЧАТОМ
РЕАКТОРЕ (4 часа)
Цель работы
Целью настоящей работы является анализ кинетических закономерностей процесса окисления сернистого ангидрида для установления технологических параметров его осуществления в промышленных реакторах.
Краткие теоретические сведения
Получение серной кислоты из колчедана и серы контактным способом по открытой (нециклической) схеме можно разделить на четыре крупные стадии (рисунки 1.1, 1.2):
- получение обжигового газа, содержащего диоксид серы;
- подготовку обжигового газа к контактному окислению;
- каталитическое окисление диоксида серы;
- абсорбцию триоксида серы.
При различном технологическом оформлении некоторые детали этих стадий, особенно второй, будут отличаться, однако принципиальный подход к их осуществлению и выбору технологического решения зависит от тех задач, которые решаются на рассматриваемом этапе, и в разных конкретных процессах получения серной кислоты будет одинаковым.

Рисунок 1.1 – Функциональная схема производства серной
кислоты методом одинарного контактирования
Воздух
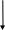
Рисунок 1.2 – Функциональная схема производства серной
кислоты из серы методом двойного контактирования
Процесс окисления сернистого
ангидрида на ванадиевой контактной
массе – важнейшая составная часть
промышленного способа получения
серной кислоты. Суть его состоит в
осуществлении реакции SO2
+ 1/2 О2
![]() SO3.
SO3.
Это гетерогенно-каталитический, экзотермический, обратимый процесс, протекающий с уменьшением объема, без побочных реакций. Скорость реакции зависит от степени приближения к равновесию и, как функция температуры, проходит через максимум (с ростом температуры растет константа скорости прямой реакции и уменьшаются константа равновесия и равновесная степень превращения). Скорость реакции повышается с ростом концентрации кислорода, поэтому процесс в промышленности проводят при избытке кислорода.
Обратимые экзотермические реакции необходимо проводить в соответствии с линией оптимальных температур (ЛОТ), т.е. понижая температуру в контактном аппарате по мере роста степени превращения реагентов.
Чаще всего в промышленности используют полочные контактные аппараты с наружным теплообменом. Схема теплообмена предполагает максимальное использование тепла реакции для подогрева исходного газа и одновременное охлаждение газа между полками.
