
Лекция 5. Растворы электролитов и не электролитов. Химия воды.
5.1 Общие понятия о дисперсных системах.
Дисперсной называют систему, состоящую из двух или более фаз, в которой одна фаза в виде отдельных частичек распределена в другой. В таких системах различают дисперсионную среду (распределяющую среду) и дисперсную фазу (раздробленное вещество).
В зависимости от размеров частиц дисперсной фазы различают: а) истинные растворы, б) коллоидные растворы, в) грубодисперсные системы. Истинные растворы - это гомогенные системы переменного состава, содержащие два или более вещества. Они являются молекулярно-дисперсными системами, так как степень измельчения дисперсной фазы молекулярная или ионная. Размеры частиц меньше 10-9 м, поэтому они не могут быть обнаружены оптическими методами.
Гетерогенные
дисперсные системы подразделяются на
коллоидные (размер частиц от 10-9
до 5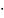 10-7
м ) и грубодисперсные (размер частиц
более 10-6
м). Частицы могут быть обнаружены
оптическими методами.
10-7
м ) и грубодисперсные (размер частиц
более 10-6
м). Частицы могут быть обнаружены
оптическими методами.
Дисперсные системы также классифицируются по агрегатным состояниям дисперсной фазы и дисперсионной среды. Системы с газовой дисперсионной средой - аэрозоли (туман, пыль, дым); с жидкой - золи, эмульсии, суспензии, пены (краски, молоко, глина в воде, мыльная пена); с твердой - твердая эмульсия, гели (масло, пеноматериалы).
В истинных растворах растворенное вещество и растворитель образуют одну фазу.
Коллоидные системы. Коллоидные системы - это дисперсные системы, в которых дисперсная фаза (коллоидные частицы) состоят из сотен, иногда тысяч элементарных частиц (молекул, ионов), вследствие чего возникает поверхность раздела между коллоидной частицей и растворителем (дисперсионной средой).
Коллоидные растворы могут быть получены агрегацией молекул или ионов в более крупные частицы либо диспергированием (измельчением) крупных частиц на мелкие до коллоидных размеров. Для достижения коллоидного состояния системы необходимо не только достигнуть нужной степени дисперсности вещества, но и создать условия для ее стабилизации, для чего добавляют стабилизаторы: ПАВ, ионы, из которых состоит частица. Коллоидные частицы обладают высокой поверхностной энергией, адсорбируют те или иные частицы из раствора, поэтому их поверхность имеет определенный заряд.
Коллоидная частица имеет сложное строение. Она состоит из ядра, адсорбированных ионов, гидратированных противоионов адсорбционного и диффузного слоев.

Ядро аодсорбационный слой диффузный слой
[Коллоидная частица (гранула)]
[мицелла ]
Из схемы видно, что мицелла нейтральна, а гранула несет электрический заряд, знак которого зависит от условий получения раствора.
Существуют лиофильные (гидрофильные) коллоиды, в которых растворитель взаимодействует с ядрами частиц, и лиофобные (гидрофобные) коллоиды, где нет такого взаимодействия. Золи - это коллоидные системы, имеющие жидкую дисперсионную среду. При длительном хранении мицеллы гидрофильных золей связываются между собой, образуя гели.
Основной особенностью коллоидных растворов является их стойкость, которая обусловлена двумя причинами: существованием одноименного электрического заряда у коллоидных частиц и наличием сольватной оболочки из молекул растворителя. Гидратная оболочка, снижая поверхностную энергию дисперсной фазы, уменьшает стремление частиц к укрупнению.
Дисперсная
фаза имеет заряд, противоположный по
знаку заряду дисперсионной среды. При
пропускании через золь постоянного
электрического тока происходит
направленное движение частиц к
электродам. При этом движение частиц
дисперсной фазы называется электрофорезом,
а движение частиц дисперсионной среды
- электроосмосом. Плотность зарядов на
поверхности гранулы выше, чем плотность
зарядов-ионов в диффузном слое,
поэтому между фазами возникает
электрокинетический, или
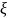 дзета-потенциал. С увеличением этого
потенциала растет устойчивость коллоидных
систем.
дзета-потенциал. С увеличением этого
потенциала растет устойчивость коллоидных
систем.
Устойчивость коллоидного раствора можно нарушить, если устранить одноименный заряд коллоидных частиц или разрушить защитную гидратную оболочку. При этом произойдет слипание и соединение частиц в более крупные агрегаты (коагуляция) и их последующее осаждение (седиментация). Процесс увеличения размеров частиц дисперсной фазы золя называется коагуляцией. Коагуляцию коллоидных растворов можно вызвать введением в коллоидную систему электролита, имеющего противоионы по отношению к коллоидным частицам, нагреванием. Например, при отрицательном заряде коллоидных частиц в раствор можно ввести сульфаты алюминия или железа. Нагревание уменьшает адсорбцию ионов коллоидными частицами, что также приводит к коагуляции. В природной воде содержатся вещества в коллоидном состоянии, поэтому ее подвергают обработке, вызывающей коагуляцию коллоидных частиц.
Очистка коллоидных растворов от присутствующих в них молекулярных и ионных примесей растворенных веществ называется диализом. При этом используются специальные мембраны, непроницаемые для коллоидных частиц.
Очистка коллоидных растворов от присутствующих в них молекулярных и ионных примесей растворенных веществ называется диализом. При этом используются специальные мембраны, непроницаемые для коллоидных частиц.
При разрушении коллоидной системы образуется грубодисперсная система.
Грубодисперсные системы. К грубодисперсным системам относятся суспензии и эмульсии. Суспензиями называются системы, в которых дисперсная фаза твердая, а дисперсионная среда жидкая. В эмульсиях дисперсная фаза и дисперсионная среда жидкие. Эмульсии должны содержать эмульгаторы - вещества, облегчающие диспергирование эмульсий и препятствующие коалесценции (слиянию капель раздробленной жидкости). Эффективными эмульгаторами являются мицеллообразующие ПАВ, растворимые высокомолекулярные вещества. Коалесценцию стабилизированной эмульсии можно вызвать центрифугированием, нагреванием, воздействием электрического поля высокого напряжения, а также с помощью деэмульгаторов, кислот, солей и других веществ, разрушающих эмульгатор.
