
- •Термодинамика и теплопередача. Учебное пособие
- •Раздел I. Техническая термодинамика
- •Содержание
- •Раздел I
- •Тема 1. Газ, как рабочее тело термодинамических систем
- •Тема 2. Первый закон термодинамики
- •Тема 3. Термодинамические процессы
- •Тема 4. Второй закон термодинамики
- •Тема 5. Идеальные циклы тепловых двигателей
- •Основные условные обозначения
- •Основные сечения потока
- •Сокращения
- •Используемые индексы
- •Предисловие
- •Введение
- •Раздел I техническая термодинамика
- •Тема 1. Газ, как рабочее тело термодинамических систем
- •1.1. Структура основных понятий термодинамики авиационных гтд
- •1.2. Основные понятия и определения термодинамики
- •1.3. Реальный и идеальный газы. Параметры состояния рабочего тела
- •1.3.1. Давление
- •1.3.2. Температура
- •1.3.3. Удельный объём, плотность
- •1.4. Уравнение состояния идеального и реального газов
- •1.4.1. Уравнение состояния идеального газа
- •1.4.2. Уравнение состояния реального газа
- •1.5. Понятие о термодинамическом процессе. Равновесные (обратимые) и неравновесные (необратимые) процессы
- •1.5.1. Равновесные (обратимые) процессы
- •1.5.2. Графическое изображение термодинамического процесса
- •1.5.3. Неравновесные (необратимые) процессы
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Проверьте, как Вы усвоили материал
- •Тема 2. Первый закон термодинамики
- •2.1. Внутренняя энергия рабочего тела. Изменение внутренней энергии
- •2.2. Работа газа, как форма передачи энергии в термодинамическом процессе
- •2.3. Теплота, как форма передачи энергии в термодинамическом процессе
- •2.4. Энтропия. Энтропийная “t-s” диаграмма
- •2.5. Зависимость количества работы и теплоты от характера термодинамического процесса
- •2.6. Теплоёмкость газа. Уравнение Майера. Показатель адиабаты
- •2.7. Энтальпия
- •2.8. Техническая работа (работа движущегося газа)
- •2.9. Содержание и уравнение первого закона термодинамики
- •2.10. Чистые вещества и смеси газов
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Проверьте, как Вы усвоили материал
- •Тема 3. Термодинамические процессы
- •3.1. Последовательность и объём расчёта термодинамических процессов
- •3.2. Изохорный процесс: определение, осуществление и исследование
- •3.2.1. Исследование изохорного процесса
- •3.3. Изобарный процесс: определение, осуществление и исследование
- •3.3.1. Исследование изобарного процесса
- •3.4. Изотермический процесс: определение, осуществление, исследование
- •3.4.1. Исследование изотермического процесса
- •3.5. Адиабатный (изоэнтропический) процесс: определение, осуществление, исследование
- •3.5.1. Исследование адиабатного процесса
- •3.6. Сравнение адиабаты и изотермы
- •3.7. Обобщающее значение политропных процессов
- •3.8. Энтальпийная “I-s” диаграмма (“I-s” координаты)
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Проверьте, как Вы усвоили материал
- •Тема 4. Второй закон термодинамики
- •4.1. Понятие о круговых процессах (циклах). Прямой цикл (цикл тепловой машины)
- •4.2. Полезная работа цикла. Термический кпд цикла
- •4.3. Цикл Карно и теорема Карно
- •4.4. Обратные циклы (циклы холодильных машин)
- •4.5. Второй закон термодинамики. Формулировки второго закона термодинамики
- •4.6. Второй закон термодинамики и энтропия
- •4.7. Статистическая интерпретация второго закона термодинамики
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Информация к размышлению
- •Проверьте, как Вы усвоили материал
- •Тема 5. Идеальные циклы тепловых двигателей
- •5.1. Особенности термодинамического метода исследования циклов тепловых двигателей
- •5.2. Схема устройства и принцип работы авиационного газотурбинного двигателя (гтд)
- •5.3. Идеальный цикл гтд (цикл Брайтона – Стечкина)
- •5.4. Работа и термический кпд цикла гтд
- •5.6. Сравнение циклов Брайтона и Гемфри
- •5.7. Цикл с регенерацией тепла
- •5.8. Цикл со ступенчатым подводом тепла
- •5.9. Эксергетический метод термодинамического анализа
- •5.10. Идеальные циклы двигателей внутреннего сгорания (двс)
- •5.10.1. Идеальный цикл двс с подводом тепла
- •5.10.2. Идеальный цикл двс с подводом тепла при постоянном
- •5.10.3. Сравнение циклов Отто и Дизеля
- •5.10.4. Цикл двс со смешанным теплоподводом
- •Примеры решения задач
- •Решение
- •Решение
- •4. Эффективность цикла оцениваем по величине термического кпд цикла
- •Решение
- •Проверьте, как Вы усвоили материал
- •Заключение
- •Список использованной литературы
- •Приложение
- •Международная стандартная атмосфера (мса) гост 4401–81 (фрагмент)
- •Теплофизические величины
- •Соблюдайте гост 8.417 – 2002
1.3.2. Температура
Температура Т характеризует степень нагретости тела. По физическому смыслу температура является мерой интенсивности теплового движения молекул.
Представление о термодинамическом равновесии позволяет уточнить термодинамический смысл температуры.
С точки зрения термодинамики температура – это единственный параметр, одинаковый во всех точках нескольких систем или частей одной и той же системы в состоянии термодинамического равновесия.
Другие параметры состояния (давление, внутренняя энергия) остаются постоянными, но не обязательно одинаковыми во всех точках системы.
Важность этого положения настолько велика, что по предложению одного известного английского физика Р. Фаулера (1889–1944) оно было названо нулевым началом (законом) термодинамики.
Из термодинамического определения температуры следует, что этот параметр является функцией состояния системы, так как не зависит от начального состояния и предыстории системы, а определяется только состоянием системы в данный момент времени.
Это
же свойство температуры подтверждается
и её статистическим смыслом, в соответствии
с которым она служит мерой средней
кинетической энергии
![]() теплового движения частиц вещества:
теплового движения частиц вещества:
![]() ,
(1.4)
,
(1.4)
где к = 1,38·10-23 Дж/К – постоянная Больцмана.
Абсолютная температура Т отсчитывается по термодинамической шкале (в Кельвинах) от абсолютного нуля температуры, которому соответствует полное прекращение поступательного движения молекул. Для измерения температуры пользуются также международной практической температурной шкалой (в градусах Цельсия). Соотношение между этими шкалами выражается формулой
Т = t + 273,15 , К. (1.5)
Величина градуса по шкале Кельвина принимается равной градусу по стоградусной шкале Цельсия.
XIII Генеральная конференция по мерам и весам (1967 г. Резолюция 4) и ГОСТ 8.417-2002 с. 3, определяют термодинамическую шкалу температур посредством тройной точки воды. Как понять такое определение? Тройной точкой называется температура, при которой все три состояния, или, как говорят, все три фазы (лёд, вода, пар), находятся в равновесии. Тройная точка характеризуется давлением пара в 4,58 мм. рт. ст. и температурой 0,0075 °С (округлённо 0,01 °С). Только при этой температуре лёд, вода и пар могут находиться при одном давлении. А разве при обычном атмосферном давлении над смесью льда и воды нет пара? Есть, конечно, но давление его составляет лишь небольшую часть атмосферного давления и равняется приблизительно 4,5 мм. рт. ст. Если мы хотим воду изо льда при 0 °С и давлении в 1 атм. (760 мм. рт. ст.) превратить в пар такого же давления, то мы должны нагреть её до 100 °С (верхняя пунктирная горизонтальная линия на рис. 1.4.). При давлении ниже 4,58 мм. рт. ст. лёд переходит в пар, минуя жидкую фазу.
Разность между температурами какого-нибудь состояния в термодинамической и стоградусной шкалах составит:
273,16 – 0,01 = 273,15 °С.
Таким образом, температура исходной точки термодинамической шкалы (абсолютный нуль) по шкале Цельсия (стоградусной шкале) равна:
0 – 273,15 = – 273,15 °С.
Как правило, в повседневной жизни пишется упрощённо:
Т = (t + 273) K.
В Англии, в США и в некоторых других странах для измерения температуры принята шкала Фаренгейта (°F), в которой за 0 °F принята температура таяния смеси льда с поваренной солью, а температура таяния воды равна 212 °F и, следовательно, разность температур кипения воды и таяния льда по шкале Фаренгейта равна 212 – 32 = 180 °F.
Таким образом, 1 °F равен 100/180 = 5/9 °C.
На основании изложенного можно написать формулы пересчета температур из одной шкалы в другую:
t
°C
= [t
°F
– 32]·![]() ;
t
°F
=
;
t
°F
=
![]() ·t
°С
+ 32.
·t
°С
+ 32.
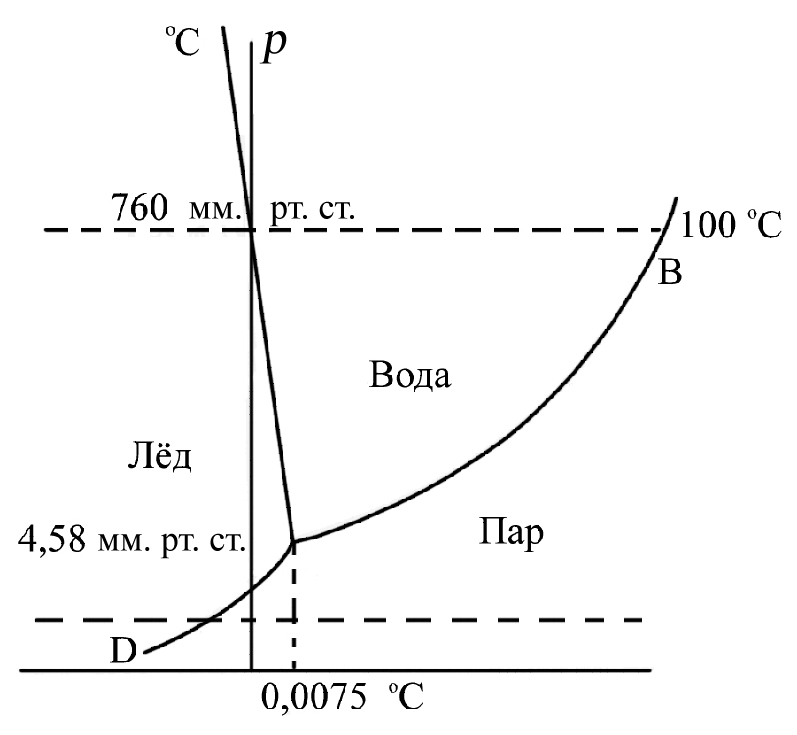
Рис. 1.4. График, иллюстрирующий тройную точку
Шкала Фаренгейта, отсчитанная от абсолютного нуля, называется шкалой Ранкина (°R) В этой шкале tо = 0 °С, Tо = 273,15 К соответствует 491,67 °R, а tk = 100 °С, Тк = 373,15 К равно 671,67 °R.
Температура измеряется с помощью термометров различных типов: жидкостных, газовых, электрических, звуковых. Например, измерение температуры газа за турбиной ГТД осуществляется с помощью электрического термометра, сигнал от которого передается на указатель температуры, размещённый в кабине пилотов.
Наряду с рассмотренными температурными шкалами применяются и другие температурные шкалы. Сравнение различных температурных шкал приведено в П. 1.
