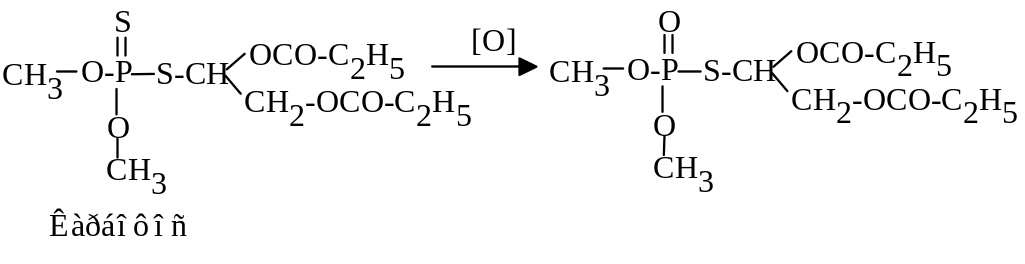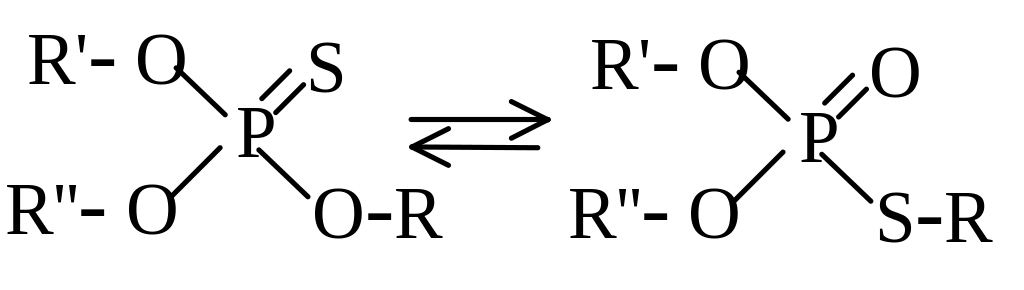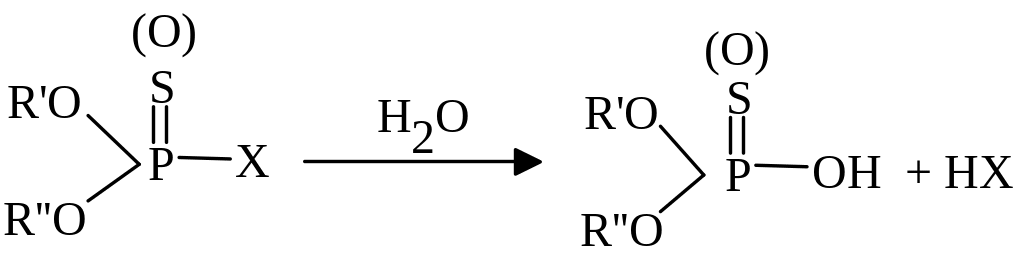- •1. Проблеми екології в сучасному світі
- •Вплив забруднень довкілля на живі організми
- •Крім того є багато неурядових програм поза оон.
- •2. Поняття хімічного складу об’єктів довкілля та основні підходи до аналізу
- •Контрольні запитання
- •3. Характеристика речовинного складу окремих об’єктів довкілля
- •3.1. Природне повітря та його забруднювачі
- •3.2. Природні води
- •3.3. Антропогенний вплив на води, забруднювачі вод
- •3.3.1. Контроль за складом вод залежно від їх використання
- •3.3.2. Контроль стічних вод різних виробництв
- •3.4. Ґрунти
- •3.4.1.Ґрунтоутворення, загальні характеристики ґрунту
- •3.4.2. Склад ґрунтів
- •3.4.3. Антропогенне забруднення ґрунтів та літосфери
- •3.5. Рослинність, як об’єкт довкілля
- •Контрольні запитання
- •4. Вплив хімічних речовин на живі організми
- •4.1. Роль макро- і мікроелементів для живих організмів
- •4.2. Вплив забруднень довкілля на живі організми
- •4.3. Перетворення токсичних речовин у довкіллі
- •Контрольні запитання
4.3. Перетворення токсичних речовин у довкіллі
Перетворення неорганічних речовин
As. Сполуки арсену у водоймі піддаються перетворенням, взаємодіючи з органічними речовинами. Найотруйніші органічні сполуки арсену: феніларсенатна кислота: C6H5-AsO-(OH)2; диметил- та метиларсенатна кислоти: (CH3)2-AsO-OH; CH3-AsO-(OH)2; бойова отрута люїзит CH3-CH=CH-AsCl2.
У пестицидах також є отруйні речовини, які містять арсен: Pb3(AsO4)2, Ca3(AsO4)2.
За участю анаеробних та аеробних мікроорганізмів у вологому середовищі відбувається відновлення арсенату і окиснення арсеніту з одночасним алкілюванням сполук арсену до летких (CH3)3As, (CH3)2As:
As(OH)3 CH 3AsO(OH)2 (CH3)2AsO(OH) CH3)2AsH |
Метиловані форми знайдені у воді, в шкаралупі яєць, морських мушлях, сечі.
Важкі метали у водному середовищі переважно утворюють комплекси з гуміновими речовинами, найчастіше фульвокислотами. За стійкістю комплексів металів з гуміновими речовинами їх можна розташувати в ряд: Hg2+>Cu2+>Ni2+, Zn2+>Co2+>Mn2+, Cd2+>Ca2+>Mg2+.
Cd. Гідроліз солей кадмію у водоймі починається при pH>9. Утворюється CdOH+, солі можуть сорбуватися зависями. Cd2+ утворює комплекси з органічними речовинами, але малостійкі. Вміст Cd у воді становить 0,01-0,5 мкг/л (до 17мкг/л у забрудненій); в атмосферних опадах >50 мкг/л.
Pb. У воді при рН>6 існує Pb(OH)+, при pH>10 – переважно Pb(OH)2. У таких формах плюмбум сильно сорбується донними відкладеннями. Вільних іонів Pb2+ у водоймі нема. Під впливом мікроорганізмів протікає метилювання неорганічних сполук плюмбуму, утворюються (CH3)4Pb, (C2H5)3Pb+, (C2H5)4Pb. Вміст Pb у воді <3 мкг/л; у воді техногенної зони >1000 мкг/л; в опадах становить1-50 мкг/л.
Hg. У водоймі залежно від рН та величини окисного потенціалу зустрічаються різні форми сполук меркурію. Найбільше є стійких комплексів [HgCl4]2-. При pH>4 сполуки Hg(II) утворюють малорозчинний гідрооксид Hg(OH)2, який переважно випадає в осад. У більш кислому середовищі у воді є невелика кількість розчинних сполук Hg2+, Hg22+, органічних сполук (C6H5-Hg-OOC-CH3, CH3-Hg-Г), комплекси з гумусовими речовинами. Чим вища солоність води, тим у меншій мірі сполуки меркурію вступають у реакції комплексоутворення.
Біологічне метилювання проходить у воді як за участю ферментів, так і фотохімічно, відбувається кругообіг сполук меркурію:
|
Вміст у прісній воді Hg – 0,02-0,1 мкг/л, CH3-Hg+ – 0,2-1 нг/л; у морській воді Hg – 0,01-0,03 мкг/л; в опадах вміст Hg – 0,01-1,0 мкг/л.
Cu. Сполуки купруму у воді є в різних формах: зависі; колоїдний розчин; розчинні сполуки (іони, дуже стійкі органічні та неорганічні комплекси). Велика кількість сполук купруму є у донних відкладеннях, однак при високій соленості та низьких рН вони легко переходить у розчин. Вміст купруму у воді: 0,5-1 мкг/л; у воді урбанізованих територій: – 2 мкг/л.
Ni. У водоймі гідрооксид та фосфат нікелю є у формі колоїдного розчину; утворюються комплексні сполуки нікелю з гуміновими речовинами. Вміст нікелю у воді становить 1-3 мкг/л; в опадах: – 0,02-5 мкг/л.
Zn. У водоймі при pH<6,7 існують іони Zn2+, утворюються стійкі комплекси з гумусовими речовинами; при pH>8 переважно є Zn(OH)2, який знаходиться у формі зависів та колоїдних частинок.
Вміст цинку у воді: 0,5-15 мкг/л
Cr. В окисному середовищі найстійкішим біхромат, який однак легко відновлюється до Cr3+, а останній дає стійкі комплекси. Велика кількість хрому поступає у водойму з комунальними стоками.
Перетворення пестицидів
Практично всі пестициди, які використовують у сільському господарстві, розкладаються в ґрунті мікроорганізмами. Це має велике значення для самоочищення ґрунтів та вод. З ґрунту та природних вод виділені різноманітні бактерії, гриби, актиноміцети і водорості, які приймають участь у розкладі. Наприклад, початковий етап розкладу ДДТ відбувається за участю анаеробних мікроорганізмів. Деградація токсичних речовин проходить за участю мікроорганізмів, а самі процеси каталізуються певними ферментами.
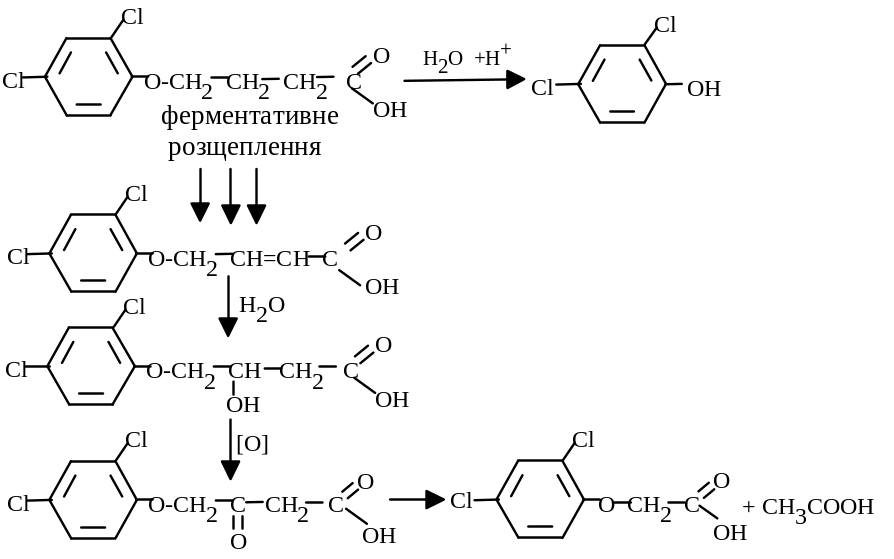
Розглянемо декілька прикладів перетворень токсичних пестицидів. Так 2,4-дихлорфеноксимасляна кислота перетворюється у нетоксичний 2,4-дихлорфенол, але при -окисненні аліфатичного ланцюга утворюється 2,4-дихлорфеноксиацетатна кислота з більш широким спектром фітотоксичності.
|
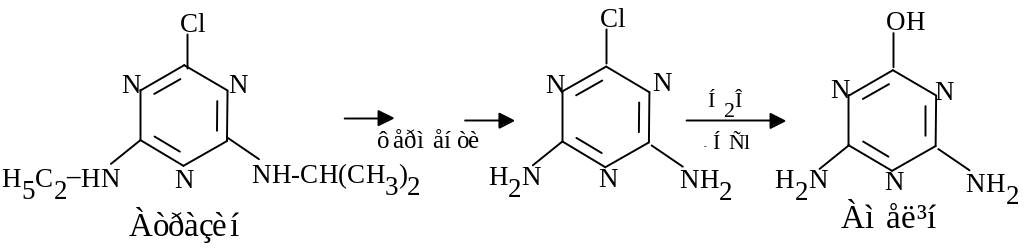
Гідролітичне дехлорування хлоразину веде до утворення гідроксихлоразину, однак при дезалкілюванні він перетворюється у триетазин та симазин з сильним фітотоксичним ефектом. Низка пестицидів, які є аналогами природних речовин, можуть бути джерелом живлення для мікроорганізмів.
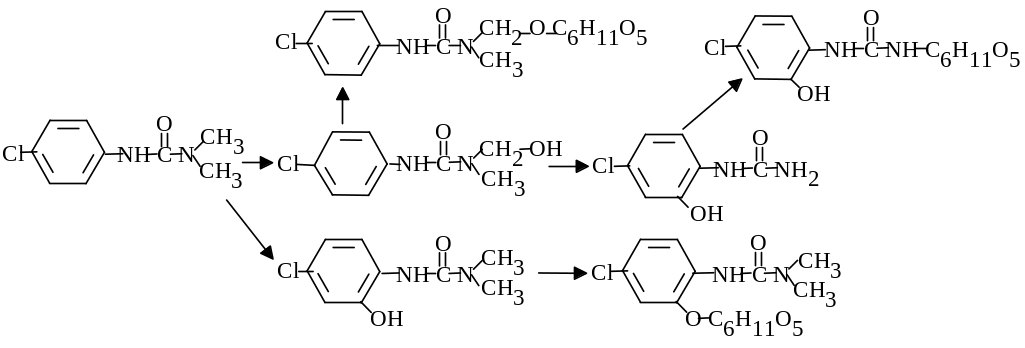
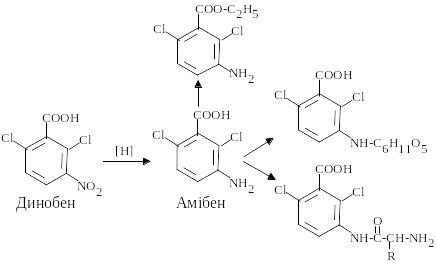
Для похідних тіофосфатної кислоти можливі різні шляхи метаболізму, але проходять переважно два. Перший – відбувається окисна десульфурація, при якій утворюються оксигеновмісні сполуки і зростає їхня токсичність для тварин. Другий шлях – гідроліз тіофосфатів і як наслідок детоксикація. Усі процеси проходять за участю мікроорганізмів, причому різних. Отже, в результаті перетворень накопичуються різноманітні продукти перетворення з різною фізіологічною дією, а які з них у найбільшій кількості – залежить від умов та наявних мікроорганізмів. Характерним для біохімічних процесів трансформації пестицидів є те, що, незалежно від шляху перетворень, утворюються певні продукти. Так для пестицидів з ароматичним кільцем продуктами є похідні фенолу і аніліну, які довго зберігаються у довкіллі (стабільність залежить від розташування замісників у ароматичному кільці).
Утворені феноли теж здатні до трансформації мікроорганізмами, спочатку внаслідок гідроксилювання, потім відбувається окиснення і руйнування кільця аж до повної мінералізації.
|
Іншим шляхом руйнування фенолів є полімеризація за участю ферментів.
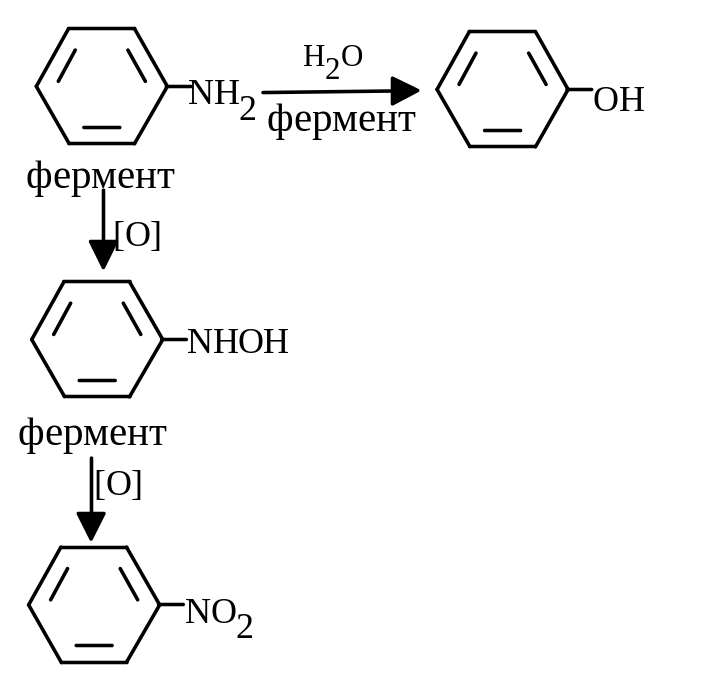
Аніліни теж трансформуються по-різному. Перший шлях – окисне дезамінування і утворення фенолів. Другий – окиснення аміногрупи до гідроксиламіну і нітробензолу. Третій шлях – конденсація анілінів і продуктів їхнього окиснення до азобензолу і утворення високо-молекулярних сполук. Всі процеси відбуваються за участю ферментів, а останній іде за участю ферменту оксидази, виявленого у грибів.
|
|
Фермент оксидаза каталізує процес конденсації хлорпохідних фенолів з хлорпохідними анілінів, а також з природними речовинами, які мають ті самі функціональні групи, наприклад з гуміновими речовинами.
|
Таким чином утворюються нові стійкі сполуки, які здатні тривалий час зберігатися у природі, наприклад у гумосфері.
Якщо у складі гумосфери є азобензоли, то вони виявляють канцерогенну дію. Тому перетворення пестициду в інші досить стабільні сполуки, зокрема високомолекулярні, не обов’язково веде до їхньої детоксикації.
Конденсація хлорпохідних фенолів призводить до утворення надзвичайно стійких та особливо токсичних діоксинів:
|
Переважно на ґрунти діють одночасно різними пестицидами. Мікробіологічна деградація суміші пестицидів може як призводити до їхньої детоксикації, так і до утворення інших токсичних сполук. Під впливом хлорметилкарбамату затримується процес конденсації продуктів трансформації гербіциду пропаніду до тетрахлорбензолу. Механізми можуть бути різними: один із компонентів гальмує розвиток мікроорганізмів, блокуються певні ферменти, особливо карбаматами. Викладене дозволяє зробити висновок, що комбінації пестицидів та послідовність їх внесення у ґрунт впливає на мікробіологічний стан ґрунту, а отже на процеси самоочищення ґрунту від отрутохімікатів. З екологічної та санітарно-гігієнічної точок зору найкращі до застосування є ті пестициди, які легко руйнуються мікроорганізмами, а потім піддаються повній мінералізації.
Ксенобіотики, потрапивши у рослину, перетворюються. Первинними процесами можуть бути гідроліз, окиснення, відновлення, гідроксилювання, дегалоїдування, дезалкілювання. Потім відбувається взаємодія продуктів перетворення з вуглеводами, переважно з глюкозою, амінокислотами. Утворюються продукти більш розчинні у воді і накопичуються в клітинах у вакуолях. Іноді наступає третій етап перетворень, часто це полімеризація, при якій утворюються нерозчинні продукти.
Розглянемо найважливіші шляхи перетворень пестицидів у рослинах. За участю активних рослинних ферментів дуже легко проходить процес гідролізу
сполук феноксикислот, а потім може іти приєднання глюкози:

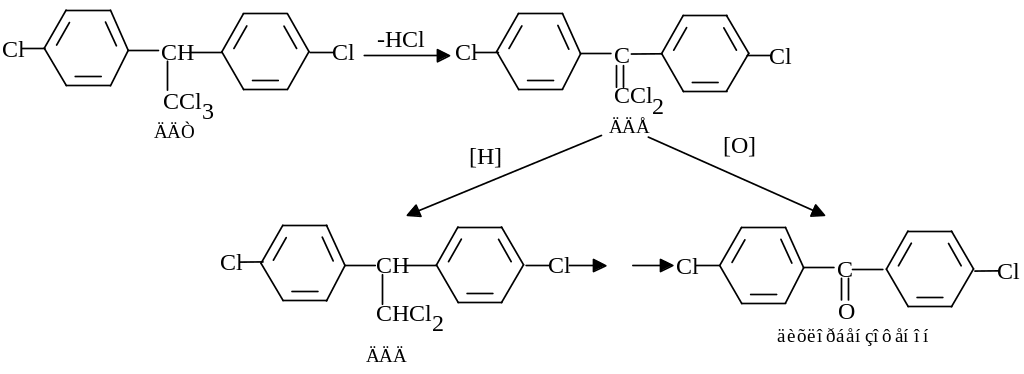
У рослинах ДДТ спочатку дехлорується, відновлюється і перетворюється у дихлорбензофенон:
|
Триазинові гербіциди в рослинах перетворюються в оксипохідні у процесі гідролітичного дехлорування і каталітичної дії ферментів:
|
У процесі перетворень гербіцидів на основі сечовини, хлорфеноксикислот і фосфорорганічних пестицидів відбувається дезалкілювання, а переважно на останній стадії приєднання глюкози, у результаті чого продукти легше піддаються детоксикації:
|
Тіофосфатні пестициди піддаються найчастіше окисному десульфуруванню:
|
|
Таким чином карбофос (малатіон) перетворюється у живих організмах, а також при тривалому нагріванні у більш токсичний ізомалатіон. Продукти перетворення пестицидів часто є більш ефективними інсектицидами. Якщо смертельна доза для щурів (на масу тіла) тіофосу становить 3,3 мг/кг, то продукту десульфурування – 1,4 мг/кг, а карбофосу і продукту перетворення відповідно 2,6 г/кг і 0,308 г/кг.
Похідні тіофосфорної кислоти легко ізомеризуються у тіолові ізомери, які переважно більш токсичні для комах та тварин:
|
Відновлення пестицидів з нітрофенільним радикалом – не дуже поширений процес. Одночасно з відновленням може іти процес дезалкілювання або приєднання вуглеводів, найчастіше глюкози, амінокислот, процес етерифікації:
Вуглеводневий ланцюг видовжується внаслідок утворенням ефірів з олігосахаридами, однак вони досить нестійкі, можуть зберігатися лише у вакуолях клітин. Якщо відбувається сполучення з амінокислотами, то утворюються поліпептиди з різними молекулярними масами.
|
Амінокислотні похідні проявляють токсичну фізіологічну дію, а при розкладі можуть вивільняти вихідну токсичну речовину.
|
Отже, пестициди в рослині перетворюються по-різному і всі процеси каталізуються різноманітними ферментами, які за нормальних умов беруть участь в обміні речовин. Тому у рослинних тканинах можна виявити як залишки самих пестицидів, так і продуктів перетворення, які можуть бути навіть більш токсичними.
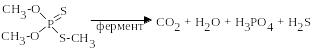
Якщо пестициди потрапляють в організм тварин і людини, то лише незначною мірою перетворюються у нетоксичні. Серед усіх пестицидів найлегше руйнуються фосфорорганічні, утворюючи СО2, Н3РО4 і воду.
|
Наприклад карбофос у живому організмі піддається дезалкілюванню та гідролізу, а за участю фермента розщеплюється; у присутності лугів та кислот піддається гідролізу.
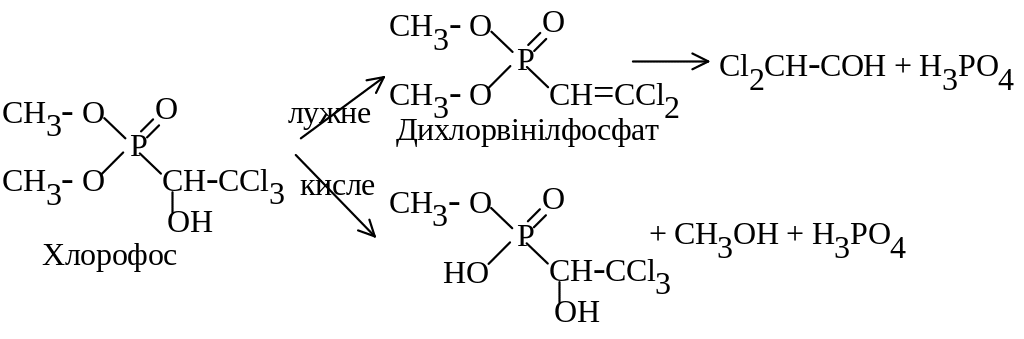
Хлорофос у лужному середовищі дегідрохлорується з перегрупуванням, а далі йде гідроліз до утворення фосфатної кислоти; у кислому середовищі теж утворюється фосфатна кислота:
|
Органами, які містять ферменти, здатні детоксикувати токсичні речовини, є печінка, органи дихання, шлунково-кишковий тракт та шкіра.
Процеси N-алкілгідроксилювання і N-дезалкілювання притаманні фосфорорганічним пестицидам:
 .
.
Проміжний продукт N-оксиалкіл є більш токсичним для ссавців, ніж вихідний пестицид, а кінцевий продукт може бути ще більш токсичним. Так перетворюється пестицид шрадан:
|
Продукт наступних перетворень може бути нетоксичним.
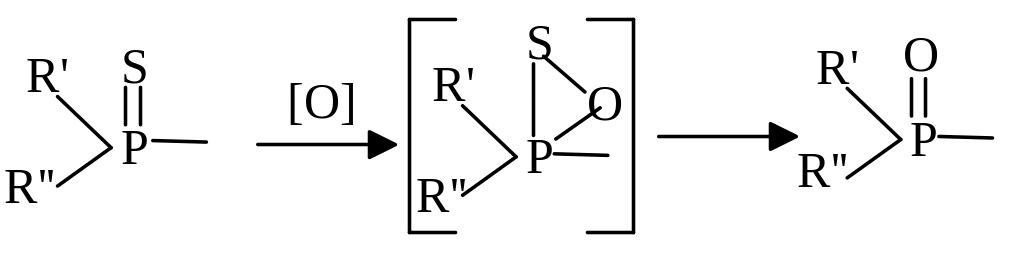
Фосфорорганічним пестицидам притаманна окисна десульфурація:
|
Тіонові сполуки (P=S) не є особливо токсичними, а проміжні оксони дуже токсичні для комах, тому мають інсектицидну дію. Для організму тварин і людини вони менш токсичні. Коли ж відбувається повний гідроліз, то токсична дія втрачається.
Гідроліз фосфорорганічних пестицидів та карбаматів є дуже поширеним процесом перетворення. Продукти гідролізу, за рідкими винятками, втрачають біологічну активність і токсичність. У випадку фосфорорганічних речовин найчастіше у реакцію гідролізу вступає частина молекули, сполучена з фосфором (Х):
|
Ферменти, які каталізують гідроліз, переважно діють на фосфати з групою Р=О і рідше на тіофосфати (P=S).
Якщо ж піддаються гідролізу карбамати, то утворюються метилкарбамінові (диметилкарбамінові) кислоти, які дальше гідролізують до амінів і СО2, а каталізують гідроліз ферменти:
|
Шляхами перетворень хлорорганічних пестицидів є аліфатичне та ароматичне гідроксилювання; окиснення атомів N i S у сполуках; дехлорування та дегідрохлорування, подібно як у рослинних організмах.
Під впливом фермента йде дезалкілювання, можливе окисненням:
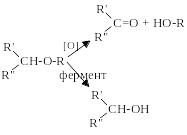
Утворюється альдегід або кетон.
Так, зокрема, перетворюється метоксихлор:
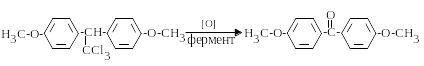
Циклодієни в складі пестицидів перетворюються окиснюються, гідратуються. Такий процес переважно притаманний хлорорганічним пестицидам (гептахлор, алдрин). Окиснення фрагменту циклодієну показано нижче:
|
Утворений оксид більш токсичний за вихідний пестицид і досить стійкий, однак в результаті гідратації відбувається його детоксикація.
Таким чином, пестициди, які потрапили в організмі тварин та людини, поступово руйнуються за участю різноманітних ферментів. Крім того участь беруть і інші речовини. Відомо, що іони Са2+ активують ферменти, які каталізують гідроліз більшості фосфорорганічних пестицидів, а хлорорганічні сполуки індукують дію ферменту оксидази і прискорюють окисний розпад пестицидів. Тому направлена дія певних ферментів могла б забезпечити повний розклад пестицидів у організмі і отже, очищення від них.

 AsO(OH)3
(CH3)3As
AsO(OH)3
(CH3)3As