
Неметаллы лекция 4
.pdf
vk.com/club152685050 | vk.com/id446425943
Получение и свойства водорода
6. Активация гомолитической диссоциации
2Na + H2 = 2NaH |
δ–H H δ– |
|
Na – Na – Na – Na – Na – Na |
7. Инициация радикалов
H2 |
|
2H• |
|
H |
2 |
+ O |
2OH• |
|
2 |
|
|
H• |
+ O |
OH• + O• • |
|
|
|
2 |
|
O• • + H2 |
OH• + H• |
||
OH• + H2 |
H2O + H• |
||
|
1) |
to |
инициирование |
2) |
h |
|
ν |
3)
разветвление
развитие
vk.com/club152685050 | vk.com/id446425943
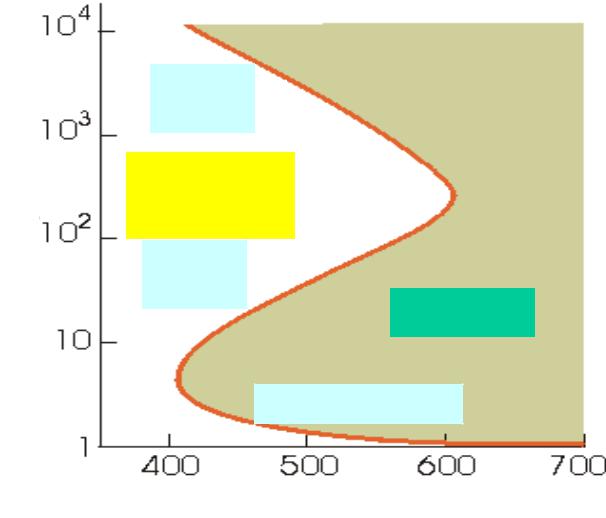
Взрывоопасность водорода
Для реакции 2H2 + O2 = 2H2O
Давление, мм.рт.ст
Третий
предел
Гладкая
реакция
Второй
предел
Взрыв
Первый предел
Температура, ОС
vk.com/club152685050 | vk.com/id446425943
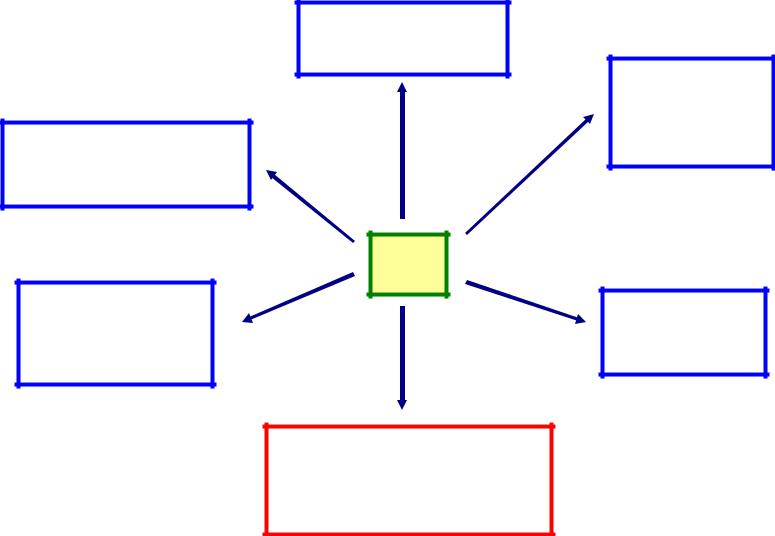
Применение водорода
Производство
металлов
Аммиак, пластики, Пищевая удобрения
промышленность
CH3OH, |
H2 |
Ракетное |
|
органический |
топливо |
синтез |
|
Топливные батареи, новые источники энергии
vk.com/club152685050 | vk.com/id446425943
Образование химической связи
χp(H) = 2.1
Si Ge B H As P C
1.92.0 2.0 2.1 2.2 2.2 2.6 E(H-H) = 435 кДж/моль
χ(H) > χ(Э) |
Эδ+··· Hδ– |
|
BeH2 |
χ(H) < χ(Э) |
Эδ– ··· Hδ+ |
|
H2S |
Энергия связи, кДж/моль
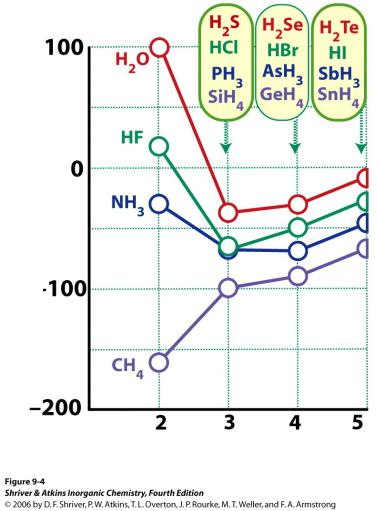
vk.com/club152685050 | vk.com/id446425943
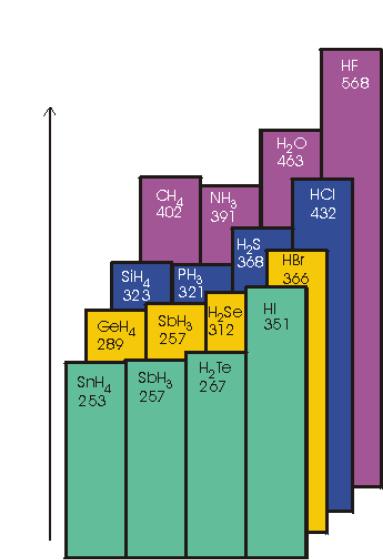
Водородная связь
Водородная связь образуется между связанным водородом и наиболее электроотрицательными элементами, имеющими неподеленную электронную пару
Е, кДж/моль |
|
F ··· H ··· F |
>200 |
H ··· FH |
29 |
H ··· OH2 |
25 |
H ··· NH3 |
17 |
H ··· SH2 |
7 |
Температура кипения, ОС
Номер периода
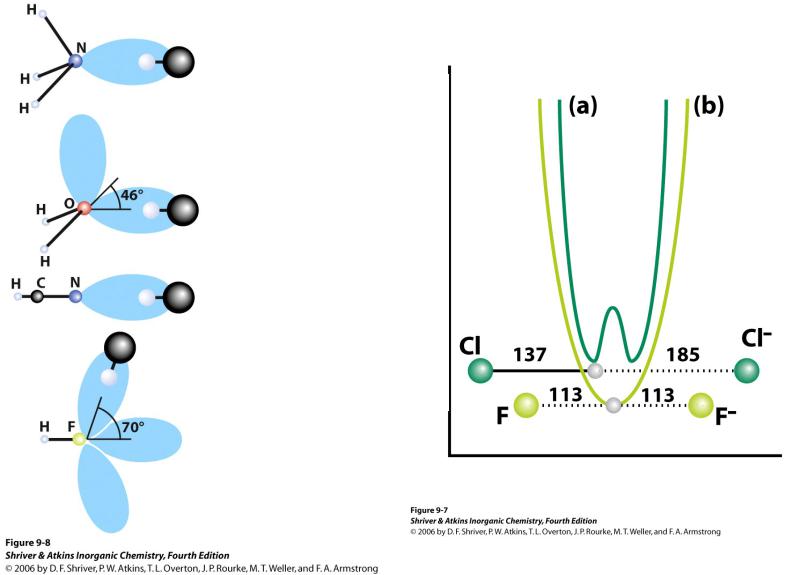
vk.com/club152685050 | vk.com/id446425943
Водородная связь
Потенциальная энергия
Длина связи
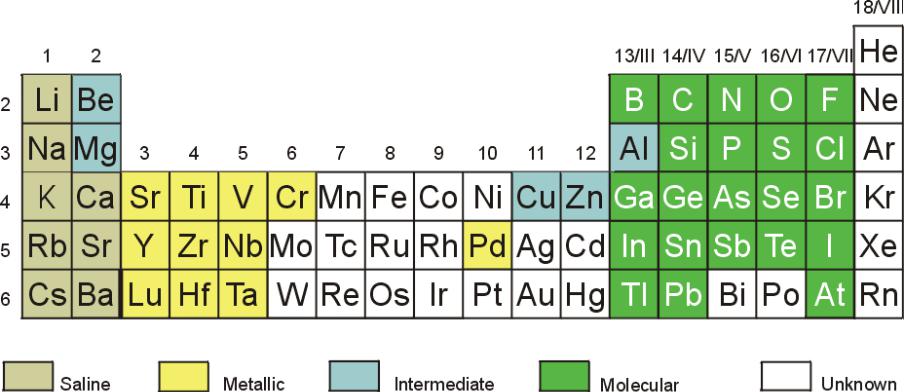
vk.com/club152685050 | vk.com/id446425943
Гидриды
|
|
|
|
|
|
|
|
|
|
солеобразные |
|
полимерные |
|
|
неизвестны |
||||
|
|
|
|||||||
металлические молекулярные
vk.com/club152685050 | vk.com/id446425943
Гидриды
1. Солеобразные гидриды
2Li + H2 = 2LiH (т.пл. 680 оС) NaH + H2O = NaOH + H2
4LiH + AlCl3 |
Et2O |
Li[AlH4] + 3LiCl↓ |
ТГФ
4NaH + BCl3  Na[BH4] + 3NaCl↓
Na[BH4] + 3NaCl↓
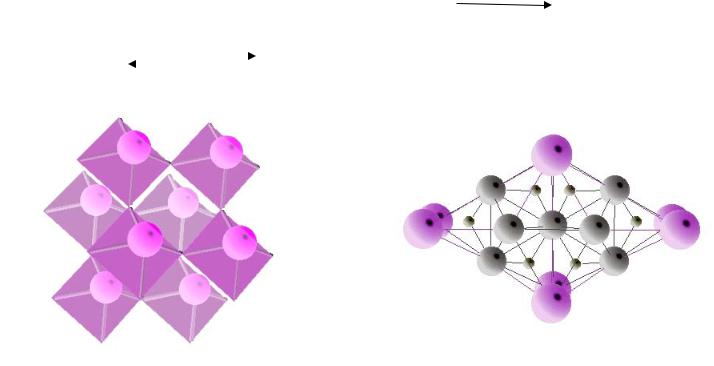
Солеобразные гидриды обладают структурами галогенидов щелочных и щелочноземельных металлов:
Ионные соединения!
MgH2
NaH
vk.com/club152685050 | vk.com/id446425943
Гидриды
2. Металлические гидриды Металлическая проводимость, нестехиометрия
Yb + H2 = YbH2 |
|
|
|
Pd |
|
|
YbH2 + 0.86[H] |
YbH2.86 |
|||
LaNi5 + 3H2 |
P |
LaNi5H6 |
(хранение водорода) |
||
t |
|||||
|
|
|
|
||
ZrHx LaNi5H6
vk.com/club152685050 | vk.com/id446425943
Гидриды
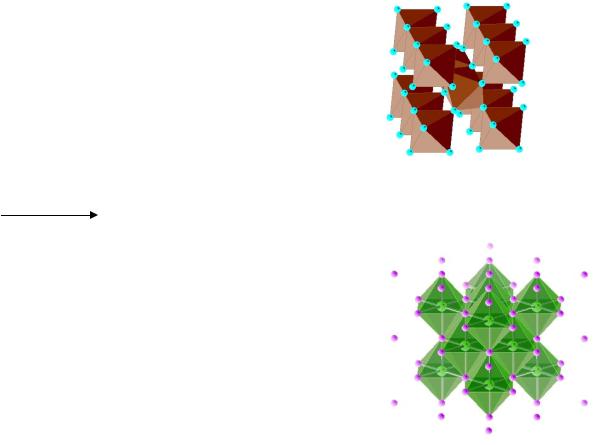
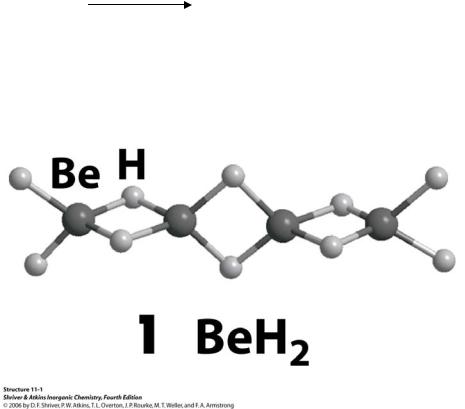
3. Полимерные гидриды
Устойчивы к действию воды и разбавленных кислот
2ZnI2 + LiAlH4 |
Et2O |
2ZnH2 |
+ LiI + AlI3 |
|
4CuSO4 + 3H3PO2 + 6H2O = 4CuH + 3H3PO4 + 4H2SO4
 μ2 - лиганд
μ2 - лиганд
