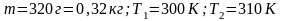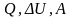Примеры решения задач
1. Кислород массой 320 г. Нагревают при постоянном давлении от 300 до 310к. Определить количество теплоты, поглощенное газом, изменение внутренней энергии и работу расширения газа.
Дано: |
|
Найти: |
|
Решение: Количество теплоты, необходимое для нагревания газа при постоянном давлении, определим из 1- го начала термодинамики:
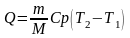 (1)
(1)
Здесь Ср - молярная изобарная теплоемкость, M – молярная масса газа;
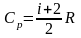 ,
где
,
где
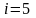 для кислорода как двухатомного газа;
для кислорода как двухатомного газа;
M=32
кг/кмоль =
Подставляя в (1) числовые значения, получим:
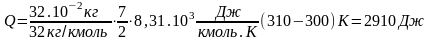
Изменение внутренней энергии газа:
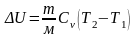 (2)
(2)
Подставляя
числовые значения и учтя, что
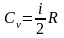 ,
получим:
,
получим:
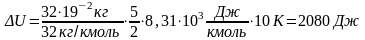
Работа
расширения газа при изобарном процессе:
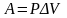 ,
(3), где
,
(3), где
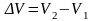 - изменение объема газа при расширении
можно найти из уравнения Клапейрона-Менделеева:
- изменение объема газа при расширении
можно найти из уравнения Клапейрона-Менделеева:
Для
двух состояний газа при изобарном
процессе:
 (4)
(4)
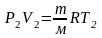 (5),
(5),
и тогда вычитая почленно (5) из (4), получим:

и подставляя в (3), находим:
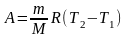 =
=
Проверка: Q = ∆U + A; 2910 Дж = 2080 Дж + 830 Дж.
Ответ: Q= 2910 Дж, U=2080 Дж, A=830Дж.
2. Как изменится энтропия 2 г водорода, занимающего объем 40 л при температуре 270К, если давление увеличить вдвое при постоянной температуре, а затем повысить температуру до 320К при постоянном объеме.
Дано: m = 2 г = 2∙10-3 кг; М = 2 кг/моль; V = 40 л = 4∙10-2 м3 Т1 = 270К; Т2 = 320К; Р2= 2Р1.
Найти: ΔS.
Решение:
Изменение энтропии определяется
формулой:
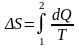 ,
,
где dQ – количество теплоты, полученное в данном процессе.
Изменение энтропии согласно условию происходит за счет двух процессов:
изотермического и 2) изохорического. Тогда:
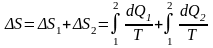
Количество теплоты dQ1 и dQ2 найдем из 1- го начала термодинамики для этих процессов:
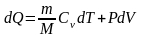 .
.
1)

P найдем из уравнения Клапейрона-Менделеева:
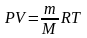 ,
тогда
,
тогда
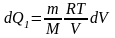 и
и
 ;
;
т.к. при T = const, P1V1 = P2V2 .
2)
 (т.к. dV
= 0 и dA
= 0 при V
= const)
(т.к. dV
= 0 и dA
= 0 при V
= const)
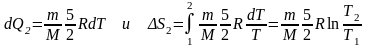 ;
;
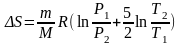
Подставляя численные значения, получим:
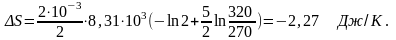
Ответ: S= -2,27Дж/К.
Задачи для самостоятельного решения
1.
Баллон объемом V=30
л заполнен кислородом. Температура Т
кислорода равна 350 К. Когда часть азота
израсходовали, давление в баллоне
понизилось на
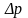 =200
кПа. Определить массу m
израсходованного кислорода. Процесс
считать изотермическим.
=200
кПа. Определить массу m
израсходованного кислорода. Процесс
считать изотермическим.
2.
В баллоне объемом V=20
л находится водород под давлением
 =600
кПа и температуре
=600
кПа и температуре
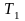 = 320 К. Когда из баллона было взято
некоторое количество водорода, давление
в баллоне понизилось до
= 320 К. Когда из баллона было взято
некоторое количество водорода, давление
в баллоне понизилось до
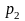 =400
кПа, а температура установилась
=400
кПа, а температура установилась
 =260
К. Определить массу m
водорода, взятого из баллона.
=260
К. Определить массу m
водорода, взятого из баллона.
3. Два сосуда одинакового объема содержат кислород. В одном сосуде давление =2,5 МПа и температура =700 К, в другом =3,5 МПа, =250 К. Сосуды соединили трубкой и охладили находящийся в них кислород до температуры T=230 К. Определить установившееся в сосудах давление p.
4. Вычислить плотность аргона, находящегося в баллоне под давлением р=2,5 МПа при температуре T=300 К.
5. Определить относительную молекулярную массу Mr газа, если при температуре T=154 К и давлении p =2,8 МПа он имеет плотность =6,1 кг/м3.
6. В сосуде объемом V=50 л находится кислород. Температура кислорода Т=350 К. Когда часть кислорода израсходовали, давление в баллоне понизилось на =150 кПа. Определить массу m израсходованного кислорода, если температура газа в баллоне осталась прежней.
7.
Количество вещества
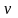 водорода равно 2,5 моль. Определить
внутреннюю энергию U
водорода, а также среднюю кинетическую
энергию <W>
молекулы этого газа при температуре T
=320 К.
водорода равно 2,5 моль. Определить
внутреннюю энергию U
водорода, а также среднюю кинетическую
энергию <W>
молекулы этого газа при температуре T
=320 К.
8.
Один баллон объемом
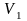 =15
л содержит кислород под давлением
=l,9
МПа, другой баллон –
=15
л содержит кислород под давлением
=l,9
МПа, другой баллон –
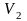 =30
л содержит азот под давлением
=0,9
МПа. Оба баллона были соединены между
собой и оба газа смешались, образовав
однородную смесь (без изменения
температуры). Найти парциальные давления
и
обоих
газов в смеси и полное давление p
смеси.
=30
л содержит азот под давлением
=0,9
МПа. Оба баллона были соединены между
собой и оба газа смешались, образовав
однородную смесь (без изменения
температуры). Найти парциальные давления
и
обоих
газов в смеси и полное давление p
смеси.
9.
Смесь водорода и азота общей массой
m=310 г при температуре T=500 К и давлении
p=1,46
МПа занимает объем V
=35 л. Определить массу
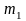 водорода и массу
водорода и массу
 азота.
азота.
10. В баллоне объемом V=22,4 л находится водород при нормальных условиях. После того как в баллон было дополнительно введено некоторое количество гелия, давление в баллоне возросло до p=0,25 МПа, а температура не изменилась. Определить массу m гелия, введенного в баллон.
11.
Смесь состоит из водорода с массовой
долей
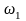 =2/9
и кислорода с массовой долей
=2/9
и кислорода с массовой долей
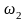 =7/9.
Найти плотность
такой смеси газов при температуре
T=350 К и давлении p=0,25
МПа.
=7/9.
Найти плотность
такой смеси газов при температуре
T=350 К и давлении p=0,25
МПа.
12.
Смесь кислорода и азота находится в
сосуде под давлением p=1,2
МПа. Определить парциальные давления
и
газов, если массовая доля
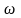 кислорода в смеси равна 20 %.
кислорода в смеси равна 20 %.
13. В сосуде объемом V=15 л при температуре T=350 К находится смесь азота массой =7 г и водорода массой =3 г. Определить давление p смеси.
14. Смесь азота с массовой долей =87,5% и водорода с массовой долей =12,5% находится в сосуде объемом V=20 л при температуре T = 560 К. Определить давление p смеси, если масса m смеси равна 8 г.
15. Определить суммарную кинетическую энергию Eк поступательного движения всех молекул газа, находящегося в сосуде объемом V=10 л под давлением p=250 кПа.
16. Количество вещества водорода =l,5 моль, температура T= 273 К. Определить суммарную кинетическую энергию Eк поступательного движения всех молекул этого газа.
17. Определить среднюю кинетическую энергию <W> одной молекулы водяного пара при температуре T=650 К.
18.
Определить среднюю квадратичную скорость
 молекулы газа, заключенного в сосуде
объемом V=10
л под давлением p
= 250 кПа. Масса газа m=0,23 г.
молекулы газа, заключенного в сосуде
объемом V=10
л под давлением p
= 250 кПа. Масса газа m=0,23 г.
19.
Водород находится при температуре T=325
К. Найти среднюю кинетическую энергию
 вращательного движения одной молекулы,
а также суммарную кинетическую энергию
Eк
всех молекул этого газа, если количество
вещества водорода
=1,5
моль.
вращательного движения одной молекулы,
а также суммарную кинетическую энергию
Eк
всех молекул этого газа, если количество
вещества водорода
=1,5
моль.
20.
При какой температуре средняя кинетическая
энергия
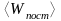 поступательного
движения молекулы газа равна 4,14
поступательного
движения молекулы газа равна 4,14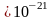 Дж?
Дж?
21.
В азоте взвешены мельчайшие пылинки,
которые движутся так, как если бы они
были очень крупными молекулами. Масса
m
каждой пылинки равна 4∙10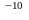 г.
Газ находится при температуре T=300
К. Определить средние квадратичные
скорости Vкв
,
а также средние кинетические энергии
поступательного движения
молекулы
азота и пылинки.
г.
Газ находится при температуре T=300
К. Определить средние квадратичные
скорости Vкв
,
а также средние кинетические энергии
поступательного движения
молекулы
азота и пылинки.
22. Определить показатель адиабаты у идеального газа, который при температуре T=350 К и давлении p=0,4 МПа занимает объем V=300 л и имеет теплоемкость CV =857 Дж/К.
23.
Определить относительную молекулярную
массу Mr
и молярную массу
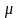 газа, если разность его удельных
теплоемкостей
газа, если разность его удельных
теплоемкостей
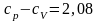 кДж/(кг∙К).
кДж/(кг∙К).
24.
В сосуде объемом V=25
л находится при нормальных условиях
двухатомный газ. Определить теплоемкость
 этого газа при постоянном объеме.
этого газа при постоянном объеме.
25.
Определить молярные теплоемкости газа,
если его удельные теплоемкости
=10,4
кДж/(кг∙К) и
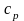 =14,6
кДж/(кг∙К).
=14,6
кДж/(кг∙К).
26.
Найти удельные
и
и молярные
и
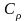 теплоемкости водорода и аргона.
теплоемкости водорода и аргона.
27. Вычислить удельные теплоемкости газа, зная, что его молярная масса =4∙10-3 кг/мoль и отношение теплоемкостей / =1,67.
28.
Трехатомный газ под давлением p=240
кПа и температуре t=25 0С
занимает объем V=15
л. Определить теплоемкость
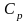 этого газа при постоянном давлении.
этого газа при постоянном давлении.
29. Одноатомный газ при нормальных условиях занимает объем V=15 л. Вычислить теплоемкость этого газа при постоянном объеме.
30. Определить удельные теплоемкости и водорода, в котором половина молекул распалась на атомы.
31. В сосуде находится смесь двух газов – водорода массой =5 г и азота массой =3 г. Определить удельные теплоемкости и такой смеси.
32.
Смесь двух газов состоит из аргона
массой
=5
г и кислорода массой
=2
г. Найти отношение теплоемкостей
 этой смеси.
этой смеси.
33. Найти молярные теплоемкости и смеси кислорода массой =3,5 г и азота массой =1,8 г.
34.
Относительная молекулярная масса газа
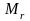 =30,
показатель адиабаты
=30,
показатель адиабаты
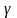 =1,40.
Вычислить удельные теплоемкости
и
этого газа.
=1,40.
Вычислить удельные теплоемкости
и
этого газа.
35. Какая часть молекул двухатомного газа распалась на атомы, если показатель адиабаты образовавшейся смеси равен 1,5?
36. Найти среднее число столкновений <Z> в единицу времени и длину свободного пробега <L> молекулы гелия, если газ находится под давлением p=2,5 кПа при температуре T =270 К.
37. Водород находится под давлением p=20 кПа и имеет температуру Т =300 К. Определить среднюю длину свободного пробега <L> молекулы такого газа.
38. При нормальных условиях длина свободного пробега <L> молекулы водорода равна 0,112 пм. Определить эффективный диаметр d молекулы водорода.
39.
Какова средняя арифметическая скорость
<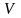 >
молекул кислорода при нормальных
условиях, если известно, что средняя
длина свободного пробега <L>
молекулы при этих условиях равна 100 нм.
>
молекул кислорода при нормальных
условиях, если известно, что средняя
длина свободного пробега <L>
молекулы при этих условиях равна 100 нм.
40. Кислород находится под давлением p=233 кПа при температуре T=250 К. Вычислить среднее число столкновений <Z> в единицу времени молекулы кислорода при этих условиях.
41.
Кислород массой m=200 г занимает объем
=100
л и находится под давлением
==200 кПа. При нагревании газ расширился
при постоянном давлении до объема
=300
л, а затем его давление возросло до
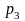 =500
кПа при неизменном объеме. Найти изменение
внутренней энергии
газа, совершенную им работу А и теплоту
Q,
переданную газу. Построить график
процесса.
=500
кПа при неизменном объеме. Найти изменение
внутренней энергии
газа, совершенную им работу А и теплоту
Q,
переданную газу. Построить график
процесса.
42. Объем водорода при изотермическом расширении увеличился в n=3 раза. Определить работу А, совершенную газом, и теплоту Q, полученную им при этом. Масса m водорода равна 200 г.
43.
Кислород массой m=60
г, имевший температуру T=300 К, адиабатически
расширился, увеличив объем в
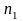 =3
раза. Затем при изотермическом сжатии
объем газа уменьшился в
=3
раза. Затем при изотермическом сжатии
объем газа уменьшился в
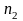 =2
раза. Определить полную работу A,
совершенную газом, и конечную температуру
Т газа.
=2
раза. Определить полную работу A,
совершенную газом, и конечную температуру
Т газа.
44. Аргон массой m =0,2 кг был изобарически нагрет от температуры T1=250 К до температуры T2=400 К. Определить работу A, совершенную газом, полученную им теплоту Q и изменение внутренней энергии азота.
45. Кислород массой m =340 г, имевший температуру =270 К, был адиабатически сжат. При этом была совершена работа A=25 кДж. Определить конечную температуру Т газа.
46. Во сколько раз увеличится объем водорода, содержащий количество вещества =0,4 моль при изотермическом расширении, если при этом газ получит теплоту Q=800 Дж? Температура водорода Т =300 К.
47. В баллоне при температуре = 145 К и давлении =2МПa находится кислород. Определить температуру и давление кислорода после того, как из баллона будет очень быстро выпущена половина газа.
48.
Определить работу
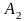 изотермического сжатия газа, совершающего
цикл Карно, КПД которого
изотермического сжатия газа, совершающего
цикл Карно, КПД которого
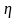 =0,4
, если работа изотермического расширения
равна
=0,4
, если работа изотермического расширения
равна
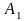 =8
Дж.
=8
Дж.
49.
Газ, совершающий цикл Карно, отдал
охладителю теплоту
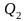 =14
кДж. Определить температуру
нагревателя, если при температуре
охладителя
=280
К работа цикла A=6 кДж.
=14
кДж. Определить температуру
нагревателя, если при температуре
охладителя
=280
К работа цикла A=6 кДж.
50.
Газ, являясь рабочим веществом в цикле
Карно, получил от нагревателя теплоту
 =4,38
кДж и совершил работу A=2,4 кДж. Определить
температуру нагревателя, если температура
охладителя
=273
К.
=4,38
кДж и совершил работу A=2,4 кДж. Определить
температуру нагревателя, если температура
охладителя
=273
К.
51. Газ, совершающий цикл Карно, отдал охладителю 67 % теплоты, полученной от нагревателя. Определить температуру охладителя, если температура нагревателя =430 К.
52.
Во сколько раз увеличится коэффициент
полезного действия
цикла Карно при повышении температуры
нагревателя от
=380 К до
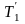 =560
К? Температура охладителя
=280
К.
=560
К? Температура охладителя
=280
К.
53. Идеальная тепловая машина работает по циклу Карно. Температура нагревателя равна 500 К, температура охладителя =250 К. Определить термический КПД цикла, а также работу , совершенную рабочим веществом при изотермическом расширении, если при изотермическом сжатии совершена работа =70 Дж.
54. Газ, совершающий цикл Карно, получает теплоту =84 кДж. Какую работу А совершает газ, если температура нагревателя в три раза выше температуры охладителя?
55. Совершая цикл Карно, газ получил от нагревателя теплоту =500 Дж и совершил работу А =100 Дж. Температура нагревателя = 400 К. Определить температуру охладителя.
56. Какую работу А надо совершить при выдувании мыльного пузыря, чтобы увеличить его объем от =8 см3 до =16 см3? Считать процесс изотермическим.
57.
Какая энергия Е выделится при слиянии
двух капель ртути диаметром
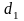 =0,8
мм и
=0,8
мм и
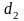 =1,2
мм в одну каплю?
=1,2
мм в одну каплю?
58. Пространство между двумя стеклянными параллельными пластинками с площадью поверхности S=100 см2 каждая, расположенными на расстоянии L=20 мкм друг от друга, заполнено водой. Определить силу F, прижимающую пластинки друг к другу. Считать мениск вогнутым с диаметром d, равным расстоянию между пластинками.
59.
Глицерин поднялся в капиллярной трубке
диаметром канала d
= 1 мм на высоту h=20 мм. Определить
коэффициент поверхностного натяжения
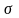 глицерина. Считать смачивание полным.
глицерина. Считать смачивание полным.
60.
Ụ-образный сосуд состоит из сообщающихся
широкой и узкой трубок. При наливании
в сосуд воды между ее уровнями в узкой
и широкой трубках устанавливается
разность h
= 8,0 см. Внутренний радиус широкой трубки
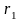 = 5,00 мм. Считая смачивание полным, найти
радиус узкой трубки
= 5,00 мм. Считая смачивание полным, найти
радиус узкой трубки
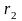 .
.
Таблица вариантов
вариант |
№ задачи |
||||
1 |
2 |
3 |
4 |
5 |
|
1 |
2 |
11 |
22 |
30 |
42 |
2 |
3 |
13 |
25 |
32 |
44 |
3 |
4 |
15 |
28 |
34 |
46 |
4 |
5 |
17 |
21 |
36 |
48 |
5 |
1 |
19 |
24 |
38 |
50 |
6 |
6 |
12 |
27 |
40 |
52 |
7 |
10 |
14 |
30 |
31 |
55 |
8 |
9 |
16 |
23 |
33 |
53 |
9 |
8 |
18 |
26 |
35 |
58 |
10 |
7 |
20 |
29 |
37 |
43 |