
- •Классификация веществ, вызывающих отравление
- •Химическая классификация:
- •2. Практическая классификация (имеет большое значение для профилактики отравлений):
- •3. Гигиеническая классификация (основана на количественной оценке токсической опасности хим веществ в соответствии со значениями токсикологических параметров (Доза смертельная средняя (dl50) :
- •4. Токсикологическая классификация (разделяет хим вещества по действию на организм, т.Е. Выделяет физиологические системы, работа которых нарушается при действии токсиканта):
- •5. Классификация по «избирательной токсичности» (учитывает процессы формирования токсических эффектов при их взаимодействии с рецепторами токсичности, расположенными в органах/системах - мишенях):
- •I. Токсические вещества органической природы.
- •II. Токсикологические вещества неорганической природы.
I. Токсические вещества органической природы.
![]() 1.
Группа токсикологически важных веществ,
изолируемых дистилляцией («летучие
яды»): синильная кислота, спирты,
этиленгликоль, алкилгалогениды
(хлороформ, хлоралгидрат, четыреххлористый
углерод, дихлоэтан), формальдегид,
ацетон, фенол, уксусная кислота.
1.
Группа токсикологически важных веществ,
изолируемых дистилляцией («летучие
яды»): синильная кислота, спирты,
этиленгликоль, алкилгалогениды
(хлороформ, хлоралгидрат, четыреххлористый
углерод, дихлоэтан), формальдегид,
ацетон, фенол, уксусная кислота.
2. Группа токсикологически важных веществ, изолируемых экстракцией и сорбцией:
лекарственные средства (барбитураты, алкалоиды, синтетические лекарственные вещества – 1,4-бензодиазепины, производные фенотиазина, фенилалкиламины);
наркотические вещества (каннабиноиды, эфедрон);
пестициды (ФОС, хлорорганические – гептахлор, гексахлорциклогексан, производные карбаминовой кислоты – севин).
II. Токсикологические вещества неорганической природы.
Группа токсикологически важных веществ, изолируемых минерализацией: «металлические яды» - соединения Ва, Pb, Mn, As, Cu, Sb, Bi, Hg и др.
Группа токсикологически важных веществ, изолируемых экстракцией водой: кислоты (серная, азотная, соляная), щелочи (гидроксиды натрия, калия, аммония), нитраты и нитриты.
Группа токсикологически важных веществ, требующих особых методов изолирования: соединения фтора.
Группа веществ, не требующих особых методов изолирования: вредные пары и газы, оксид углерода.
Степень токсичности вещества определяет ДОЗА
Детоксикационная терапия (детокс) Детоксикационная терапия - это выведение токсинов из организма человека. Болезни, для лечения которых незаменим этот метод:
приём чрезмерных доз алкоголя идругих психоактивных веществ;
лекарственная интоксикация (прием препаратов, содержащих токсичные вещества, или прием в больших дозировках);
пищевые отравления;
нарушение работы кишечника - дисбактериоз;
гепатиты различной формы;
заболеванияя ротоносоглотки – ангина, фарингит, грипп, ОРЗ;
пародонтит, пародонтоз, гингивит;
заболевания почек;
аллергические состояния;
стресс и т.д.
етоксикация (лат. приставка de — означающая устранение, прекращение + др.-греч. τοξίνη — яд) — разрушение и обезвреживание различных токсических веществ химическими, физическими или биологическими методами.
Детоксикация (мед.) — естественное и искусственное удаление токсинов из организма.
Естественные методы детоксикации подразделяются
Естественные: цитохромоксидазная система печени — окисление, иммунная система — фагоцитоз, связывание с белками крови,экскреторная — выведение с помощью печени, почек, кишечника, кожи и легких.
Стимулированные: применение медикаментозных и физиотерапевтических методов стимулирующих естественные методы детоксикации.
[править]Искусственные методы детоксикации подразделяются
Физические- механическое удаление из организма токсических веществ посредством очистки кожи, слизистых оболочек и крови современными методиками:
сорбционными — гемосорбция, энтеросорбция, лимфосорбция, плазмосорбция,
фильтрационными методиками — гемодиализ, ультрафильтрация, гемофильтрация, гемодиафильтрация,
аферезные методы — плазмаферез, цитаферез, селективная элиминация (криоседиментация, гепаринкриоседиментация).
Химические — связывание, дезактивация, нейтрализация и окисление (антидоты, сорбенты, антиоксиданты, непрямое электрохимическое окисление, квантовая гемотерапия).
Биологические — введение вакцин и сыворотки крови.
[править]Детоксикационная терапия
Детоксикационная терапия или современное определение эфферентная терапия, после стихания ажиотажа, заняла достойное и взвешенное место в современной медицине, но наиболее популярна и рекламируема остаётся в области наркологии и косметологии.
Может быть:
Интракорпоральной — энтеросорбция, непрямое электрохимическое окисление крови, квантовая гемотерапия (ультрафиолетовое облучение крови (УФОК), внутривенная лазеротерапия, озонотерапия).
Экстракорпоральной — гемосорбция, плазмаферез, гемодиализ, гемофильтрация, гемодиафильтрация, криоседиментация.
Искусственное удаление токсинов из организма может рассматриваться как временная замена или стимуляция одной из страдающих в каждом конкретном случае естественной системы детоксикации:
Монооксидазной системы печени (частично) — гемосорбцией, непрямым электрохимическим окислением крови, ультрафиолетовое облучение крови (УФОК), низкопоточной мембранной оксигенацией крови.
Экскреторной — гемодиализом, ультрафильтрацией, гемофильтрацией, гемосорбцией, плазаферезом, плазмосорбцией, лимфосорбцией.
Иммунной — иммуносорбция, цитаферез, ультрафиолетовое облучение крови (УФОК).
Детоксикация — это процесс обезвреживания ядов и ускорения их выделения из организма. Различные методы детоксика-ции способствуют освобождению желудка и кишок от еще невсо-савшегося в кровь яда, а также освобождению крови и тканей организма от находящихся в них токсического вещества и егометаболитов.
Освобождение организма от ядов производится путем усиления определенных естественных физиологических процессов (вызывание рвоты, промывание желудка, очищение кишок, форсированный диурез, гипервентиляция), искусственной детоксикации (гемодиализ, перитониальный диализ, гемосорбция, обменное переливание крови и др.) или методом антидотной терапии.
Указанные выше методы освобождения организма от ядов производятся специалистами-медиками. Однако химики-токсикологи должны знать принципы указанных выше мероприятий и процедур, направленных на удаление из организма ядов и их метаболитов. Необходимость знания этих мероприятий химиками-токсикологами связана с тем, что они должны производить исследования рвотных масс, мочи, диализатов и других жидкостей, полученных в процессе детоксикации. Ниже приводится краткое описание основных методов детоксикации.
Вызывание рвоты. После поступления ядов в желудок может наступить рефлекторная рвота, как самопроизвольный акт. При этом часть яда удаляется из желудка с рвотными массами. Однако не всегда после поступления яда в желудок наступает рвота. Ее можно вызвать путем механического раздражения глотки и корня языка, а также применением некоторых лекарственных средств (апоморфин и др.).
При отравлении сильными кислотами и концентрированными растворами едких щелочей удаление яда из желудка с рвотными массами является нежелательным. Выделяясь во время рвоты наружу, эти веществаусиливают степень повреждения пищевода. Кроме этого, рвотные массы, содержащие сильные кислоты ищелочи, могут попадать в дыхательные пути и вызывать их ожог.
Промывание желудка. Для детоксикации широко применяется промывание желудка с помощью зонда. Приотравлении хлорорганическими и фосфорсодержащими ядохимикатами промывание желудка производится несколько раз через 3—4 ч.
Больные, отравленные наркотическими веществами, в течение нескольких суток могут находиться в бессознательном состоянии. Таким больным промывают желудок несколько раз (через 4—6 ч). При однократном промывании из желудка удаляется основная часть невсосавшегося яда. Однако после этого, в результате обратной перистальтики, из кишок в желудок может поступать определенное количество яда, для удаления которого необходимо проводить повторное промывание желудка.
Желудок промывают также тем больным, у которых наступила рвота, но нет уверенности в том, что ее следствием было полное опорожнение желудка. Промывают желудок также и при отравлении сильнымикислотами. В этих случаях для промывания желудка нельзя применять раствор гидрокарбоната натрия. При взаимодействии кислот и гидрокарбоната натрия выделяется большой объем оксида углерода (IV), который значительно расширяет стенки желудка. В результате этого усиливаются боли в области желудка и может возникнуть кровотечение. Промывание желудка противопоказано при отравлении ядами, вызывающими судороги (стрихнин и др.)· Введение зонда таким больным увеличивает частоты и тяжести судорог.
Чтобы воспрепятствовать всасыванию яда, оставшегося в желудке после промывания, больным назначаютсуспензию активированного угля в воде или другие сорбенты, поглощающие яды и препятствующие проникновению их в кровь.
После вызывания рвоты и промывания желудка больным назначают слабительные средства, способствующие выведению содержимого кишок и освобождению их от ядовитых веществ. С помощью слабительных средствкишки освобождаются не только от находящегося в них яда, но и от ядов, уже всосавшихся в кровь, а затем выделившихся в пищевой канал через слизистую кишок или с желчью. В качестве слабительных средствприменяют вазелиновое масло (100—150 мл), хорошо растворяющее некоторые жирорастворимые яды и некоторые другие слабительные.
Форсированный диурез. Это один из способов ускоренного удаления токсических веществ из организма, выделяющихся с мочой. Форсированный диурез позволяет удалять уже всосавшийся яд из кровеносного русла (был предложен в 1948 г. для лечения острых отравлений снотворными средствами).
Пользуясь методом форсированного диуреза, больным внутривенно вводят 1,5—2 л жидкости (изотонический раствор хлорида натрия, 5 %-й раствор глюкозы и др.)· Для стимуляции диуреза назначают диуретические средства. Ими могут быть так называемые осмотические диуретики (15—20 %-е растворы мочевины илиманнита). После внутривенного вливания раствора диуретика вводят растворы электролитов, содержащихионы калия и натрия, со скоростью, равной скорости диуреза (500—800 мл/ч).
Скорость выделения некоторых ядов из организма зависит от рН мочи. Чтобы моча, выделяющаяся изорганизма, имела более щелочную реакцию, больным внутривенно вводят растворы лактата натрия,гидрокарбоната натрия или трисамина (триоксиметиламинометанола H 2 N (CH 2 OH) 3 ).
От рН мочи зависит диссоциация в ней веществ, являющихся слабыми кислотами или слабыми основаниями. Чем лучше диссоциируют ядовитые вещества, тем в больших количествах они выделяются с мочой.
При небольшом смещении рН артериальной крови в щелочную область повышается содержаниебарбитуратов в плазме и уменьшается содержание их в тканях. Это объясняется увеличением ионизациимолекул барбитуратов и снижением проницаемости этих веществ через клеточные мембраны.
Метод форсированного диуреза в основном применяется при отравлении веществами, которые легко выводятся из организма почками. Этот метод является малоэффективным в тех случаях, если токсическиевещества связаны с белками прочными связями, а также если яды относятся к числу жирорастворимыхвеществ.
Гипервентиляция (форсированное дыхание) в ряде случаев является эффективным методом ускоренного выведения некоторых ядов из организма. Этот метод применяется только при отравлении летучими ядами, которые в определенной степени выделяются из организма легкими с выдыхаемым воздухом. Для гипервентиляции применяется аппарат искусственного дыхания.
Метод гипервентиляции показан при отравлении спиртами, бензином, ацетоном, хлороформом,трихлорэтиленом, растворителями для красок, оксидом углерода (II) и др. Однако имеется и ряд противопоказаний для применения этого метода.
Гемодиализ — один из эффективных методов ускорения выведения токсических веществ из организма. Он основан на явлении диализа, используемого для освобождения крови от токсических веществ. Гемодиализ проводится с помощью аппарата, известного под названием «искусственная почка». Этот аппарат снабженполупроницаемой мембраной, через которую из крови переходят токсические вещества в процессе гемодиализа.
Гемодиализ применяется при отравлении веществами, которые имеют небольшую молекулярную массу и проходят через полупроницаемую мембрану. Метод гемодиализа применяется для выведения из организмабарбитуратов, изониазида, дифе-нилгидантоина, хлордиазепоксида, этиленгликоля, метилового спирта,четыреххлористого углерода, анилина, хинина, уксусной кислоты, производных фенотиазина, растворимыхсолей ртути, мышьяка, кадмия, свинца, фторидов и других веществ, вызвавших отравление.
Гемодиализ особенно эффективен в тех случаях, когда его применяют в ранней стадии острого отравления (в первые 24 ч после поступления токсического вещества в организм). Поэтому такой метод детоксикацииорганизма называется «ранний гемодиализ».
Перитониальный диализ является одним из способов детоксикации. Он известен также под названием перитониальный лаваж, или брюшинный диализ.
Перитониальный диализ основан на введении в брюшную полость специального раствора, в который из кровипутем диализа переходят токсические вещества. При использовании метода перитониального диализа рольполупроницаемой мембраны выполняет брюшина, имеющая большую поверхность (около 20 000 см 2 ). Через брюшину из крови легко диффундируют токсические вещества во введенный в брюшную полость раствор. Переход токсических веществ из крови через брюшину в этот раствор объясняется разностью концентрацийэтих веществ по обе стороны брюшины. Известно, что в процессе диализа вещество переходит черезполупроницаемую мембрану из среды с большей концентрацией в среду с меньшей концентрацией. Поскольку раствор, введенный в брюшную полость, не содержит токсического вещества, оно проникает изкрови через брюшину в указанный раствор.
В качестве раствора, вводимого в брюшную полость, при перитониальном диализе применяют смесьрастворов хлоридов калия, натрия, кальция, магния, глюкозы в определенных соотношениях. Однако в зависимости от природы токсических веществ, которые должны удаляться из организма, состав вводимого в брюшную полость раствора может изменяться. При отравлениях барбитуратами и другими веществамислабокислого характера этот раствор доводят до рН = 7,5...8,4, а при отравлениях токсическими веществами, принадлежащими к числу слабых оснований — до рН = 7,1...7,25. Для доведения вводимого раствора до необходимого рН прибавляют раствор гидрокарбо-ната натрия. В ряде случаев к вводимому растворуприбавляют альбумин, который связывает некоторые токсические вещества и способствует переходу их изкрови в брюшную полость. Раствор, в который путем диализа перешло ядовитое вещество, из брюшной полости выводится с помощью специального катетера.
Гемосорбция (гемоперфузия) является одним из способов искусственной детоксикации организма. Этот метод основан на поглощении сорбентами ядовитых веществ, находящихся в крови. При гемосорбции в качестве сорбентов в основном применяются активированный уголь и ионообменники (иониты). Гемосорбцию проводят с помощью прибора (детоксикатора), снабженного насосом для перекачивания крови и набором колонок (капсул), содержащих указанные выше сорбенты. Этот аппарат с помощью специального приспособления подключают к кровотоку больного. Кровь, проходящая через сорбенты, освобождается от токсических веществ, которые поглощаются этими сорбентами.
Применение активированных углей и ионообменников, как сорбентов при гемосорбции, в ряде случаев приводит к некоторым нежелательным явлениям (уменьшению количества тромбоцитов, снижению артериального давления и т. д.). Эти нежелательные явления можно предотвратить путем нанесения белковых покрытий на гранулы сорбентов. Для этой цели рекомендован альбумин. За рубежом ряд фирм для гемосорбции выпускает гранулы активированного угля, покрытые очень тонкой пленкой акрилового гидрогеля.
Гемосорбция применяется для выведения из организма ядов, находящихся в крови, а не в клетках, и рекомендуется при отравлении барбитуратами, салицилатами, глютетимидом, гликозидами наперстянки, производными фенотиазина, ядовитыми грибами и др.
Обменное переливание крови. Этот метод детоксикации организма основан на кровопускании и замещении удаленной крови больного одногруппной кровью донора. Для детоксикации организма также применяется метод замещения плазмы крови больного плазмой доноров или плазмозаменителями.
Детоксикация организма с помощью антидотов (противо ядий). Детоксикацию организма с помощьюантидотов вначале производили в основном для обезвреживания токсических веществ, находящихся в желудке. Затем антидоты нашли применение и для инактивирования токсических веществ в крови, паренхиматозных органах и т. д.
Применение антидотов является эффективным способом детоксикации только на ранней стадии острыхотравлений. Продолжительность этой стадии зависит от свойств токсического вещества. Для быстро метаболизирующихся соединений (синильная кислота, ее соли и другие токсические вещества) стадия острогоотравления непродолжительна, а для тяжелых металлов она достигает 8—12 сут. При отравлениисоединениями тяжелых металлов антидоты могут применяться и на более поздних стадиях интоксикации. Они постепенно связывают катионы тяжелых металлов, ранее поступивших в организм и образовавших комплексы с сульфгидрильными группами ферментов и других белковых веществ.
Некоторые антидоты являются специфичными по отношению к определенному яду. Поэтому для рационального применения антидотов необходимо знать, каким веществом вызвано отравление. При неправильном выборе антидота и введении его в организм в большой дозе может наступать отравлениесамим антидотом. Поэтому данные клинико-лабораторного (в том числе и химико-токсикологического) исследования яда, находящегося в организме, имеют большое значение для правильного выбора и применения соответствующего антидота.
В качестве антидота часто используют активированный уголь, действие которого основано на адсорбции ядов в желудке. Благодаря большой удельной поверхности частиц активированного угля он адсорбирует находящиеся в желудке ядовитые вещества и этим препятствует всасыванию их в кровь.
Большую группу антидотов составляют вещества, вступающие ь химическое взаимодействие с ядами. В результате этого происходит инактивация ядов, которые превращаются в безвредные вещества, выделяемые из организма с мочой или калом. В качестве антидотов могут применяться и смеси нескольких веществ, вводимых в организм в определенной последовательности или же одновременно.
Заслуживают внимания антидоты, принадлежащие к группе меркаптосоединений (унитиол, димеркаптоянтарная кислота, пеницилламин и др.). Одним из представителей меркаптосоединений, часто применяемых в качестве антидота, является унитиол (2, 3-димеркаптопропансульфонат натрия). Он содержит две сульфгидрильные группы, способные взаимодействовать с ионами металлов с образованием прочных соединений.
Унитиол можно вводить в организм парентерально и через рот. Этот антидот применяется при отравлениисоединениями мышьяка, тяжелыми металлами. Их токсическое действие на организм объясняется тем, что при поступлении в кровь эти яды взаимодействуют с сульфгидрильными группами ферментных систем и других белков. Таким образом, ионы тяжелых металлов блокируют сульфгидрильные группы ферментов, играющих жизненно важную роль в организме, в результате чего наступает отравление.
Унитиол взаимодействует не только с соединениями мышьяка и ионами тяжелых металлов, находящихся вкрови, но и с уже вступившими во взаимодействие с ферментами и другими белковыми веществами ворганизме. При этом освобождаются ранее связанные с ионами металлов сульфгидрильные группы белков и восстанавливается их функция. Способность унитиола реагировать с ионами тяжелых металлов, связанных с сульфгидрильными группами белков, объясняется тем, что связь унитиола с ионами тяжелых металлов более прочная, чем связь тех же металлов с сульфгидрильными группами белков. Соединения унитиола с ионамитяжелых металлов являются малотоксичными, водорастворимыми, и поэтому легко выделяются из организмас мочой.
Аналогично унитиолу действует и димеркаптоянтарная кислота (так называемый сукцимер). Она содержит две сульфгидрильные группы и применяется в качестве антидота при отравлении соединениями свинца, ртути и др.
Пеницилламин (диметилцистеин) также относится к группе антидотов, содержащих сульфгидрильную группу. Кроме этого в молекуле пеницилламина содержится атом азота и карбоксильная группа. В связи с наличием вмолекуле пеницилламина указанных функциональных групп и атома азота он легко образует прочное соединение с атомами ряда металлов, имеющих токсикологическое значение. ПеницилЛамин используется в качестве антидота при отравлении соединениями свинца и ртути.
К антидотам, содержащим сульфгидрильные группы, относятся цистеин и ацетилцистеин.
Цистеин — это серосодержащая аминокислота, являющаяся эффективным антидотом при отравленииоднозамещенными галоидопроизводными алифатических углеводородов (бромистый метил, йодистый метил,хлористый этил и др.). Эти галоидопро-изводные углеводородов с цистеином образуют конъюгаты, в составе которых и выделяются из организма с мочой. С увеличением количества атомов галоида в молекулахгалоидопроизвод-ных углеводородов эффективность действия цистеина как антидота уменьшается. Эффективным антидотом при отравлении дигалоидопроизводными алифатических углеводородов являетсяацетилцистеин.
В качестве антидотов широко используются некоторые вещества, образующие с ионами металловвнутрикомплексные соединения (хелаты). Чтобы такой антидот мог проникнуть в клетки и быстро выводиться из организма, его молекула должна содержать определенное количество атомов водорода, способных ионизироваться или образовывать водородные связи. Такие атомы водорода содержатся в некоторыхфункциональных группах (—ОН, —СООН, —SH, —NH 2 ) хелатообразующих антидотов. Причем после связывания ионов металлов с антидотами в них должен оставаться хотя бы один атом водорода, способный ионизироваться или образовывать водородные связи.
Указанным выше требованиям, предъявляемым к антидотам, которые с ионами металлов образуют хелаты, отвечают комплексоны (производные этилендиаминтетрауксусной кислоты, ЭДТА). Некоторые комплексоны сионами металлов образуют прочные хелаты, которые относительно быстро выводятся из организма. К такимкомплексонам относятся тетацин-кальций (кальцийди-натриевая соль этилендиаминтетрауксусной кислоты) и пен- тацин.
Тетацин-кальций хорошо растворим в воде, изотоническом растворе хлорида натрия и в растворе глюкозы. Его вводят в организм внутривенно (капельно) или назначают внутрь в виде таблеток.
Известны и другие антидоты, не относящиеся к меркапто-соединениям или веществам, образующим хелаты. Отдельную группу веществ, применяемых в медицине при отравлениях, составляют так называемые физиологические или функциональные антидоты. Они упреждают или устраняют вредное действие ядов наорганизм. При отравлении синильной кислотой и ее солями в качестве антидота последовательно применяютнитриты, тиосульфат натрия и глюкозу.
При отравлении грибами — мухоморами, содержащими мускарин, ацетилхолином, пилокарпином,ареколином, физостигмином, прозерином, галантамином, фосфорсодержащими органическими соединениями(пестицидами), в качестве антидота применяют атропин и другие холиноблокаторы. При тех же отравленияхменее выраженное действие оказывают скополамин, платифиллин,тропацин и др.
Бемегрид применяется в качестве антидота при острых отравлениях препаратами снотворного действия. Приотравлении морфином и промедолом в качестве антидота применяется гидрохлорид налорфина. Приотравлении соединениями марганца в качестве антидота назначают L-дофу.
СОДЕРЖАНИЕ
АНТИДОТЫ (от греч. antidoton, букв. - даваемое против) (противоядия), препараты, применяемые для профилактики и лечения поражений токсичными в-вами. По характеру действия различают след. типы антидотов.
1) Взаимодействующие с токсичными в-вами с образованием нетоксичных продуктов; напр., глюкоза и Na2S2O3реагируют с цианидами, давая соотв. нетоксичные цианги-дрины и роданиды.
2) Конкурирующие с токсичными в-вами за биомишени (гл. обр. ферменты и рецепторы). Так, галантамин (см.Амариллисовые алкалоиды)и др. обратимые ингибиторы холинэстераз защищают эти ферменты от взаимод. с фосфорорг. ОВ (ФОВ) и пестицидами.
3) Реактивирующие активные центры ферментов, угнетенных токсичными в-вами. Так, иодметилат пиридин-2-альдоксима (ф-ла 1)-реактиватор холинэстераз, ингибированных ФОВ, унитиол HSCH2CH2(SH)CH2SO3Na и 2,3-димеркаптопропанол - реактиваторы пируватоксидазы, ингибированной люизитом или др. соед. As, а также лек. ср-ва при отравлении солями тяжелых металлов, к-рые в организме взаимод. с HS-группами ферментов. При поражениях синильной к-той или ее солями применяют "амилнитрит" (CH3)2CHCH2CH2ONO, при действии к-рого в организме из гемоглобина крови образуется метгемоглобин, являющийся реактиваторомцитохромоксидазы клеток, ингибиро-ванных циан-ионами.
4) Основанные на принципах фармакологич. антагонизма, т.е. вызывающие симптомы, противоположные тем, к-рые наблюдаются при действии токсичного в-ва. К таким антидотам относятся холинолитические средства-атропин и др. Подобные в-ва взаимод. с холинорецепторами и предотвращают их перевозбуждение под действием высоких концентраций ацетилхолина, избыток к-рого в холинергич. синапсах образуется при угнетении холинэстераз ФОВ и др. антихолинэстеразными соединениями.
К этому же типу
антидотов относятся нек-рые противосудорожные
средства и транквилизаторы,
действующие на тормозные синапсы,
в к-рых медиатором является![]() аминомасляная
к-та, - барбитураты (фенобарбитал и
др.) и бенздиазепины, напр. диазепам (II).
аминомасляная
к-та, - барбитураты (фенобарбитал и
др.) и бенздиазепины, напр. диазепам (II).
5) Способствующие выведению токсичных соед. из организма, гл. образом комплексоны-тетацинкальций (кальцийдинатриевая соль этилендиаминтетраацетата), трилон Б (III) и др. Эти соед. с катионами тяжелыхметаллов и нек-рыми РЗЭ образуют устойчивые комплексы, к-рые хорошо раств. в воде и относительно быстро выводятся из организма. Применяются также при поражениях радиоактивными изотопами.
Нек-рые антидоты
обладают смешанным действием. Так,
бисаммониевые соед. ф-лы IV (п = 3-5) -
реактиваторы ингибированных холинэстераз
и, кроме того, обладают противосудорожным
действием (как н-холинолитики).
Эффективность антидотов может быть
повышена при совместном применении
соед. разл. типов. Обычно антидоты
используются в виде водных р-ров для
подкожного или внутримышечного введения
(при оказании первой медицинской помощи
- с использованием шприц-тюбиков или
авто-инъекторов). Профилактич. ср-ва,
как правило, используют в виде таблеток.

Некоторые антидоты
В качестве противоядий используют те или иные вещества или смеси, в зависимости от характера яда (токсина):
этанол может быть использован при отравлении метиловым спиртом
атропин — используют при отравлении M-холиномиметиками (мускарин и ингибиторами ацетилхолинэстеразы(фосфорорганические яды).
глюкоза — вспомогательный антидот при многих видах отравлений, вводится внутривенно или перорально. Способна связыватьсинильную кислоту.
налоксон — используют при отравлении и передозировке опиоидами
[править]Антидоты, наиболее часто используемые при острых отравлениях
Унитиол — низкомолекулярный донатор SH-групп, универсальный антидот. Обладает широким терапевтическим действием, малотоксичен. Применяется как антидот при острых отравлениях люизитом, солями тяжелых металлов (ртуть, медь, свинец), припередозировке сердечных гликозидов, отравлении хлорированными углеводородами.
ЭДТА-тетацин-кальций, Купренил — относится к комплексонам (хелатообразователям). Образует легко растворимые низкомолекулярные комплексы с металлами, которые быстро выводятся из организма через почки. Применяется при острых отравлениях тяжелыми металлами (свинец, медь).
ОКСИМЫ (аллоксим, дипироксим) — реактиваторы холинэстераз. Используются при отравлениях антихолинэстеразными ядами, такими как ФОВ. Наиболее эффективны в первые 24 часа.
Атропина сульфат — антагонист ацетилхолина. Применяется при острых отравлениях ФОВ, когда в избытке накапливается ацетилхолин. При передозировке пилокарпина, прозерина, гликозидов, клофелина, бета-блокаторов; а также при отравлении ядами, вызывающими брадикардию и бронхорею.
Этиловый спирт — антидот при отравлении метиловым спиртом, этиленгликолем.
Витамин В6 — антидот при отравлении противотуберкулезными препаратами (изониазид, фтивазид); гидразином.
Ацетилцистеин — антидот при отравлении дихлорэтаном. Ускоряет дехлорирование дихлорэтана, обезвреживает его токсичныеметаболиты. Применяется также при отравлении парацетамолом.
Налорфин — антидот при отравлении морфином, омнопоном, бенздиазепинами.
Цитохром-С — эффективен при отравлении окисью углерода.
Липоевая кислота — применяется при отравлении бледной поганкой как антидот аманитина.
Протаминсульфат — антагонист гепарина.
Аскорбиновая кислота — антидот при отравлении перманганатом калия. Используется для детоксикационной неспецифической терапии при всех видах отравлений.
Тиосульфат натрия — антидот при отравлении солями тяжелых металлов и цианидами.
Противозмеиная сыворотка — используется при укусах змей.
СИНИЛЬНАЯ КИСЛОТА
Синильная кислота – бесцветная жидкость с температурой кипения 26,5°С. Удельный вес при температуре 20°С – 0,69. Смешивается во всех отношениях с водой, спиртом, диэтиловым эфиром. Легко воспламеняется и горит голубоватым пламенем. Чрезвычайно слабая кислота, ее соли легко гидролизуются. Перегоняется с водяным паром в первые порции дистиллята. Граница отгонки 1 мг из 100 г биологического материала.
Токсикологическое значение и метаболизм. Ядовитость синильной кислоты обусловлена присутствием в HCN изоцианистой кислоты, одной из таутомерных форм HCN:
![]()
Токсикологическое значение синильной кислоты и ее производных определяется ядовитостью их, с одной стороны, и сравнительно широким применением – с другой. Цианиды калия и натрия применяются в металлургии для извлечения благородных металлов из руд и в ювелирном деле, благодаря их способности образовывать легко растворимые комплексы с благородными металлами, их которых благородные металлы затем легко вытесняются цинком. Кроме того, различные производные синильной кислоты применятся в качестве компонентов при производстве фармпрепаратов, средств дезинсекции и дезинфекции, при цианидировании сталей и т.д.
Источниками отравления, особенно детей,
нередко становятся ядра горького
миндаля, абрикоса вишни, лавровишни и
др. растений семейства Rosaceae,
содержащие гликозид амигдалин
 ,
который способен в кислом растворе, а
под влиянием энзима эмульсина даже в
нейтральной среде, расщепляться на
виноградный сахар, бензойный альдегид
и синильную кислоту. Известны отравления
также спиртовыми настойками, приготовленными
на плодах косточковых растений сем.
Rosaceae. Иногда источником
отравления был и фасеолюнатин – гликозид
индийскихбобов (Phaseolus
lunatus)
,
который способен в кислом растворе, а
под влиянием энзима эмульсина даже в
нейтральной среде, расщепляться на
виноградный сахар, бензойный альдегид
и синильную кислоту. Известны отравления
также спиртовыми настойками, приготовленными
на плодах косточковых растений сем.
Rosaceae. Иногда источником
отравления был и фасеолюнатин – гликозид
индийскихбобов (Phaseolus
lunatus)
![]() дающий
при гидролизе HCN и ацетон,
а также линамарин – гликозид семян
льна, имеющий близкое строение и
являющийся причиной отравления скота
при поедании льняного жмыха. Описаны
случаи отравления животных манником
водяным, содержащим гликозид, отщепляющий
HCN.
дающий
при гидролизе HCN и ацетон,
а также линамарин – гликозид семян
льна, имеющий близкое строение и
являющийся причиной отравления скота
при поедании льняного жмыха. Описаны
случаи отравления животных манником
водяным, содержащим гликозид, отщепляющий
HCN.
Токсикологическое значение имеет также дициан [(CN)2], хлор- и бромцианы (ClCN, BrCN), которые могут вызывать отравления в производственных условиях.
Имеются сведения об образовании синильной кислоты при горении целлулоида. Следы HCN содержатся также в табачном дыме.
Есть сообщения о нормальном содержании цианидов в организме человека: ~6,7 мкг% в моче некурящих людей и 17,4 мкг% в моче курящих. Повышение нормального содержания цианидов отмечается у лиц, страдающих рассеянным склерозом. В крови цианиды могут образовываться и посмертно.
Смертельной дозой чистой синильной кислоты считают 0,05 — 0,1 г; смертельная доза цианида калия 0,15—0,25 г. Описаны случаи выздоровления после приема 0,3 мг и даже 3,25 г KCN. Отравление ядрами горького миндаля может наступить при поедании 40—60 штук, а у детей — даже 10—12 шт.
Горькоминдальная вода (Aqua Amygdalarum amararum) может оказать токсическое и даже смертельное действие при приеме внутрь 60—100 мл. Одним из наводящих указаний при вскрытии трупов лиц, погибших от отравления синильной кислотой, является запах горького миндаля (но далеко не всегда) от внутренних органов трупа и мозга (отмечено, что при отравлениях препаратами синильной кислоты она иногда обнаруживается в желудке с содержимым, а в паренхиматозных органах при этом результаты анализа бывают негативными).
В организме в тканях трупа, во внешней среде цианиды подвергаются биотрансформации несколькими путями.
1. Гидролиз

2. Превращение в роданиды под влиянием фермента роданазы: KCN→KSCN (составная часть организма).
Соединение с гемоглобином крови.
Связывание с цистеином.
Присоединение к веществам, содержащим альдегидную группу, например к сахарам:
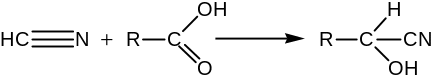
В судебной практике известны случаи, когда препарат цианида калия, доставленный на анализ как орудие замышляемого отравления, при исследовании оказывался карбонатом калия: имело место (или могло иметь место) покушение на отравление с негодными средствами. При этом цианид калия, сохраняемый без особых предосторожностей (в отношении внешних воздействий), подвергался действию влаги воздуха и углекислоты и превращался в неядовитый карбонат калия:
KCN + СО2 + НОН = КНСО3 + HCN
Возможность превращения синильной кислоты и ее производных в другие вещества связана с необходимостью проведения химико-токсикологического исследования на наличие HCN в день поступления объектов в лабораторию.
Качественное обнаружение.
В химико-токсикологическом анализе может иметь значение только реакция образования берлинской лазури.
NaOH + HCN = NaCN + Н2О;
FeSO4 + 2NaCN = Fe(CN)2 + Na2SO4;
Fe(CN)2 + 4NaCN = Na4[Fe(CN)6];
3Na4[Fe(CN)6] + 2Fe2(SO4)3 = Fe4[Fe(CN)6]3 + 6Na2SO4
Реакция проводится со всем объемом первого дистиллята. Признаком наличия CN- в дистилляте служит появление синего осадка или синего окрашивания. При образовании значительного синего осадка берлинской лазури реакцию необходимо повторить с добавлением растворов FeSO4 и FeCl3 перед подкислением соляной кислотой.
Заключение о качественном обнаружении (если синий осадок не выпадает тотчас) или необнаружении синильной кислоты дается лишь по истечении 24—48 часов, так как при следах синильной кислоты в присутствии органических веществ осадок берлинской лазури может выпадать медленно.
Чувствительность реакции 20 мкг HCN в 1 мл раствора. Открываемый минимум 20 мкг при предельном разбавлении 1: 100 000. При содержании 20—30 мкг HCN в пробе образуется соответственно зеленое или голубое окрашивание раствора, а при количествах, больших 30 мкг, выделяется характерный синий осадок берлинской лазури.
Выделившийся осадок берлинской лазури может быть представлен в качестве доказательства обоснованности заключения об обнаружении синильной кислоты.
Достаточно высокая чувствительность реакции, ее специфичность и возможность сохранения осадка ферриферроцианида (берлинской лазури) для представления судебно-следственным органам делают ее особенно ценной для судебно-химических исследований.
Количественное обнаружение синильной кислоты. При исследовании свежего трупного материала, содержащего сравнительно небольшие количества синильной кислоты (о количестве ее дает возможность судить качественная проба), а также при других объектах исследования (нетрупный материал) применяют объемное определение. Метод основан на взаимодействии HCN с 0,1н (или 0,01н при малых количествах HCN) раствором AgNO3. Непрореагировавший нитрат серебра оттитровывают 0,1н (или 0,01н) раствором роданида аммония или калия при индикаторе железоаммонийные квасцы.
При не вполне свежем трупном материале такой способ количественного определения неприменим, так как сероводород, содержащийся в объекте исследования, будет реагировать с нитратом серебра, образуя сульфид серебра, искажая результаты количественного определения. В таких случаях обычно применяют весовой метод определения CN.
Весовое определение синильной кислоты сводится к отгонке синильной кислоты из новой навески объекта исследования, собиранию дистиллятов в 2—3 приемника, содержащие 0,2% раствор нитрата серебра, отделению после подкисления азотной кислотой (не содержащей CN) осадка AgCN с возможной примесью Ag2S, обработке полученного осадка избытком раствора аммиака в целях отделения растворимого в нем цианида серебра от нерастворимого сульфида серебра, выделению из раствора с помощью азотной кислоты цианида серебра и определению металлического серебра после высушивания, сжигания и прокаливания фильтра с осадком.
ЯДОВИТЫЕ ГАЛОГЕНОПРОИЗВОДНЫЕ
Хлороформ и хлоралгидрат
Хлороформ (трихлорметан) — бесцветная, прозрачная, подвижная и легколетучая жидкость, обладающая характерным запахом и жгучим вкусом. Температура кипения 59,5—62°. Удельный вес 1,498 при температуре 15°. Растворяется в воде в соотношении 1:200. Со спиртом, эфиром, бензином смешивается во всех отношениях.
Хлоралгидрат (1,1-диокси-2,2,2-трихлорэтан)•—бесцветные кристаллы с острым запахом, слегка горьковатого царапающего вкуса. Легко растворяется в воде, спирте, эфире, хлороформе. На воздухе расплывается и медленно улетучивается. Температура плавления 49—53°.
Хлороформ и хлоралгидрат перегоняются (особенно при малых количествах их в объектах исследования) в первые порции дистиллята. При количестве более 1 г в дистилляте (редко встречается в практике химико-токоикологического анализа) удается наблюдать наличие капель хлороформа и ощущать его характерный запах. При больших количествах хлоралгидрата (что также встречается редко) прибавление едкой щелочи и очень слабое нагревание приводят к появлению запаха хлороформа, а иногда даже капель хлороформа:
Количество веществ, которое может быть изолировано с водяным паром из 100 г биологического материала животного происхождения, составляет не менее 0,2 г хлороформа и 0,05 г хлоралгидрата.
Токсикологическое значение и метаболизм. Хлороформ является хорошим растворителем эфиров, лаков, некоторых алкалоидов. Поэтому он имеет большое промышленное значение. Как вещество, способное вызывать наркоз, хлороформ применяется в медицине. Хлоралгидрат используется в медицине в качестве быстродействующего снотворного средства.
Хлороформ и хлоралгидрат являются наркотиками, вначале возбуждают, а затем парализуют центральную нервную систему.
Смерть от хлороформа при наркозе объясняется не только токсичностью хлороформа, но и рядом других причин. При типичной интоксикации она наступает от паралича дыхания. Химико-токсикологическое исследование внутренних органов трупов лиц, погибших от отравления хлороформом при наркозе, в подавляющем большинстве случаев приводит к обнаружению его в органах. При введении хлороформа через желудок уже 5—10 г вызывают тяжелые признаки отравления: боли, рвоту и явления общего отравления. Смертельной дозой хлороформа считают 50—70 г.
Хлоралгидрат по общему действию на организм напоминает хлороформ. Сильнее выражено его действие на сердечно-сосудистую систему. При остром отравлении смерть нередко наступает от паралича сердца. Смертельная доза, по данным Н. В. Попова и О. И. Глазовой, составляет около 10 г, при заболеваниях сердца опасны дозы менее 10 г. Секционная картина в большинстве случаев нехарактерна. Иногда от мозга, и внутренних органов трупа ощущается запах хлороформа, что дает наводящие указания для правильного направления хода исследования.
О сохраняемости хлороформа в трупе имеются противоречивые мнения. Одни авторы отмечают, что хлороформ быстро выводится из организма и исчезает из трупа благодаря летучести (И. Гадамер), другие указывают на сравнительно продолжительное сохранение его в трупе. Конечными продуктами метаболизма хлороформа являются НС1 и СО2.
Основные метаболиты хлоралгидрата в организме человека следующие: СС13-СН2ОН — трихлорэтанол, возможно СС13-СООН (частично) трихлоруксусная кислота и глюкуронид трихлорэтанола СС13-СH2-С6Н9O6. Все метаболиты выделяются с мочой.
Качественное обнаружение (см. методичку к лаборатрным занятиям).
Количественное определение. Количественное определение галогенопроизводных основано на отщеплении при нагревании со спиртовым раствором едкого натра органически связанного хлора и аргентометрическом определении хлорид-иона.
Четыреххлористый углерод
Четыреххлористый углерод представляет собой прозрачную, подвижную, тяжелую жидкость с удельным весом 1,594—1,600 и запахом, напоминающим запах хлороформа. Почти не растворяется в воде (растворимость 0,077 г/мл при температуре 25°), хорошо смешивается с безводным спиртом, эфиром, бензолом, бензином. Температура кипения 75,5—77,5°, [α]20D = 1,462—1,464.
Дистиллят при содержании CCl4 в объекте исследования в количестве большем, чем 1—1,2 г, обладает своеобразным запахом. Иногда в нем наблюдается наличие капель CCl4. При меньших количествах CCl4 перегоняется с водяным паром в первые порции дистиллята (5 мл). Количества CCl4, которые могут быть изолированы дистилляцией с водяным паром из 100 г биологического материала животного происхождения, составляют около 1 г.
Токсикологическое значение и метаболизм. Четыреххлористый углерод широко используется как хороший растворитель жиров, лаков, смол, восков, каучука и т. п., а также для удаления жировых пятен и в качестве консервирующего вещества для меховых изделий. Преимущество его как органического растворителя заключается в том, что он не воспламеняется.
В ветеринарной практике четыреххлористый углерод применяется в качестве противоглистного средства. В результате всасывания его из кишечника, особенно в присутствии жиров, при неосторожном применении его имели место отравления.
Четыреххлористый углерод применяется и как средство для гашения пожаров, особенно для тушения горящей нефти, бензина и т. п.: тяжелые пары его изолируют горящее вещество от кислорода воздуха. Однако при этом возможно отравление фосгеном — продуктом разложения четыреххлористого углерода.
Четыреххлористый углерод ядовит при вдыхании и при приеме внутрь. При вдыхании он вызывает наркоз медленнее, чем хлороформ; действие его на организм напоминает действие хлороформа, но изменения в органах (печень, почки, сердце) более глубоки (жировое перерождение). По вопросу о смертельной дозе CCl4 при приеме внутрь сведения разноречивы. Указывают дозы 29—50 мл и больше.
В литературе приводятся случаи отравления CCl4 как производственного характера, так и связанные с применением его в медицине и ветеринарии. Метаболизм четыреххлористого углерода полностью не изучен, хотя известно, что одним из метаболитов является СНС13 (хлороформ).
Качественное обнаружение. 1. Отщепление хлора и последующее доказательство наличия хлорид-иона реакцией взаимодействия с AgNO3 в азотнокислой среде.
Реакция образования изонитрила.
Получение розового окрашивания с резорцином в щелочной среде.
В отличие от хлороформа и хлоралгидрата четыреххлористый углерод не обладает восстановительной способностью, так как при кипячении его с едким натром не образуются вещества, обладающие восстановительным свойством.
Учитывая низкую чувствительность этой реакции в отношении хлороформа и хлоралгидрата, исключать CCl4 при положительных результатах других реакций следует с осторожностью. Нужно также учитывать неспецифичность реакции: кроме хлороформа и хлоралгидрата, способностью восстанавливать Сu(ОН)2 обладают многие альдегиды. Поэтому химико-токсикологическое значение описанные реакции приобретают только в их совокупности
Количественное определение основано на том же принципе, что и определение хлороформа и хлоралгидрата.
1,2-дихлорэтан (хлористый этилен) и трихлорэтилен
Дихлорэтан представляет собой тяжелую, бесцветную, подвижную жидкость с запахом, напоминающим запах хлороформа. Температура кипения — 83,7°, удельный вес 1,25 при температуре 20°. Растворимость его 0,922 г в 100 мл воды при 0°, 0,855 г при 10°, 0,869 г при 20°, 0,894 г при 30°. Хорошо растворяется в спирте и других органических растворителях. Весьма стоек к действию кислот и щелочей. Воспламеняется с трудом. Технический препарат всегда содержит примесь трихлорэтилена.
Трихлорэтилен — бесцветная жидкость с запахом, напоминающим запах хлороформа. Температура кипения 86,9°. При окислении трихлорэтилена образуется фосген.
Из биологического материала дихлорэтан изолируют дистилляцией с водяным паром. При наличии в объекте исследования более 1 г хлористого этилена в дистилляте можно наблюдать капли вещества. При малых количествах дихлорэтан перегоняется главным образом с первыми порциями дистиллята. Перегоняется с водяным паром и трихлорэтилен.
При специальных исследованиях на наличие дихлорэтана целесообразно собирать дистиллят в количестве 300 мл, затем подвергать его перегонке из колбы Вюрца, собирая первые 200 мл дистиллята. Второй дистиллят нужно дважды дефлегмировать, собирая сначала 50 мл, а затем при четвертой перегонке 10 мл. С последним дефлегматом производят качественные реакции.
Токсикологическое значение и метаболизм. Дихлорэтан имеет большое применение в промышленности. Являясь прекрасным растворителем жиров, смол, масел, восков и парафинов, он используется в разнообразных экстракционных процессах, для обработки кожи перед дублением, для извлечения жира из шерсти, изолирования алкалоидов из растительного сырья, химической чистки и т.д. Дихлорэтан — исходный продукт для синтеза различных веществ (двухатомных спиртов и их эфиров, аминов, непредельных соединений, например хлористого винила, и др.). Используется также как антисептик и как инсектофунгицид в пушном хозяйстве при токсокарозе и уницинариозе серебристо-черных лисиц.
Трихлорэтилен также широко применяется в качестве растворителя, консерванта яиц, средства борьбы с паразитами и для других целей.
Дихлорэтан относится к наркотикам, занимающим по силе действия едва ли не первое место среди галогенопроизводных. Как вещество, ядовитое при вдыхании и приеме внутрь и имеющее широкое применение, неоднократно приводило к необходимости производства судебно-химического исследования «неизвестных жидкостей», выпитых вместо водки, ликера, пива, к которому «для крепости» был добавлен (по незнанию его токсичности) дихлорэтан, а также к анализу внутренних органов трупов людей. Отравления, даже со смертельным исходом, имели место также при вдыхании паров дихлорэтана на производстве и в быту, например при чистке одежды в тесном и плохо проветриваемом помещении. В предупреждении промышленных отравлении большую роль сыграл порядок, требующий сообщать органам санитарного надзора о каждом заказе, например, на лак, содержащий хлористый этилен, с указанием количества лака, его рецептуры, назначения, места применения, что позволяет своевременно требовать принятия соответствующих мер. Судебно-химические исследования на наличие трихлорэтилена были связаны главным образом с применением этого вещества в ветеринарной практике в качестве противоглистного средства.
Картина отравления дихлорэтаном напоминает отравление четыреххлористым углеродом. При введении токсической дозы через рот наблюдаются рвота, понос, увеличение и болезненность печени, резкое вздутие живота, анурия, приступы уремии и смерть. Основное его действие проявляется на центральную нервную систему и кроветворный аппарат. Смертельной дозой дихлорэтана при приеме внутрь считается 15—50 мл. Судебно-медицинское исследование трупа не дает характерных признаков, за исключением асфиксии и запаха от полостей трупа (при остром отравлении), напоминающего запах хлороформа.
Трихлорэтилен является наркотиком, поражает нервную систему и вызывает заболевания печени и почек.
В организме трихлорэтилен подвергается превращениям с образованием трихлоруксусной кислоты (СС13СООН) и трихлор-этанола (СС13-СН2ОН). Последний конъюгирует с глюкуроновой кислотой.
Качественное обнаружение (см. методичку к лабораторным занятиям)
Количественное определение. Количественное определение возможно по отщепленному с помощью металлического натрия в присутствии этилового спирта хлору. Определяется около 50% хлора от теоретически вычисленного.

