Билет № 23
1)Биотрансформация — метаболическое превращение эндогенных и экзогенных химических веществ в более полярные (гидрофильные) соединения.
Фазы биотрансформации

Реакции 1-й фазы Реакции 2-й фазы(реакции синтеза)
гидролиз, -глюкуронирование,
восстановление, -сульфатирование,
окисление. -ацетилирование,
-метилирование,
конъюгация(соединение) с:
а) глутатионом (синтез меркаптуровой кислоты) б) аминокислотами (глицином,таурином и глутаминовой кислотой).
Основные пути биотрансформации чужеродных соединений.
1. Окисление:
а) микросомальное
– алифатичекое или ароматическое гидроксилирование,
– эпоксидирование,
– N-гидроксилирование,
– N, S-окисление,
– дезалкилирование,
– дезаминирование,
– десульфирование;
б) немикросомальное
– окислительное дезаминирование,
– окисление спиртов, альдегидов,
– ароматизация алициклических соединений.
2. Восстановление:
а) восстановление нитросоединений, азотсоединений микросомальными ферментами;
б) микросомальное восстановительное галогенирование;
в) немикросомальное восстановление.
3. Гидролиз с участием микросомальных и немикросомальных ферментов.
4. Синтез (реакции коньюгирования):
а) образование коньюгатов с глюкуроновой кислотой;
б) образование сложных эфиров с серной и фосфорной кислотами;
в) метилирование;
г) ацетилирование;
д) пептидная коньюгация.
Классическим примером биотрансформации ксенобиотиков является метаболизм бензола в организме

Рис. Метаболизм бензола
В ходе l фазы метаболизма обеспечивается превращение жирорастворимого субстрата в полярный продукт путем включения в молекулу гидроксильной группы. В ходе ll фазы образовавшийся фенол взаимодействует с эндогенным сульфатом, в результате полярность образующегося продукта еще более возрастает. Фенилсульфат прекрасно растворяется в воде и легко выделяется из организма.
Далеко не всегда преобразования молекулы представляет собой простое чередование 1 и 11 фаз метаболизма. Возможна и более сложная последовательность реакций биопревращений.
Ферменты 1-й фазы биотрансформации ксенобиотиков
l фаза метаболизма в широком смысле может быть определена, как этап биотрансформации, в ходе которого к молекуле соединения либо присоединяются полярные функциональные группы, либо осуществляется экспрессия таких групп, находящихся в субстрате в скрытой форме
Разнообразие чужеродных химических веществ, способных подвергаться в организме метаболическим превращениям, является следствием многообразия энзимов, участвующих в l фазе биотрансформации и их низкой субстратной специфичности. Многие из энзимов существуют в нескольких формах (изоферменты), различающихся по своим физико-химическим свойствам (молекулярная масса, электрофоретическая подвижность, абсорбцией света с разними длинами волн), отношению к индукторам и ингибиторам (см. ниже) и активностью в отношении субстратов различного строения.
Энзимы l фазы, участвующие в процессе биотрансформации ксенобиотиков, можно классифицировать в соответствии с типом активируемой ими реакции:
1. Оксидазы смешанной функции: цитохромР-450 (Р-450) и флавинсодержащие монооксигеназы (ФМО);
2. Простогландинсинтетазы - гидропероксидазы (ПГС) и другие пероксидазы;
3. Алкогольдегидрогеназы и альдегиддегидрогеназы;
4. Флавопротеинредуктазы;
5. Эпоксидгидролазы;
Эпоксидирование и гидроксилирование ароматических соединений.
Метаболизм полициклических и ароматических углеводородов сопровождается образованием реакционно-способных промежуточных продуктов метаболизма, в частности ареноксидов, способных вызывать некроз клеток и являющихся канцерогенами. Таким образом осуществляется, в частности, превращение бенз(а)пирена (см. выше) или нафталена:
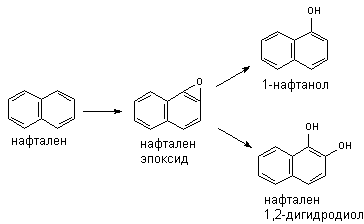
Эпоксид, возникающий в процессе метаболизма, может подвергаться неэнзиматическому гидролизу с образованием нафтанола, либо, взаимодействуя с эпоксидгидролазой, превращаться в дигидродиол, а также образовывать конъюгаты с глутатионом, которые выделяются из организма в виде производных меркаптуровой кислоты.
Эпоксидирование алифатических и алициклических соединений.
Многие алифитические и алициклические соединения, содержащие в молекуле непредельные связи метаболизируют с образованием чрезвычайно стабильных эпоксидов (превращение алдрина в диалдрин). Это же превращение лежит в основе образования канцерогенных продуктов метаболизма афлатоксинов:
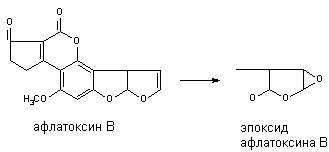
N-окисление.
Превращению могут подвергаться такие вещества, как анилин и его производные, ацетаминофлюорен и др. В результате окисления атома азота могут образовываться гидроксиламины, оксимы и N-оксиды:
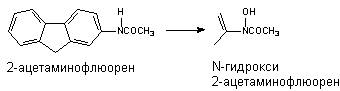
Оксимы образуются в процессе гидроксилирования иминов или первичных аминов:
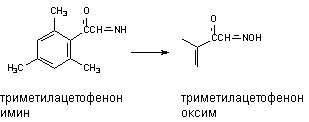
Окисление тиоэфиров.
При участии цитохромаР-450 и других монооксигеназ происходит окисление тиоэфирных связей, в молекулах таких ксенобиотиков как хлорпромазин, альдикарб, метиокарб и др. Этот вид превращения характерен также для метаболизма сернистого иприта:
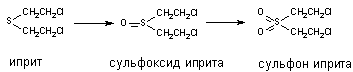
Установлено, что при этом токсичность вещества возрастает (сульфон иприта токсичнее исходного вещества).
Оксилительное деалкилирование.
Классическим примером превращения данного типа является О-деалкилирование р-нитроанизола. Поскольку продукт превращения легко определяется, реакцию нередко используют для оценки активности Р-450:
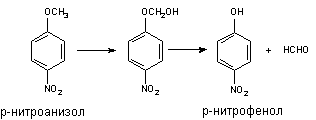
Другим примером может служить метаболизм инсектицида этоксихлора:
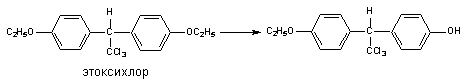
В результате деятельности монооксигеназ возможно и N-деалкилирование ксенобитиков:

Десульфурирование и расщепление эфиров.
Фосфоротиоаты (1) и фосфородитиоаты (2), являющиеся представителями большой группы инсектицидов, приобретают способность угнетать активность ацетилхолинэстеразы (за счет этого реализуется их биологическая активность) в результате ферментативного преобразования соединений:
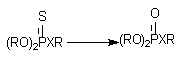
Х = О (1); Х = S (2).
Процесс разрушения эфирных связей при атоме фосфора ФОС также во многом обусловлен действием Р-450, хотя процесс может идти и при участии гидролитических энзимов.
Активация ксенобиотиков цитохромом Р450. Цитохром Р450 человека способен активировать образование проканцерогенов и протоксикантов. Многие химические вещества, напротив, могут снижать свою токсичность в реакциях биотрансформации, катализируемых цитохромом Р450, превращаясь в менее токсичные метаболиты. В некоторых случаях один и тот же фермент катализирует реакции и детоксикации, и активации токсиканта.
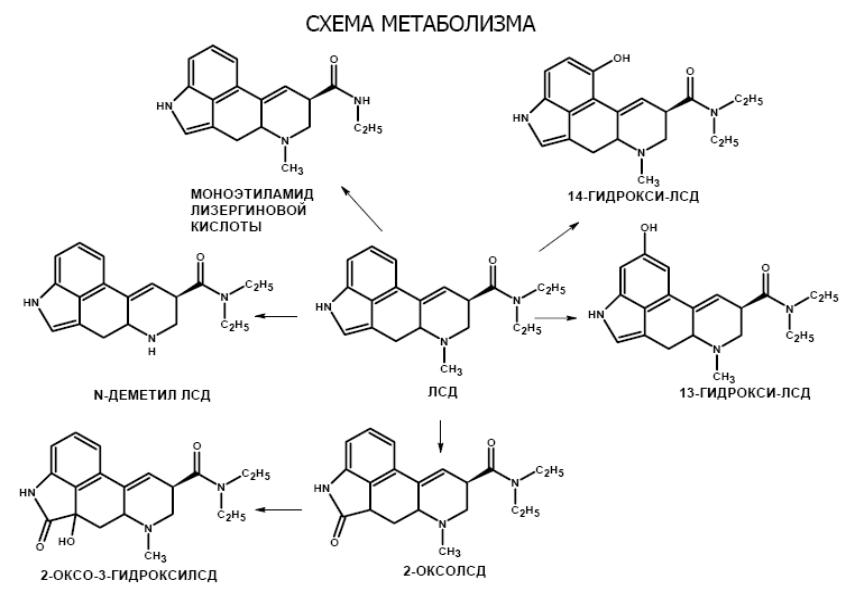
2) ГАЛЛЮЦИНОГЕНЫ
ГАЛЛЮЦИНОГЕНЫ - вещества, вызывающие нарушения в восприятии реального мира, особенно световых сигналов, запаха, вкуса, а также искажения в оценке пространства (направления, расстояния) и времени. Под влиянием галлюциногенов может происходить визуализация цвета и звука, по субъективным отзывам можно "слышать цвет" и "видеть звуки". Большие дозы вызывают визуальные галлюцинации и видения.
Общей чертой галлюциногенов является их способность изменять настроение и характер мышления. Они вызывают состояние возбуждения ЦНС, приводящее к сдвигу сознания, обычно к эйфории, но иногда к сильной депрессии или агрессивному состоянию. Самым опасным следствием применения галлюциногенов является нарушение способности логически рассуждать, что ведет к неадекватным решениям и несчастным случаям. Находящиеся под воздействием галлюциногенов люди должны быть под постоянным наблюдением, чтобы не спровоцировать критическую ситуацию, когда они могут причинить вред себе или окружающим. Острое состояние - беспокойство, возбуждение, бессонница - обычно длится, пока не прекратится действие средства. Иногда депрессия и "деперсонализация" столь велики, что приводят к самоубийству.
В течение долгого времени после выведения из организма могут ощущаться "возвратные вспышки" (flashbacks) - небольшие повторения психоделических эффектов, таких как интенсификация цветового восприятия, наблюдение передвижения фиксированных объектов, путаница в идентификации объектов.
Наиболее известные галлюциногены: ЛСД, мескалин, псилоцибин и псилоцин грибов, фенциклидин (РСР), метоксипроизводные амфетамина.
КЛАССИФИКАЦИЯ ПО СПОСОБУ ВОЗДЕЙСТВИЯ
Серотонергические галлюциногены - ЛСД, МЕСКАЛИН, ПСИЛОЦИБИН/ПСИЛОЦИН. Их эффекты объясняются влиянием на обмен серотонина в мозге.
Диссоциативные анестетики - РСР и его аналоги, в том числе применяемый в медицине анестетик КЕТАМИН, которые действуют преимущественно на глутаминергические рецепторы.
D-ЛИЗЕРГИД(ЛСД;,
ЛСД-25)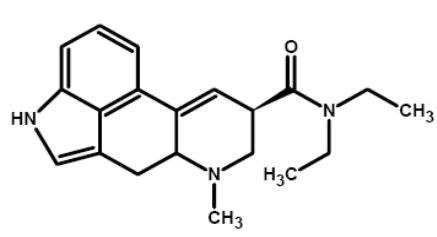
Галлюциноген.
Впервые был синтезирован А.Гофманом в 1938 г в лаборатории фирмы Sandoz. D-изомер ЛСД - один из самых активных галлюциногенов, в то время как L-изомер практически неактивен.
Мало токсичен, имеет индекс безопасности около 1000. Менее активное вещество – амид лизергиновой кислоты, встречается в природе в различных растениях и грибах, например, спорынье.
Обычно применяется перорально в виде тартрата в дозах 25-250 мкг. Легко синтезируется из диэтиламида и ЛИЗЕРГИНОВОЙ КИСЛОТЫ. В качестве прекурсора широко применяется ЭРГОТАМИН, спорынья.
За 48 ч с мочой выводится до 25% принятой дозы. Концентрации неизмененного вещества в моче в течение 24 ч составляют 1-55 мкг/л после приема 200-400 мкг.
Основной побочный эффект ЛСД представляет собой непредсказуемые повторяющиеся галлюцинации спустя недели и месяцы после последнего приема.