
- •Концентрация раствора.
- •Скорость реакции.
- •Элемент Даниэля–Якоби:
- •Измерение эдс цепи:
- •Направление протекания овр:
- •Коррозия под действием блуждающих токов
- •Метод валентных связей
- •1927 Г. – Гейтлер и Лондон Квантово-механический расчет молекулы водорода
- •Механизмы образования связи
- •Механизм образования ковалентной связи.
- •Донорно-акцепторный и дативный механизмы.
- •Экзаменационный билет № 12
- •Энтропия
- •Закон Вант-Гоффа:
- •Экзаменационный билет № 13
- •Периодическое изменение свойств
- •Экзаменационный билет № 14
- •Химическая связь
- •Виды ковалентной связи
- •Экзаменационный билет № 15
- •Гибридизация
- •Экзаменационный билет № 16
- •Отличительные черты катализаторов:
- •Химические источники тока
- •Экзаменационный билет № 17
- •Энтальпия
- •Второй закон Фарадея
- •Экзаменационный билет № 19
- •Химическая термодинамика
- •Свойства системы
- •Коррозия (по механизму)
- •Экзаменационный билет № 20
- •Устойчивость коллоидных систем.
- •Экзаменационный билет № 21
- •Экзаменационный билет № 22
- •Экзаменационный билет № 23
- •Экзаменационный билет № 24
- •Гидролиз солей.
- •Основные свойства
- •Основные виды
- •Коллоидные системы, применяемые в химическом анализе
- •Экзаменационный билет № 25
- •Экзаменационный билет № 26
- •Ионное произведение воды
- •Вывод значения ионного произведения воды
- •Практическое значение ионного произведения воды
- •Ионные произведения других растворителей
- •Водородный показатель
- •Экзаменационный билет № 27
- •Экзаменационный билет № 28
- •Химическое равновесие
- •Принцип Ле Шателье
- •Химические источники тока
- •Экзаменационный билет № 29
- •Феноменология
- •Природа поляризации
- •Экзаменационный билет № 30
- •Основные свойства
- •Электрохимическая коррозия
- •Электрохимическая коррозия.
Коррозия под действием блуждающих токов
"Вход" тока – катодный участок, "выход" тока – анодный участок (корродирует)
Защита:
Дренаж – соединение проводником анодной зоны трубы и катодной зоны рельса
Дополнительный анод, соединенный с катодным участком рельса
Оглавление:
Билет №11
Билет №12
Билет №13
Билет №14
Билет №15.
ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ № 11
Окислительно-восстановительные реакции. Степень окисления элемента. Примеры окислителей и восстановителей.
Метод валентных связей (МВС). Обменный и донорно-акцепторный механизмы образования ковалентной связи.
Ответ:
ОВР
Окислительно-восстановительные реакции (ОВР) – реакции, которые идут с изменением с.о. атомов. Окисли́тельно-восстанови́тельные реа́кции — это химические реакции, протекающие с изменением степеней окисления атомов, входящих в состав реагирующих веществ, реализующихся путём перераспределения электронов между атомом-окислителем и атомом-восстановителем.
Степень окисления (с.о.) – заряд, который приписывается атому, считая его ионом
Окислитель (Ox) – принимает электроны.
Восстановитель (Red) – отдает электроны
Ox1
+ Red2
Red1
+Ox2
Ox1 + ne– → Red1
Cu2+ + 2e– → Cu0
CuSO4
+ Zn →
ZnSO4
+ Cu
Red2 – ne– → Ox2
Zn0 – 2e– → Zn2+
Метод валентных связей
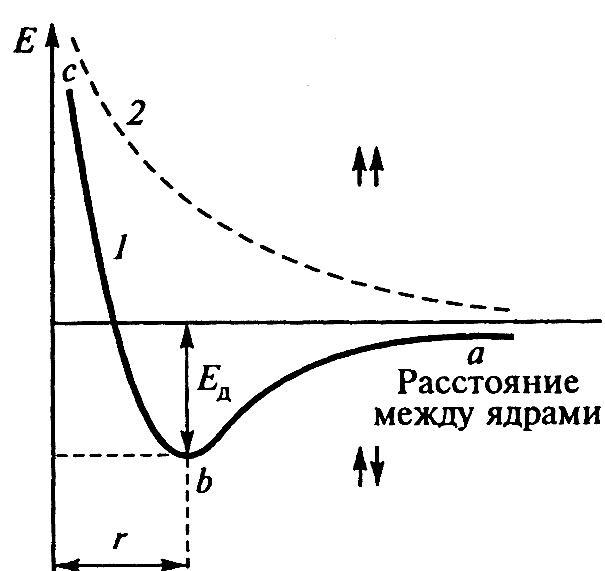
1927 Г. – Гейтлер и Лондон Квантово-механический расчет молекулы водорода
|
Внешние (валентные) электроны Спины электронов антипараллельны r – длина связи, min E Максимальное перекрывание атомных орбиталей Валентность = число неспаренных электронов
|
Механизмы образования связи
Обменный А• + •B А:В
|
Донорно-акцепторный А: + В А:В BF3 + F– [BF4]– :NH3 + H+ [NH4]+
|
Механизм образования ковалентной связи.
МВС позволяет различать три механизма образования ковалентной связи: обменный, донорно-акцепторный, дативный.
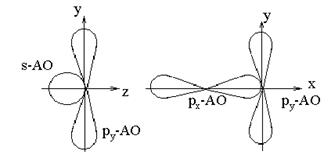
Обменный механизм. К нему относят те случаи образования химической связи, когда каждый из двух связываемых атомов выделяет для обобществления по одному электрону, как бы обмениваясь ими. Для связывания ядер двух атомов нужно, чтобы электроны находились в пространстве между ядрами. Эта область в молекуле называется областью связывания (область наиболее вероятного пребывания электронной пары в молекуле). Чтобы произошел обмен не спаренными электронами у атомов необходимо перекрывание атомных орбиталей. В этом и заключается действие обменного механизма образования ковалентной химической связи. Атомные орбитали могут перекрываться только в том случае, если они обладают одинаковыми свойствами симметрии относительно межъядерной оси .
|
