- •1.Современное состояние гидролизного производства в Республике Беларусь.Перспективы его развития.
- •2.Сырье для гидролизной и микробиологической промышленности. Сырьевая база гидролизного производства Республики Беларусь.
- •3.Технологическая характеристика гидролизного сырья. Его подготовка, хранение и подача в про-во
- •4 Кинетика перколяционного гидролиза (пг) полисахаридов. Факторы влияющие на скорость гидролиза.
- •5 Константа скорости гидролиза пс. Факторы вл-е на скорость гидролиза пс.
- •6. Причины трудной гидролизуемости полисахаридов. Особенности гидролиза гц и ц.
- •7.Кинетика вторичных превращений моносахаридов. Факторы, влияющие на скорость распада моносахаридов.
- •8.Механизм кислотно-каталитического расщепления гликозидных связей пс разбавл. К-ми
- •9. Превращение ком-ов древесины в пр-се гид-за
- •10. Выход мс при одноступенчатом многоступенчатом и пггц. Влияние кинетических и макрокинетических факторов на реальный выход мс.
- •11. Классификация основных методов гидролиза.
- •I.По факторам химической кинетики.
- •II.Макрокинетические признаки(диффузионные и гидродинамич явления)
- •III.По техническим признакам.
- •12.Особенности гидролиза растительного сырья концентрированными кислотами. Превращение целлюлозы под действием концентрированных кислот.
- •13. Техн. Схема гид-го отделения.
- •16. Двухстадийный гидролиз растительного сырья с раздельным отбором пентозного и гексозного г-та.
- •17.Двухстадийный гидролиз растительного сырья с возвратом части гексозного гидролизата на загрузку и гидролиз гемицеллюлоз.
- •18.Устройство гидролизаппарата (г/а) периодическо действия(п/д).
- •20.Риу. Пути повышения эффективности его работы.
- •22.Химический состав гидролизата. Влияние компонентов гидролизата на процессы биохимической переработки.
- •24. Продуценты кб и требов., предъявл. К ним. Хар-ка микрофлоры ф-ов в пр-ве кд.
- •25. Влияние физических и химических факторов на мо. Способы хранения посевн-о мат-ла.
- •26. Строение и состав дрожжевой клетки.
- •27.Способы питания микроорганизмов. Особенности поступления питательных веществ в клетку.
- •29. Теоретические основы непрерывного глубинного культивирования дрожжей в режиме хемостата.
- •30.Фермен-ры и режимы ферм-ции в произ-ве корм дрож-й.
- •31.Двухступенчатая ферментация в произв-ве корм белка.
- •32.Технология концентрирования дрожжевой суспензии.
- •33.Сушка дрожж. Рецирк суш агента. Получ гран-го прод. Устр,прин действия срц и меропр,обесп её норм безопасн.
- •34. Технология производства кормовых дрожжей. Требов к кач-ву корм дрожжей. Технико-эк пок-ли произ-ва.
- •35.Проблема охраны окр среды в гидролизном произв-ве и пути их решения.
- •36.Состав и доброкачественность сфи щёлока, особ-сти его подготовки к ферментац процессам.
- •37. Предгидролизаты сф(а)вц. Состав и переработка.
- •38. Получение лс при перераб-ке сф(и)щ и их исп-ие.
- •39. Прямая микробиологическая трансформация целлюлозосодержащих материалов в этанол.
- •40. Ферментативный гидролиз растительного сырья, его преимущества и недостатки. Механизм ферментативного гидролиза.
- •41. Методы повышения реакц спос-сти ц из растит сырья
- •39. Прямая микробиол трансформации целлюлозосод-х субстратов с целью получэтил спирта
- •42.Перспективы и основные направления прямой биоконверсии растительного сырья.
- •44. Производство кормового гидролизного сахара.
- •45.Виды раст.-углевод. Добавок,принц.Их получ.
- •46.Получение рук-1 и рук-2
- •47.Облагораживание сырья,пг и очисткаПг в производстве пищевого ксилита.
- •49.Технология спирт брожения и пути её соверше-ния. Микрофлора. Способы борьбы с инфекцией.
- •50.Теоретич основы ректиф-го выд-ния и очистки этанола.
- •51. Технология пр-са ректификации спирта из бражки
- •52.Получение жидкого и тв со2
- •53. Методы получения фск
- •54. Технология получения фск с прим кислотных катализаторов.
- •55. Фурфурольно-гексозный гидролиз
- •56. Получение ф-ла в пр-се парофазного гид-за пентозансодержащ раст-го сырья с исп-ем солевых кат.
- •57. Кинетика образов-ия фур-ла.
- •59. Особен-ти технологии выделения ф-ла из конд-ов паров самоиспар-ия гидрол-та.
- •60.Производные ф. И принц. Их получ.
- •62.Технол.Получ. Фурфурил.Спирта фс
- •63. Пути создания малоотходных производств в гидролизном производстве. Окж исп и очистка.
- •64. Методы очистки сточных вод.
- •65 Харак-ка основных направлений использов-я гидролиз лигнина (л):
- •66.Методы химической переработки лигнина.
- •67.Использование гидролизного лигнина в натуральной форме.
- •70. Биосинтез белка в дрожжевой клетке.
- •72. Биохимия образования этанола дрожжами.
- •73. Производство премиксов.
- •74. Получ-ие мат-ов на основе сорбц-ых св-в л: полифепана,удоб-ий (лсу,ому), коллактивита.
- •31. Особ-ти получения эт. Спирта из пищевого сырья
- •32.Получение топливного этанола.
- •71 Ассимиляция мс и орг к-т…
70. Биосинтез белка в дрожжевой клетке.
C 2H12O6 2CH3COCOOH
2H12O6 2CH3COCOOH
гликолиз пируват пируват-декар
боксилаза
2 CH3CH2OH 2CH3CHO
Алкаголь-дегидрогеназа
-
Спиртовое брожение. Преоблад. продукт - этиловый спирт. Возбудители: дрожжи Saccharomyces ccrevisiac, S.uvarum, Schizosacci aromyces pombe, бактерии Zymomonas mob His. Субстраты - глюкоза, фруктоза, сахароза, мальтоза, галактоза. Изв-но 3 сп-ба спиртового брож-я, отлич-ся др. от др. ем, какой из 3-х катабол. путей расщепления глюкозы реализ-ся - гликолиза (дрожжи), пентозофосф. пути (гетерофермент. молочнокислые бактерии, прод-ты брож-я - этанол и молочная к-та) или путь Энтнера-Дудорова (бактерии Zymomonas mobilis, прод-ты брож-я -этанол, ССЬ, небольшое кол-во молочной к-ты). Чаще клетки дрожжей исп-т гликолиз, и его конечный продукт (пируват) служит субстратом спиртового брож-я. В ходе 2-х р-ций брожения пируват превр-ся в этанол. Проц-с сопровожд-ся регенерацией 2-х мол-л НАД4, к-рые снова могут уч-ть в окислении глюкозы до пирувата.
Следуе отметить, что_АТФ запас-ся только в гликолизе, в р-циях собственно спирт брож-я этого не происх-т. Этанол удал-ся из клеток. м-ду кол-вом этанола и СО2 собл-ся эквивал-ть - на 2 мол-лы этанола образ-ся 2 мол-лы СО2. Кроме этанола образ-ся примеси - глицерол, уксусны альдегид, др. альдег, эфиры, кетоны, спирты, орг. к-ты.
72. Биохимия образования этанола дрожжами.
В связи с тем, что дрожжи ассимилируют готовые органические соединения и не усваивают Н2СО3, они относятся к гетеротрофным микроорганизмам, а по типу дыхания − к факультативным анаэробам, т. е. способны развиваться как в анаэробных условиях в отсутствии кислорода, так и в аэробных условиях.
При спиртовом брожении происходят ферментативные превращения гексозных моносахаридов в анаэробных условиях, приводящие к их неполному окислению и сопровождающиеся выделением энергии. В этих окислительных реакциях акцептором водорода является не кислород, а промежуточные продукты превращений углеводов, например уксусный альдегид. Биохимические процессы анаэробиоза протекают внутри дрожжевой клетки, куда через полунепроницаемую оболочку поступают моносахариды и необходимые неорганические питательные вещества. Продукты метаболизма − этанол, диоксид углерода и примеси выделяются из клетки в сбраживаемое сусло.
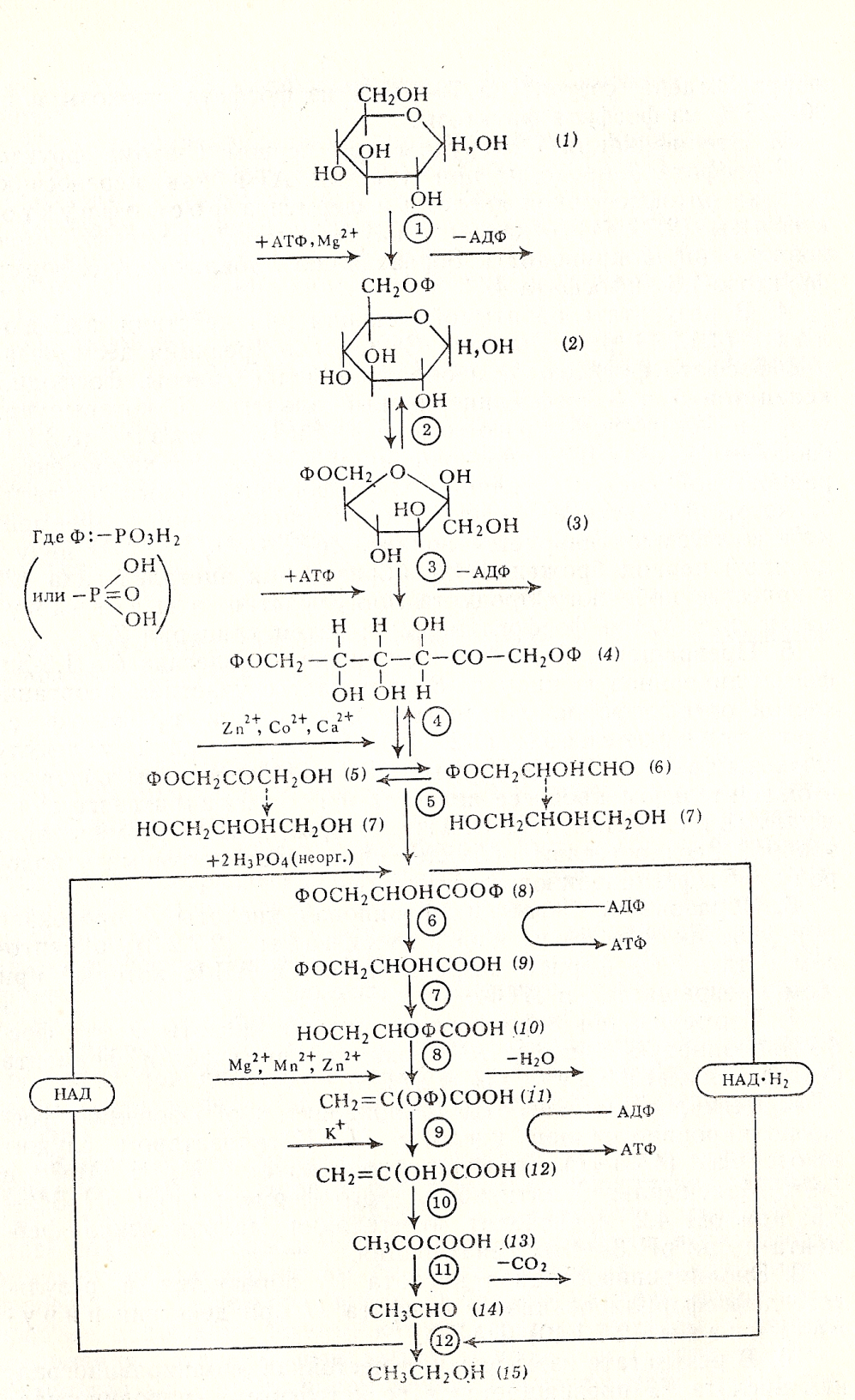
Основные стадии химизма спиртового брожения на примере превращений D-глюкозы, которая является основным углеводным компонентом гидролизных субстратов.
Фосфорилирование D-глюкозы 1 происходит при участии в качестве катализатора фермента гексокиназы. Каталитическая активность этого фермента повышается в присутствии Mg2+. Переносчиком группы − РО3Н2 является трифосфат адениновой кислоты (аденозинтрифосфат − АТФ), который превращается в аденозиндифосфат (АДФ). D-Глюкоза в этой реакции этерифицируется в пиранозной форме; ее реакционная способность при этом возрастает. Скорость образования фосфорного эфира D-глюкозы (глюкозо-6-фосфата) 2 определяет общую скорость брожения.
Изомеризация глюкозо-6-фосфата 2 в фруктозо-6-фосфат 3 протекает при участии фермента глюкозофосфатизомеразы. Равновесная система, получившая название эфира Эмдена, состоит на 70−75% из фосфата глюкозы и на 30−25 % из фосфата фруктозы.
Этерификация ОН-группы при первом С-атоме фруктозо-6-фосфата 3 проходит при участии АТФ как переносчика остатка ортофосфорной кислоты и фермента фосфофруктокиназы в качестве катализатора. Раскрытие пиранозного цикла приводит к образованию лабильной оксоформы фруктозо-1,6-дифосфата 4.
4.В результате обратимой реакции при действии альдолазы расщепляется С−С-связь (реакция десмолиза) в дифосфате фруктозы 4 и образуются две триозы: фосфодиоксиацетон 5 и 3-фосфоглицериновый альдегид 6, которые при участии фермента триозофосфатизомеразы способны к взаимным превращениям. Основным компонентом равновесной системы является 3-фосфоглицериновый альдегид 6, который участвует в дальнейших превращениях. Фермент альдолаза активируется ионами Zn2+, Со2+, Са2+. В индукционный период брожения (до образования ацетальдегида 12) в качестве побочного продукта при участии альдегидмутазы образуется фосфоглицерин и затем глицерин 7.
Превращение 3-фосфоглицеринового альдегида 6 в 1,3-дифос-фоглицериновую кислоту 8 протекает с участием неорганической ортофосфорной кислоты в присутствии триозофосфатдегидрогеназы. В расчете на 1 молекулу глюкозы требуется 2 молекулы Н3Р04. Переносчиком водорода в окислительном процессе является никотинамидаденин-иуклеотид (НАД), который как кофермент анаэробной дегидрогеназы обладает способностью отнимать водород от фосфоглицеринового альдегида.
Образование 3-фосфоглицериновой кислоты 9 протекает при участии фосфоглицераткиназы; акцептором остатка фосфорной кислоты является АДФ, который при этом превращается в АТФ.
Изомеризация 3-фосфоглицериновой кислоты 9 в 2-фосфоглицериновую кислоту 10 проходит при участии фермента фосфоглицеромутазы.
Дегидратация кислоты 10 приводит к образованию фос-фоэнолпнровиноградной кислоты 11. Катализатором служит энолаза, активируемая ионами Mg2+, Мп2+ и Zn2+. Максимальная активность этого фермента при рН 5,2− 5,5; при рН 4,2 происходит агрегатация макромолекул фермента и при рН 3−4 их денатурация.
Энолпировиноградная кислота 12 образуется в результате дефосфорилирования ее фосфата 11 при действии пируваткиназы и АДФ.
Декарбоксилирование пировиноградной кислоты 13 при участии пируватдекарбоксилазы приводит к образованию уксусного альдегида 14.
Восстановление ацетальдегида 14 в этанол 15 протекает при участии НАД-2Н и фермента алкогольдегидрогеназы. При этом кофермент регенерируется путем окисления в НАД.
По такой же схеме происходит биосинтез этанола и из других гексоз гидролизного субстрата − D-маннозы и D-галактозы.
Из рассмотренной схемы видно, что для нормального протекания спиртового брожения необходимо наличие в субстрате неорганического фосфорного питания и макро- и микроэлементов К, Mg, Са, Mn, Zn и Со, активирующих ферменты.
Суммарное стехиометрическое уравнение спиртового брожения, установленное еще Гей-Люссаком,
С6Н1206 − > 2С2Н5ОН + 2С02
может быть представлено с учетом роли АТФ в жизненных процесса следующим образом:
С6Н1206 + 2АДФ + 2Н3Р04 −> 2С2Н5ОН + 2С02 + 2АТФ
Изменение свободной энергии в этом процессе составляет более 200 кДж/моль, в том числе 83,4 кДж/моль улавливается в АТФ и используется для осуществления жизненных функций микроорганизмов. Остатки фосфорной кислоты в АТФ присоединены макроэргическими связями, при расщеплении которых освобождается примерно в 3 раза больше энергии, чем при расщеплении обычных химических связей. Освобождение энергии макроэргических связей происходит при переносе − РО3Н2 групп, а не путем гидролиза, при котором свободная энергия переходит в тепловую.
В анаэробных условиях происходит медленное размножение дрожжей. При биосинтезе белка и других компонентов клеток кроме энергии затрачивается часть питательных веществ субстрата.
При спиртовом брожении в качестве примеси образуется глицерин, выход которого возрастает в присутствии бисульфита (например, NaHS03, KHS03) или в щелочной среде. В составе спиртовой бражки содержится ацетальдегид, являющийся промежуточным продуктом биосинтеза этанола. Среди многочисленных легколетучих примесей бражки найдены альдегиды, простые и сложные эфиры, кетоны, спирты, кислоты и другие соединения. Значительный выход эфиров при спиртовом брожении связан с протеканием реакций этерификации, катализируемых ферментами эстеразами. Основной компонент эфирной фракции − этилацетат 17, образуется при взаимодействии этанола 15 и уксусной кислоты 16.
С2Н5ОН + СН3СООН <=> CH3CO2C2H5 + Н20
15 16 17
В процессе обмена веществ, главным образом при размножении микроорганизмов, в качестве побочных продуктов брожения образуются высшие спирты. Их выход возрастает при наличии аминокислот, которые попадают в субстрат из исходного сырья, а также при автолизе отмерших дрожжевых клеток. В условиях брожения происходит декарбоксилирование и гидролитическое дезаминирование аминокислот с образованием пропанола, изобутанола, амилола, изоамилола и других спиртов, которые при ректификации образуют фракцию сивушных масел.
Основным компонентом сивушных масел является изоамиловый спирт 21, который образуется из лейцина 18:
( (СН3)2СНСН2СН (NH2) СООН + СНзСОСООН −> СН3СН (СН3) СН2СОСООН + 18 13 19
+ CH3CH(NH2)COOH
20
-С02 +Н2
СОН3СН(СН3)СН2СОСОО −−> (СН3)2СНСН2СНО −−> СН3СН(СН3)СН2ОН
19 20 21
На первой стадии происходит процесс переаминирования − обмен аминогруппой между аминокислотой 18 и кетокислотой (пировиноградной кислотой 13, при этом образуется аланин 20 и изопропилвиноградная кислота 19, декарбоксилирование которой приводит к изовалериановому альдегиду 20, при восстановлении которого образуется изоамилол 21. Все стадии процесса протекают при участии ферментов.