- •1. Понятие об электродном потенциале. Равновесный электродный потенциал.
- •2. Гальванический элемент Якоби-Даниэля.
- •3. Газовые электроды: водородный, кислородный
- •4. Эдс гальванического элемента. Связь эдс с энергией Гиббса
- •5. Водородный электрод. Стандартные потенциалы металлов.
- •6. Ряд напряжений металлов. Уравнение Нернста.
- •7. Концентрационный гальванический элемент.
- •8. Окислительно-восстановительные г.Э.
- •9. Поляризация электродов в г.Э.
- •10. Понятие об электролизе. Электролиз расплавов солей.
- •11. Электролиз водных растворов солей.
- •12. Поляризация электродов при электролизе. Потенциал разложения.
- •13. Электролиз с растворимыми анодами.
- •14. Электрохимическое рафинирование металлов.
- •15. Практическое применение электролиза.
- •16. Влияние кислотности среды на процесс коррозии.
- •17. Устройство и принцип действия свинцового аккумулятора.
- •18. Устройство и принцип действия сухого марганцево-цинкового элемента.
- •19. Устройство и принцип действия щелочных аккумуляторов.
- •20. Химическая и электрохимическая коррозия металлов.
- •21. Коррозия металлов в кислой и нейтральной среде.
- •22. Коррозия технического железа.
- •23. Электрохимическая коррозия при контакте двух металлов.
- •27. Диэлектрики и полупроводники.
- •28. Полупроводники примесного типа.
- •29. Собственные полупроводники.
- •30. Закон сохранения энергии. Энтальпия системы.
- •31. Закон Гесса. Термодинамические уравнения.
- •32. Энтропия и её изменение при химических процессах.
- •33. Энергия Гиббса и энергия Гельмгольца.
- •34. Связь между различными термодинамическими функциями.
- •35. Скорость гомогенных химических реакций.
- •36. Молекулярность и порядок реакций. Константа скорости реакции первого порядка.
- •37. Скорость гетерогенных химических реакций.
- •38. Зависимость скорости химической реакции от температуры. Правило Вант-Гоффа и уравнение Аррениуса.
- •39. Энергия активации химических реакций.
- •40. Химическое равновесие, константа равновесия, её связь с термодинамическими функциями.
- •41. Смещение химического равновесия. Принцип Ле-Шателье.
- •42. Зонная теория кристаллов.
- •43. Типы и свойства кристаллов.
- •44. Строение кинофотоматериалов.
- •45. Химизм основных стадий фотографического процесса.
- •46. Связь между различными термодинамическими функциями.
- •47. Структура и свойства полимеров.
- •48. Химические свойства полимеров.
- •49. Материалы на основе полимеров.
- •50. Методы получения полимеров.
15. Практическое применение электролиза.
- рафинирование металлов - при электролизе водных растворов солей с активным анодом получают Zn,Mn, Cr, Ni, Co - при электролизе расплавов солей получают активные металлы - при электролизе получают важнейшие газы (Сl, H, O) - электролизом наносят защитные покрытия на изделия: * защита от коррозии * (защитно)декоративные * (Cu, Ag, Au) для увеличения электропроводности металла * с целью увеличения твердости * с целью придания металлических свойств(Ni+Co, Ni+Fe) - гальванопластика – получение точных копий изделий, имеющих сложную форму, методом электролиза - анодирование Al (Al -3e --> Al2O3)
16. Влияние кислотности среды на процесс коррозии.
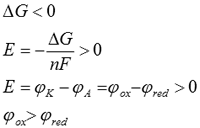
Окислителем в кислой среде являются ионы водорода.

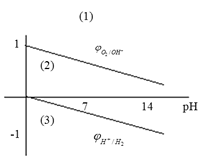
1. ![]() водородного
и кислородного электродов. Такие металлы
коррозии не подвергаются.
водородного
и кислородного электродов. Такие металлы
коррозии не подвергаются.
2. ![]() подвергаются
коррозии в нейтральной среде (Ag, Cu).
подвергаются
коррозии в нейтральной среде (Ag, Cu).
3. ![]() подвергаются
коррозии в кислой и нейтральной среде.
подвергаются
коррозии в кислой и нейтральной среде.
17. Устройство и принцип действия свинцового аккумулятора.
аккумулятор – устройство, в котором химическая энергия превращается в электрическую, а электрическая – в химическую. Свинцовый аккумулятор имеет 2 вида пластин: одни из чистого свинца, а другие – из двуокиси свинца (PbO2). В качестве электролита используется серная кислота концентрацией 32-39% имеющая плотность 1,23-1,30 грамм/см3. чем выше концентрация серной кислоты, тем ЭДС аккумулятора больше. Однако не рекомендуется использовать кислоту с концентрацией больше 39% (она начинает реагировать с синцом, и снижается ее электропроводность).
Разрядка
(эксплуатация)
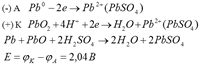 Т.
к. в процессе эксплуатации понижается
концентрация серной кислоты и расходуется
энергия, то ЭДС постоянно уменьшается.
И она может быть снижена до ЕПР~1,7 В.
При
меньшем значении ЭДС наблюдается
явление сульфитации пластин, т. е.
покрытие пластин пленкой сульфата
свинца с особой кристаллической
структурой, которая изолирует активную
массу пластин и не может быть разрушена
при дальнейшем процессе зарядки.
Т.
к. в процессе эксплуатации понижается
концентрация серной кислоты и расходуется
энергия, то ЭДС постоянно уменьшается.
И она может быть снижена до ЕПР~1,7 В.
При
меньшем значении ЭДС наблюдается
явление сульфитации пластин, т. е.
покрытие пластин пленкой сульфата
свинца с особой кристаллической
структурой, которая изолирует активную
массу пластин и не может быть разрушена
при дальнейшем процессе зарядки.
Процесс
зарядки: При
зарядке химические реакции протекают
в противоположную сторону
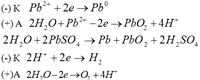
|+| относительно недорогой, высокий КПД (до 80%), высокая электрохимическая емкость |-| саморазряд при хранении, срок службы 2-5 лет
18. Устройство и принцип действия сухого марганцево-цинкового элемента.
Сухой марганцево-цинковый Г. Э.: металлический стакан из цинка – анод. В качестве катодного вещества – двуокись марганца. Графитовый стержень является токоотводом. В качестве электролита используется водный раствор хлористого аммония (NH4Cl). В качестве загустителя – мука, крахмал. Элемент одноразового использования.