
- •1. Понятие об электродном потенциале. Равновесный электродный потенциал.
- •2. Гальванический элемент Якоби-Даниэля.
- •3. Газовые электроды: водородный, кислородный
- •4. Эдс гальванического элемента. Связь эдс с энергией Гиббса
- •5. Водородный электрод. Стандартные потенциалы металлов.
- •6. Ряд напряжений металлов. Уравнение Нернста.
- •7. Концентрационный гальванический элемент.
- •8. Окислительно-восстановительные г.Э.
- •9. Поляризация электродов в г.Э.
- •10. Понятие об электролизе. Электролиз расплавов солей.
- •11. Электролиз водных растворов солей.
- •12. Поляризация электродов при электролизе. Потенциал разложения.
- •13. Электролиз с растворимыми анодами.
- •14. Электрохимическое рафинирование металлов.
- •15. Практическое применение электролиза.
- •16. Влияние кислотности среды на процесс коррозии.
- •17. Устройство и принцип действия свинцового аккумулятора.
- •18. Устройство и принцип действия сухого марганцево-цинкового элемента.
- •19. Устройство и принцип действия щелочных аккумуляторов.
- •20. Химическая и электрохимическая коррозия металлов.
- •21. Коррозия металлов в кислой и нейтральной среде.
- •22. Коррозия технического железа.
- •23. Электрохимическая коррозия при контакте двух металлов.
- •27. Диэлектрики и полупроводники.
- •28. Полупроводники примесного типа.
- •29. Собственные полупроводники.
- •30. Закон сохранения энергии. Энтальпия системы.
- •31. Закон Гесса. Термодинамические уравнения.
- •32. Энтропия и её изменение при химических процессах.
- •33. Энергия Гиббса и энергия Гельмгольца.
- •34. Связь между различными термодинамическими функциями.
- •35. Скорость гомогенных химических реакций.
- •36. Молекулярность и порядок реакций. Константа скорости реакции первого порядка.
- •37. Скорость гетерогенных химических реакций.
- •38. Зависимость скорости химической реакции от температуры. Правило Вант-Гоффа и уравнение Аррениуса.
- •39. Энергия активации химических реакций.
- •40. Химическое равновесие, константа равновесия, её связь с термодинамическими функциями.
- •41. Смещение химического равновесия. Принцип Ле-Шателье.
- •42. Зонная теория кристаллов.
- •43. Типы и свойства кристаллов.
- •44. Строение кинофотоматериалов.
- •45. Химизм основных стадий фотографического процесса.
- •46. Связь между различными термодинамическими функциями.
- •47. Структура и свойства полимеров.
- •48. Химические свойства полимеров.
- •49. Материалы на основе полимеров.
- •50. Методы получения полимеров.
49. Материалы на основе полимеров.
(Волокна, пенки, лаки, пластмассы, композиты)
волокна получают путем продавливания расплава полимера через тонкие отверстия – фильеры. А затем проводится процесс охлаждения. В качестве волокнообразующих полимеров используют полиакрилоамиды, полиакрилонитрилы пленки получают путем продавливания расплавов полимеров через фильеры, которые имеют щелевидную форму. Или путем нанесения раствора полимера на движущуюся ленту (полиэтилен, полистирол, полипропилен) лаки – растворы волокнообразующих полимеров в растворителях. Кроме полимера в лаках содержатся: красители, наполнители, стабилизаторы, отвердители (покраска, нанесение на контакты) пластмассы. Кроме полимера вводят следующие вещества: красители, наполнители, пластификаторы, стабилизаторы делятся на 1 термопласты (могут неоднократно переходить из вязко-текучего состояния в стеклообразное. Используются шире, чем реактопласты (полиэтилен, полистирол, полихлорвинил)) 2 реактопласты ( при получении происходит образование сетчатой структуры полимера. В результате полимер из вязко-текучего состояния переходит в стеклообразное и в дальнейшем не может быть возвращен в исходное состояние (фенолформальдегидные и эпоксидные смолы)) композиты. Основу составляет полимер, в который вводятся армирующие добавки (ткань, металл, керамика). Все композиты обладают повышенной прочностью, в некоторых случаях превышающей прочность металла.
Отдельные представители: Полиэтилен получают радикальной полимеризацией из этилена. Существует полиэтилен высокого давления (Т=2000С, p=300 атм.) и низкого давления (Т=2000С, р<5 атм.), он обладает лучшими физико-механическими свойствами ( - СН2 – СН2 -) Полиэтилен используют при температуре от 20 до 1000С. Стоек к действию кислот и щелочей, однако набухает в органических растворителях, является хорошим изоляционным материалом, не про пускает влагу, используется для получения пленок в аппаратуростроении
Полистирол получают
радикальной полимеризацией стирола.
Стоек к действию кислот, оснований,
органических растворителей. Дороже
полиэтилена, используется реже (в
приборостроении)
![]()
Политетрофторэтилен (фторопласт) получают радикальной полимеризацией тетрофторэтилена. Температурный предел от -200 до 2500С. Исключительно стоек к действию концентрированных кислот, щелочей, органических растворителей. Используется как изоляционный материал для химической промышленности ( - CF2 – CF2 - )
Каучуки
Общего
назначения – получение резины для
массового потребления (бутадиеновый
каучук, изопропеновый каучук, бутадиенстирольный
каучук
![]() Специального
назначения – стойкие к действию масел
(хлоропреновый каучук), высокопрочные
(полиуретановый каучук)
Бутадиен-нитрильный
каучук
Специального
назначения – стойкие к действию масел
(хлоропреновый каучук), высокопрочные
(полиуретановый каучук)
Бутадиен-нитрильный
каучук
![]()
50. Методы получения полимеров.
1 метод полимеризации Полимеризация – метод получения полимеров путем последовательного присоединения отдельных молекул мономера, в результате которого образуются длинные цепи и не выделяется побочных продуктов в качестве исходных продуктов используют соединения, содержащие двойные или тройные связи, или высокореакционные циклы (из трех атомов). В результате процесса полимеризации происходит раскрытие двойных и тройных связей и циклов.
Процесс полимеризации самопроизвольно протекающий процесс, энергия Гиббса меньше 0, протекает очень медленно. Для увеличения скорости процесса вводят катализаторы. В зависимости от того, какие введены катализаторы, механизм полимеризации может быть радикальным или ионным. Радикальная полимеризация включает 3 стадии 1. зарождение цепей 2. рост цепей 3. обрыв цепи 1) частицы, несущие неспаренный е – радикальные частицы
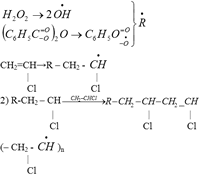
R – концевая группа. Не влияет на свойства полимера, ее молекулярная масса низка по отношению к массе полимера 3) Наступает: - в реакционную массу вводят ингибиторы - если в реакционной массе сталкиваются 2 радикальные частицы - в процессе радикалы сталкиваются между собой R+R. Ионная полимеризация может инициироваться положительно заряженными частицами (катионами) или отрицательно заряженными частицами (анионами) 3 стадии
2 метод поликонденсации в реакцию вступают мономеры, содержащие по крайней мере 2 функциональные группы, различающиеся по основности. В результате происходит взаимодействие между этими функциональными группами и последующий рост молекулы полимера. Образуются побочные продукты (H2O, HCl, NH3). Общая формула полимера не соответствует формуле мономера.
