
- •1. Электролитическая диссоциация.
- •2. Электролитическая диссоциация воды. Ионное произведение воды.
- •2. Электролитическая диссоциация воды. Ионное произведение воды.
- •3. Равновесие на границе раствор-электрод. Электрохимические цепи.
- •4. Водородный электрод. Электродные реакции. Электродный потенциал.
- •5. Элемент Якоби-Даниэля. Уравнение Нернста.
- •6. Химическая связь и строение полупроводниковых веществ. Металлы, полупроводники и диэлектрики. Энергетические зоны в металлах, полупроводниках и диэлектриках.
- •7. Собственная проводимость полупроводников. Элементарные полупроводники IV группы
- •8. Донорные и акцепторные примеси в полупроводниках.
- •9. Бинарные полупроводники aiiibv типа. Бинарные полупроводники аiibvi типа.
- •10. Бинарные полупроводники aiiibv типа. Бинарные полупроводники аiibvi типа.
- •11. Первый закон термодинамики. Энтальпия.
- •12. Первый закон термодинамики. Закон Гесса.
- •13. Определение теплового эффекта химической реакции
- •14. Второй закон термодинамики. Энтропия
- •17. Второй закон термодинамики. Энтропия как степень беспорядка системы.
- •18. Химическая термодинамика. Предмет и методы. Перечень вопросов на который позволяет ответить химическая термодинамика.
- •19. Понятие функции состояния. Закон Гесса.
- •20. Следствия из закона Гесса. Вычисление тепловых эффектов химических реакций. Следствия из закона Гесса
- •1) Тепловой эффект образования химического соединения равен тепловому эффекту разложения со знаком (-)
- •21. Химическая термодинамика. Предмет и методы. Перечень вопросов на который позволяет ответить химическая термодинамика.
- •22. Термодинамика агрегатных (фазовых) превращений. Процессы фазовых превращений.
- •23. Уравнение Клапейрона — Клаузиуса
- •24. Фазовое равновесие: твердое кристаллическое тело — жидкость.
- •25. Фазовое равновесие: жидкость — пар.
- •26.Фазовое равновесие: твердое тело — пар.
- •27. Правило фаз Гиббса. Диаграмма состояния однокомпонентной системы.
- •28. Адсорбция. Природа адсорбционных сил. Физическая и химическая адсорбция. Определение абсорбции.
- •29. Потенциальная кривая адсорбированной молекулы. Теплота адсорбции.
- •30. Адсорбционное равновесие. Время жизни адсорбированной молекулы.
- •31. Многомолекулярная локализованная адсорбция. Изотерма адсорбции Ленгмюра.
- •32. Диффузия. Определение и основные понятия.
7. Собственная проводимость полупроводников. Элементарные полупроводники IV группы
*Собственной проводимостью полупроводников называется проводимость, обусловленная движением под действием электрического поля одинакового числа свободных электронов и дырок, образовавшихся вследствие перехода электронов полупроводника из валентной зоны в зону проводимости. В идеальном полупроводнике при собственной проводимости концентрации электронов (ni) и дырок (pi) равны и много меньше числа уровней в валентной зоне и зоне проводимости. Поэтому свободные электроны занимают уровни вблизи дна зоны проводимости Ec, а свободные дырки - вблизи потолка валентной зоны Ev (рис. 1). При этом:
ni = pi = A exp(-DE/2kT), (1)
где A=4,82Ч1015T 3/2(mn*mp*/m2)3/4;
mn*, mp* - эффективные массы электрона и дырки;
m - масса электрона;
k - постоянная Больцмана;
DE - ширина запрещенной зоны полупроводника;
T - абсолютная температура (дыркам приписывается эффективная масса mp, равная по абсолютной величине эффективной массе того электрона, который занял бы это валентное состояние, но с противоположным знаком; эффективная масса электрона в валентной зоне вблизи Ev отрицательна).
*С точки зрения зонной теории, полупроводники – это вещества, ширина запрещенной зоны у которых находится в диапазоне 0,3< ΔE0 <3эВ Чем больше ширина запрещенной зоны, тем меньше вероятность того, что электрон перескочит в зону проводимости. Если это все же произошло, в зоне проводимости появляются подвижные электроны, а в валентной зоне – дырка. Электроны могут двигаться только в зоне проводимости, а дырки – только в валентной зоне. Наличие подвижных электронов и дырок обеспечивает полупроводникам собственную проводимость.
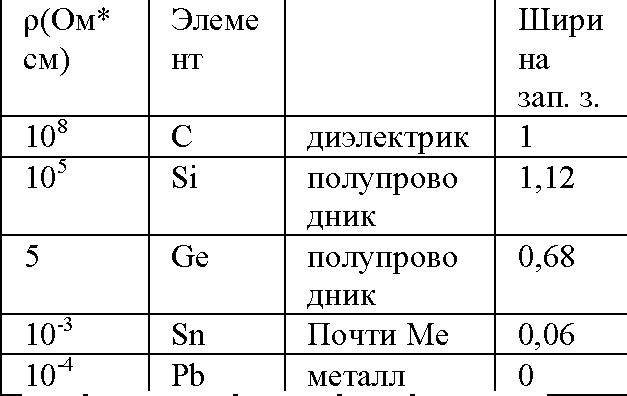
Элементарные полупроводники IV группы
Типы полупроводников в периодической системе элементов
В нижеследующей таблице представлена информация о большом количестве полупроводниковых соединений. Их делят на несколько типов: одноэлементные полупроводники IV группы периодической системы элементов, сложные: двухэлементные AIIIBV и AIIBVI из третьей и пятой группы и из второй и шестой группы элементов соответственно. Все типы полупроводников обладают интересной зависимостью ширины запрещённой зоны от периода, а именно — с увеличением периода ширина запрещённой зоны уменьшается.
Группа |
IIB |
IIIA |
IVA |
VA |
VIA |
|
|
|||||||||||||||||||||
Период |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
2 |
|
5 B |
6 C |
7 N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
3 |
|
13 Al |
14 Si |
15 P |
16 S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
4 |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
5 |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
6 |
80 Hg |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
