- •1. Электролитическая диссоциация.
- •2. Электролитическая диссоциация воды. Ионное произведение воды.
- •2. Электролитическая диссоциация воды. Ионное произведение воды.
- •3. Равновесие на границе раствор-электрод. Электрохимические цепи.
- •4. Водородный электрод. Электродные реакции. Электродный потенциал.
- •5. Элемент Якоби-Даниэля. Уравнение Нернста.
- •6. Химическая связь и строение полупроводниковых веществ. Металлы, полупроводники и диэлектрики. Энергетические зоны в металлах, полупроводниках и диэлектриках.
- •7. Собственная проводимость полупроводников. Элементарные полупроводники IV группы
- •8. Донорные и акцепторные примеси в полупроводниках.
- •9. Бинарные полупроводники aiiibv типа. Бинарные полупроводники аiibvi типа.
- •10. Бинарные полупроводники aiiibv типа. Бинарные полупроводники аiibvi типа.
- •11. Первый закон термодинамики. Энтальпия.
- •12. Первый закон термодинамики. Закон Гесса.
- •13. Определение теплового эффекта химической реакции
- •14. Второй закон термодинамики. Энтропия
- •17. Второй закон термодинамики. Энтропия как степень беспорядка системы.
- •18. Химическая термодинамика. Предмет и методы. Перечень вопросов на который позволяет ответить химическая термодинамика.
- •19. Понятие функции состояния. Закон Гесса.
- •20. Следствия из закона Гесса. Вычисление тепловых эффектов химических реакций. Следствия из закона Гесса
- •1) Тепловой эффект образования химического соединения равен тепловому эффекту разложения со знаком (-)
- •21. Химическая термодинамика. Предмет и методы. Перечень вопросов на который позволяет ответить химическая термодинамика.
- •22. Термодинамика агрегатных (фазовых) превращений. Процессы фазовых превращений.
- •23. Уравнение Клапейрона — Клаузиуса
- •24. Фазовое равновесие: твердое кристаллическое тело — жидкость.
- •25. Фазовое равновесие: жидкость — пар.
- •26.Фазовое равновесие: твердое тело — пар.
- •27. Правило фаз Гиббса. Диаграмма состояния однокомпонентной системы.
- •28. Адсорбция. Природа адсорбционных сил. Физическая и химическая адсорбция. Определение абсорбции.
- •29. Потенциальная кривая адсорбированной молекулы. Теплота адсорбции.
- •30. Адсорбционное равновесие. Время жизни адсорбированной молекулы.
- •31. Многомолекулярная локализованная адсорбция. Изотерма адсорбции Ленгмюра.
- •32. Диффузия. Определение и основные понятия.
5. Элемент Якоби-Даниэля. Уравнение Нернста.
Гальванический элемент Якоби-Даниэля состоит из двух полуэлементов соединенных металлических
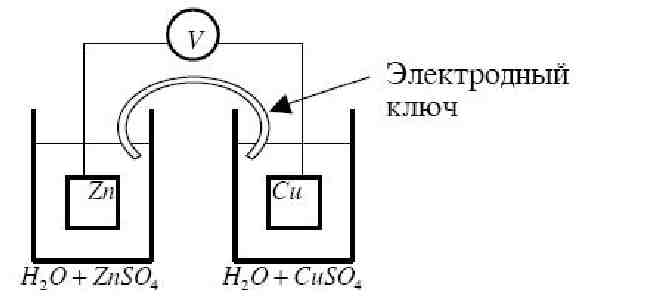
проводником.
Электродный ключ – стеклянная трубка,
заполненная агар-агаром, который
пропитан ионами солей и таким образом
ЭК обладает электродной
проводимостью.
Схема цепи:
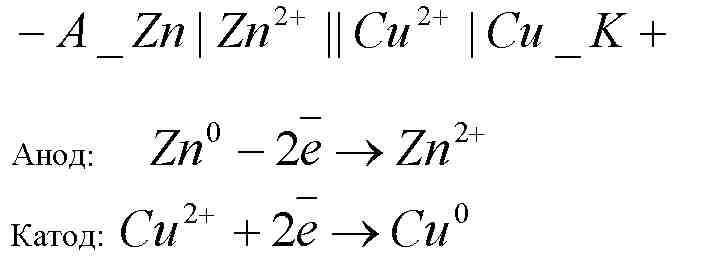
Катодная реакция осуществляется за счет электронов, которые переходят с анода на катод по металлическому проводнику, т.е. по нему течет электрический ток. Таким образом в гальваническом элементе Якоби-Даниэля происходит окислительно-восстановительная реакция, разнесенная в пространстве.
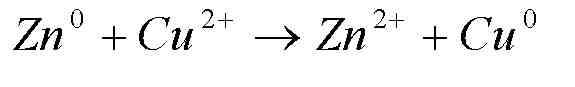
Уравнение Нернста связывает окислительно-восстановительный потенциал системы с активностями веществ, входящих в электрохимическое уравнение, и стандартными потенциалами окислительно-восстановительных пар.

6. Химическая связь и строение полупроводниковых веществ. Металлы, полупроводники и диэлектрики. Энергетические зоны в металлах, полупроводниках и диэлектриках.

Чтобы вещество проводило электрический ток необходимо и достаточно, чтобы в нем были электрические заряды в определенной концентрации и эти заряды имели возможность двигаться под действием электрического поля. Введем несколько количественных характеристик, с помощью которых можно описать проводимость вещества.
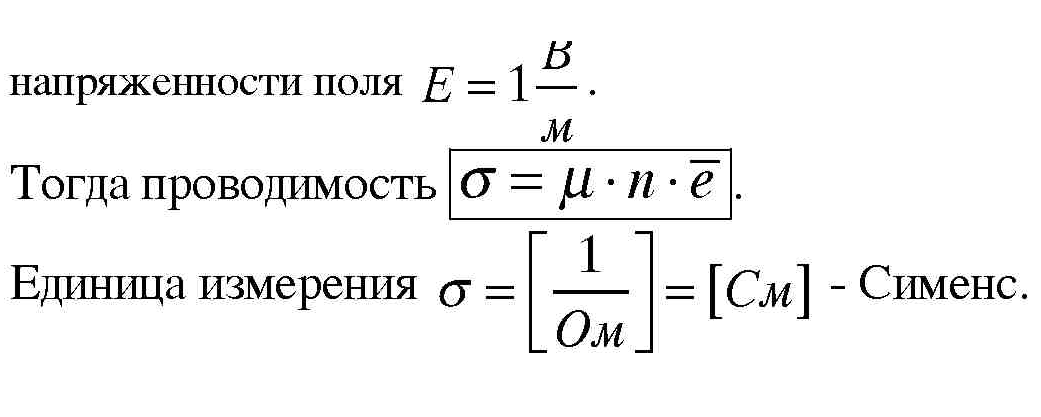
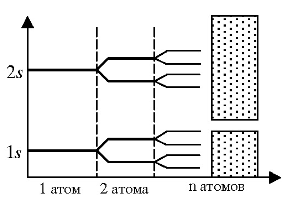
Рассмотрим Li, Z = 3, 1s22s1
|
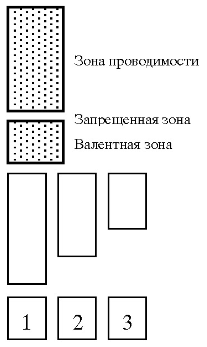
Зона, полностью заполненная электронами -валентная зона. Зона свободная от электронов и находящаяся по энергии выше валентной зоны - зона проводимости. Между валентной и зоной проводимости
может находиться запрещенная зона шириной АЕ0 .
Ширина запрещенной зоны определяется природой вещества:
- металлы АЕ0 <0,3эВ;
- полупроводники 0,3 < АЕ0 < 3эВ;
- диэлектрики АЕ0 > ЗэВ .
Рассмотрим два ярко выраженных проводника IV группы - Ge и Si. Ковалентные кристаллы этих веществ образуют кристаллическую решетку структуры алмаза. Каждый атом связан с четырьмя другими за счет ковалентных связей, образованных
sp3 гибридными орбиталями.
Полупроводник — материал, электрические свойства которого в сильной степени зависят от концентрации в нём химических примесей и внешних условий (температура, излучение и пр.).
Полупроводники – вещества, которые по своей удельной проводимости занимают промежуточное место между проводниками и диэлектриками и отличаются от проводников сильной зависимостью удельной проводимости от концентрации примесей, температуры и различных видов излучения. Полупроводниками являются вещества, ширина запрещённой зоны которых составляет 0-3 электрон-вольта, например, алмаз можно отнести к широкозонным полупроводникам, а InAs к узкозонным.
В зависимости от того, отдаёт ли примесь электрон или захватывает электрон, примесь называют донорной или акцепторной. Свойство примеси может меняться в зависимости от того, какой атом кристаллической решётки она замещает, в какую кристаллографическую плоскость встраивается. Проводимость полупроводников сильно зависит от температуры. Вблизи абсолютного нуля температуры полупроводники имеют свойства изоляторов.