
- •10. Реакции электрофильного присоединения в алкенах. Правило Марковникова с электронной точки зрения.
- •11. Рекция окисления, полимеризации алкенов. Использование продуктов полимеризации в ветеринарии, с/х( полипропилен, полиэтилен и др.).
- •13. Диеновые углеводороды с сопряженными связями. Строение. Дать понятие сопряжению. Способы получения.
- •14. Алкадиены с сопряженными связями. Особенности их поведения в химических реакциях 1,4- и 1,2- присоединения.
- •15. Строение тройной углерод-углеродной связи, ее реакционная способность
- •16. Гомологический ряд алкинов. Способы получения. Физические свойства. Физиологическое действие алкинов. Реакции замещения в Алкинах.
- •17. Взаимодействие алкинов с галогенами, водой, галогеноводородами. Использование продуктов реакции.
- •18. Бензол- ароматическая система. Дать понятия ароматичности. Ее влияние на реакционную способность соединения. Привести примеры ароматических соединений из других классов.
- •Число изомеров в ряду спиртов быстро растет: с5-восемь изомеров, с6- семнадцать, с10- пятьсот семь.
- •30. Реакционная способность глицерина. Применение продуктов реакции.
- •31. Простые и сложные эфиры на основе этанола. Их реакционная способность, практическое применение.
- •32. Способы получения фенолов, использование их в ветеринарии.
- •33. Реакционная способность фенола. Показать взаимное влияние гидроксильной группы и бензольного кольца на их реакционную способность.
- •34. Классификация альдегидов, кетонов. Номенклатура, изомерия. Физические свойства. Строение карбонильной группы. Реакционные центры.
- •35. Получение альдегидов и кетонов. Распространение в природе. Использование в ветеринарии и медицине.
- •36. Реакции замещения в альдегидах и кетонах по функциональной группе и по радикалу.
- •37. Реакции присоединения, идущие в альдегидах. Кетонах. Использование и распространение в природе продуктов реакции.
- •38. Получение полуацеталей (полукеталей). Значение этих реакций в химии углеводов.
- •39. Реакции полимеризации и конденсации альдегидов и кетонов. Их отличие.
- •64.Простые липиды(жиры). Классиф-я, распр-ние в природе,хим.Св-ва. Применение.
- •70. Аминоспирты. Строение. Распространение в природе. Холин. Коламин. Химические свойства.
- •71. Диамины. Путресцин. Кадаверин. Способы получения из аминокислот. Физ и хим свойства.
- •72. Анилин – ароматический амин. Физ и хим свойства. Использование производных анилина в ветеринарии, медицине. Сульфаниламидные препараты.
- •73. Амиды карбоновых кислот. Мочевина. Свойства, применение в сельском хозяйстве. Строение глутамина и аспарагина.
- •74. Аминокислоты. Строение. Биполярность аминокислот. Амфотерные свойства аминокислот. Строение и свойства глутамина и аспарагина. Электрофорез.
- •75. Химические свойства а-аминокислот. Реакции, идущие по nh2-группе.
- •76. Химические свойства аланина. Реакции, идущие по карбоксильной группе.
- •77. Отношение к нагреванию а,в,V аминокислот (дигидратация). Лактамы. Дикетопиперазины.
- •78. Белки. Общие представления о строении белков. Структурная организация белков. Денатурация.
- •79. Белки. Классификация. Протеины. Протеиды. Биологическая роль белков.
- •80. Пиридин как представитель шестичленных азотистых гетероциклов. Свойства. Биологически активные соединения на его основе. Никотиновая кислота.
- •81. Конденсированные азотистые гетероциклы. Индол и биологически активные соединения на его основе(триптофан, индолилуксусная кислота, триптамин).
- •82. Пиримидиновые азотистые основания и нуклеотиды на их основе.
- •83. Шестичленные азотистые гетероциклы с двумя гетероатомами. Пиримидин, цитозин, урацил, тимин.
- •84. Нуклеиновые кислоты. Нуклеозид, нуклеотид. Строение. Привести пример динуклеотида.
13. Диеновые углеводороды с сопряженными связями. Строение. Дать понятие сопряжению. Способы получения.
ДИЕНОВЫЕ УГЛЕВОДОРOДЫ (диены), ненасыщенные углеводороды с двумя двойными связями. Алифатич. диены СnН2n_2 наз. алкадиенами, алициклич. СnН2n_4 - циклоалкадиенами. Сопряжение - выравнивание, делокализация электронной плотности в молекуле с участием электронов п-связи
Сопряжение в алкадиенах наблюдается, когда две двойные связи разделены одной одинарной, как, например, в бутадиене- 1,3. При этом имеет место дополнительное перекрывание тт- орбиталей центральных углеродных атомов: 2-го и 3-го.
1 2 3 4
СН2—СН—СН—СН2
sр2- гибридизация
В
диеновых углеводородах
все четыре атома
углерода
сопряженной системы имеют sp2-гибридизацию
и лежат в одной плоскости. Четыре
р-электрона (по одному от каждого атома
углерода)
комбинируются, образуя четыре
-молекулярные
орбитали (две связывающих - занятые и
две разрыхляющих - свободные), из к-рых
только низшая делокализована по всем
атомам
углерода.
Частичная
делокализация -электронов
обусловливает эффект
сопряжения,
проявляющийся в уменьшении энергии
системы (на 13-17 кДж/моль
по сравнению с системой
изолированных
двойных
связей),
выравнивании межатомных расстояний:
двойные
связи
несколько длиннее (0,135 нм), а простые -
короче (0,146 нм), чем в молекулах
без сопряжения (соотв. 0,133 и 0,154 нм),
повышении поляризуемости,
экзальтации молекулярной
рефракции
и др. физ. эффектах.
Диеновые
углеводороды
существуют в виде двух конформаций,
переходящих друг в друга, причем
s-транс-форма более устойчива:
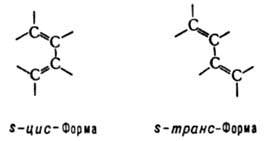
1. Получение бутадиена-1,3 по способу Лебедева.
Лебедев С В. синтезировал бутадиен-1,3 из этилового спирта с оксидными катализаторами, содержащими Zn, Mg, Al/
При этом протекают процессы дегидратации и дегидрирования спирта.
2СНз-СН2-ОН-------► СН2=СН-СН=СН2 + 2Н20 + Н2
Получение бутадиена-1,3 из бутана. Происходит постадийное дегидрирование в присутствии медно-хромовых катализаторов.
СН3-СН2-СН2-СНз---- ► СН2=СН-СН=СН2 + 2Н2
Получение изопрена (2-метилбутадиена-1,3). Современный способ заключается в дегидрировании З-метилбутена-1 с медно-хромовыми катализаторами:
Cat, 400 "С
сн3-снCH3 -сн=сн2 ► сн2=CCH3-сн=сн2 + н2
14. Алкадиены с сопряженными связями. Особенности их поведения в химических реакциях 1,4- и 1,2- присоединения.
Сопряжение - выравнивание, делокализация электронной плотности в молекуле с участием электронов п-связи
Сопряжение в алкадиенах наблюдается, когда две двойные связи разделены одной одинарной, как, например, в бутадиене- 1,3. При этом имеет место дополнительное перекрывание тт- орбиталей центральных углеродных атомов: 2-го и 3-го.
1 2 3 4
СН2—СН—СН—СН2
sр2- гибридизация
для алкадиенов характерны реакции электрофильного присоединения(АЕ)
галогенирование(1,2- и 1,4- присоединение). В зависимости от условий реакции могут быть два варианта:
1,2- присоединение, когда реагент присоединяется по одной из двух π-связей;
1,4-присоединение, когда реагент присоединяется по концам молекулы бутадиена; из двух тг-связей остается одна и перемещается в центр молекулы.
→CH2=CH-CH2 Br-CH12Br 1,2- ПРИСОЕДИНЕНИЕ(20%)
CH2=CH-CH=CH2 Br2→ →CH21Br-CH=CH-CH42Br 1,4 ПРИСОЕДИНЕНИЕ(80)
1,4-присоединение более характерно и подчеркивает наличие сопряжения и единой π-системы в диеновом фрагменте.
