
- •10. Реакции электрофильного присоединения в алкенах. Правило Марковникова с электронной точки зрения.
- •11. Рекция окисления, полимеризации алкенов. Использование продуктов полимеризации в ветеринарии, с/х( полипропилен, полиэтилен и др.).
- •13. Диеновые углеводороды с сопряженными связями. Строение. Дать понятие сопряжению. Способы получения.
- •14. Алкадиены с сопряженными связями. Особенности их поведения в химических реакциях 1,4- и 1,2- присоединения.
- •15. Строение тройной углерод-углеродной связи, ее реакционная способность
- •16. Гомологический ряд алкинов. Способы получения. Физические свойства. Физиологическое действие алкинов. Реакции замещения в Алкинах.
- •17. Взаимодействие алкинов с галогенами, водой, галогеноводородами. Использование продуктов реакции.
- •18. Бензол- ароматическая система. Дать понятия ароматичности. Ее влияние на реакционную способность соединения. Привести примеры ароматических соединений из других классов.
- •Число изомеров в ряду спиртов быстро растет: с5-восемь изомеров, с6- семнадцать, с10- пятьсот семь.
- •30. Реакционная способность глицерина. Применение продуктов реакции.
- •31. Простые и сложные эфиры на основе этанола. Их реакционная способность, практическое применение.
- •32. Способы получения фенолов, использование их в ветеринарии.
- •33. Реакционная способность фенола. Показать взаимное влияние гидроксильной группы и бензольного кольца на их реакционную способность.
- •34. Классификация альдегидов, кетонов. Номенклатура, изомерия. Физические свойства. Строение карбонильной группы. Реакционные центры.
- •35. Получение альдегидов и кетонов. Распространение в природе. Использование в ветеринарии и медицине.
- •36. Реакции замещения в альдегидах и кетонах по функциональной группе и по радикалу.
- •37. Реакции присоединения, идущие в альдегидах. Кетонах. Использование и распространение в природе продуктов реакции.
- •38. Получение полуацеталей (полукеталей). Значение этих реакций в химии углеводов.
- •39. Реакции полимеризации и конденсации альдегидов и кетонов. Их отличие.
- •64.Простые липиды(жиры). Классиф-я, распр-ние в природе,хим.Св-ва. Применение.
- •70. Аминоспирты. Строение. Распространение в природе. Холин. Коламин. Химические свойства.
- •71. Диамины. Путресцин. Кадаверин. Способы получения из аминокислот. Физ и хим свойства.
- •72. Анилин – ароматический амин. Физ и хим свойства. Использование производных анилина в ветеринарии, медицине. Сульфаниламидные препараты.
- •73. Амиды карбоновых кислот. Мочевина. Свойства, применение в сельском хозяйстве. Строение глутамина и аспарагина.
- •74. Аминокислоты. Строение. Биполярность аминокислот. Амфотерные свойства аминокислот. Строение и свойства глутамина и аспарагина. Электрофорез.
- •75. Химические свойства а-аминокислот. Реакции, идущие по nh2-группе.
- •76. Химические свойства аланина. Реакции, идущие по карбоксильной группе.
- •77. Отношение к нагреванию а,в,V аминокислот (дигидратация). Лактамы. Дикетопиперазины.
- •78. Белки. Общие представления о строении белков. Структурная организация белков. Денатурация.
- •79. Белки. Классификация. Протеины. Протеиды. Биологическая роль белков.
- •80. Пиридин как представитель шестичленных азотистых гетероциклов. Свойства. Биологически активные соединения на его основе. Никотиновая кислота.
- •81. Конденсированные азотистые гетероциклы. Индол и биологически активные соединения на его основе(триптофан, индолилуксусная кислота, триптамин).
- •82. Пиримидиновые азотистые основания и нуклеотиды на их основе.
- •83. Шестичленные азотистые гетероциклы с двумя гетероатомами. Пиримидин, цитозин, урацил, тимин.
- •84. Нуклеиновые кислоты. Нуклеозид, нуклеотид. Строение. Привести пример динуклеотида.
75. Химические свойства а-аминокислот. Реакции, идущие по nh2-группе.
Все входящие в состав живых организмов α-аминокислоты, кроме глицина, содержат асимметричный атом углерода (треонин и изолейцин содержат два асимметричных атома) и обладают оптической активностью. Почти все встречающиеся в природе α-аминокислоты имеют L-форму, и лишь L-аминокислоты включаются в состав белков, синтезируемых на рибосомах.
Данную особенность «живых» аминокислот весьма трудно объяснить, так как в реакциях между оптически неактивными веществами L и D-формы образуются в одинаковых количествах. Возможно, выбор одной из форм (L или D) — просто результат случайного стечения обстоятельств: первые молекулы, с которых смог начаться матричный синтез, обладали определенной формой, и именно к ним «приспособились» соответствующие ферменты.
Все аминокислоты амфотерные соединения, они могут проявлять как кислотные свойства, обусловленные наличием в их молекулах карбоксильной группы —COOH, так иосновные свойства, обусловленные аминогруппой —NH2. Аминокислоты взаимодействуют с кислотами и щелочами:
NH2 —CH2 —COOH + HCl → HCl • NH2 —CH2 —COOH (хлороводородная соль глицина)
NH2 —CH2 —COOH + NaOH → H2O + NH2 —CH2 —COONa (натриевая соль глицина)
Растворы аминокислот в воде благодаря этому обладают свойствами буферных растворов, т.е. находятся в состоянии внутренних солей.
NH2 —CH2COOH N+H3 —CH2COO-
Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов.
Этерификация:
NH2 —CH2 —COOH + CH3OH → H2O + NH2 —CH2 —COOCH3 (метиловый эфир глицина)
Важной особенностью аминокислот является их способность к поликонденсации, приводящей к образованию полиамидов, в том числе пептидов, белков, нейлона, капрона.
Реакция образования пептидов:
HOOC —CH2 —NH —H + HOOC —CH2 —NH2 → HOOC —CH2 —NH —CO —CH2 —NH2 + H2O
76. Химические свойства аланина. Реакции, идущие по карбоксильной группе.
Аланин (аминопропановая кислота) — алифатическая аминокислота. α-аланин входит в состав многих белков, β-аланин — в состав ряда биологически активных соединений.
Аланин легко превращается в печени в глюкозу и наоборот. Этот процесс носит название глюкозо-аланинового цикла и является одним из основных путей глюконеогенеза в печени.
взаимодействие с основаниями
NH2-C2H4-COOH + NaOH → NH2-C2H4-COONa + H2O
взаимодействие с кислотами
NH2-C2H4-COOH + HCl → HOOC-C2H4-NH2•HCl
взаимодействие со спиртами
NH2-C2H4-COOH + C2H5OH → NH2-C2H4-COО-С2Н5 + H2O реакция этерификации
образование пептидной связи
NH2-C2H4-COOH + NH2-C2H4-COOH → NH2-C2H4-CO-NH-C2H4-COOH + H2O

77. Отношение к нагреванию а,в,V аминокислот (дигидратация). Лактамы. Дикетопиперазины.
α-аминокислоты при нагревании димеризуются с образованием шестичленных циклических дикетопиперазинов
β-аминокислоты при нагревании отщепляют аммиак, превращаясь в α, β-непредельные кислоты, точнее, в их аммонийные соли
γ-аминокислоты претерпевают внутримолекулярную циклизацию,отщепляя молекулу воды с образованием внутреннего циклического амида (γ-лактама)
Лактам — циклический амид. Количество атомов в цикле может быть указано с помощью префиксов, например β-лактам (4-членный), γ-лактам (5-членный), δ-лактам (6-членный цикл). Также у многих лактамов есть исторически сложившиеся тривиальные названия, например γ-лактам — пирролидон, ε-лактам — капролактам.
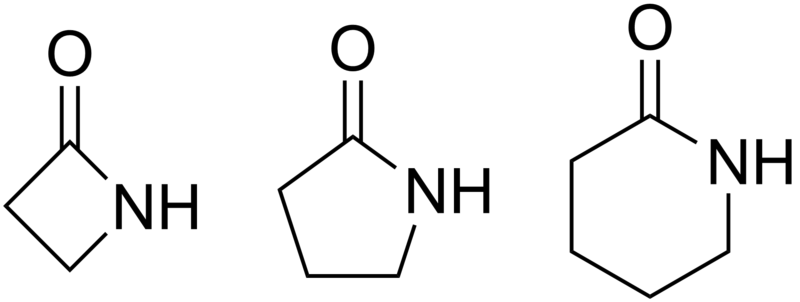
Слева направо: β-лактам, γ-лактам, δ-лактам
Дикетопиперазины, шестичленные
гетероциклические соединения, производные
пиперазина. Дикетопиперазины -
циклические ангидриды
a-аминокислот:
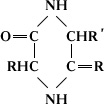 Дикетопиперазины -
бесцветные кристаллы; нейтральные
соединения, легко растворимые в горячей
воде, трудно - в холодной. При
гидролизе Дикетопиперазины образуются
дипептиды, затем аминокислоты; натрием в
спирте Дикетопиперазинывосстанавливаются
до пиперазинов.
Дикетопиперазины могут
быть получены циклизацией a-аминокислот
или их эфиров, а также выделены из
гидролизатов белков.
Дикетопиперазины -
бесцветные кристаллы; нейтральные
соединения, легко растворимые в горячей
воде, трудно - в холодной. При
гидролизе Дикетопиперазины образуются
дипептиды, затем аминокислоты; натрием в
спирте Дикетопиперазинывосстанавливаются
до пиперазинов.
Дикетопиперазины могут
быть получены циклизацией a-аминокислот
или их эфиров, а также выделены из
гидролизатов белков.
