
- •1. Цели и задачи изучаемой дисциплины.
- •2. Основные понятия и определения в области безопасности чрезвычайных ситуаций.
- •3. Опасности, характерные для Республики Беларусь.
- •4. Понятие чс, их особенности. Стадии развития чс.
- •5. Классификация чс.
- •6.Землетрясения Пожары.
- •7. Оползни, сели, лавины.
- •8.Наводнения. Ураганы
- •9. Микроорганизмы, их классификация.
- •10.Чс биологического характера. Понятие об инфекционном заболевании.
- •11.Профилактика инфекционных заболеваний
- •12.Характеристика химич соединений, используемых в рб
- •13.Классификация сдяв
- •14.Характеристика очага поражения сдяв. Оценка химической обстановки.
- •15.Особенности аварий и катастроф на транспорте.
- •16.Чс экологического характера, классификация
- •17.Ядерное оружие. Виды ядерных взрывов.
- •Поражающие факторы ядерного оружия. Очаг ядерного поражения и его характеристика.
- •Химическое оружие. Классификация и краткая характеристика ов.
- •Бактериологическое оружие.
- •21.Обычные средства поражения, их краткая хар.
- •22. Основные принципы и способы защиты населения.
- •23. Мероприятия пр и пх защиты. Режимы рад защиты.
- •24. Способы защиты населения при радиоактивном и химическом загрязнении местности.
- •25. Обеспеч населения и го средствами пр и пхз. Проведение эвакуационных мероприятий.
- •28А.Открытая травма. Первая помощь при ранах. Правила наложения кровоостанавливающего жгута и основы десмургии.
- •29.Закрытая травма. Первая помощь. Правила иммобилизации и транспортировки пострадавших.
- •30.Ожоги, обморожения, электротравма, утопление, тепловой и солнечный удар. Принципы оказания первой помощи.
- •31. Первая помощь при травмах головы, грудной клетки и живота.
- •32.Синдром длительного сдавливания, травматический шок. Оказание первой помощи.
- •33.Терминальные состояния. Оказание слр.
- •34.Первая помощь при лучевых поражениях.
- •35.Характеристика и классификация сиз.
- •36.Противогазы, защитные костюмы.
- •37.Медицинские средства индивидуальной защиты
- •38.Коллективные средства защиты. Убежища.
- •39.Пру и простейшие укрытия. Защитные свойства местности.
- •40.Понятие и принципы радиационной безопасности.
- •41.Пути обеспечения радиационной безопасности. Международные организации по защите от ионизирующих излучений
- •42. Строение атома и атомного ядра
- •43А. Явление радиоактивности. Виды превращения ядер изотопов
- •44. Понятие ионизирующих излучений. Характеристика электромагнитных ии
- •45. Корпускулярные ии, характеристика
- •46А. Единицы измерения радиоактивности и дозы излучений
- •47. Общая характеристика естественных источников излучения
- •48. Космическая радиация
- •49. Земная радиация
- •51.История использования ядерной энергии. Сравнение тепловой и ядерной энергетики.
42. Строение атома и атомного ядра
Атом состоит из ядра и окружающего его электронного "облака". Находящиеся в электронном облаке электроны несут отрицательный электрический заряд. Протоны, входящие в состав ядра, несут положительный заряд.
Кроме протонов, в состав ядра большинства атомов входят нейтроны, не несущие никакого заряда. Масса нейтрона практически не отличается от массы протона. Вместе протоны и нейтроны называются нуклонами (от латинского nucleus – ядро).
В любом атоме число протонов в ядре в точности равно числу электронов в электронном облаке, поэтому атом в целом – нейтральная частица, не несущая заряда.
Атом может потерять один или несколько электронов или наоборот – захватить чужые электроны. В этом случае атом приобретает положительный или отрицательный заряд и называется ионом.
Практически вся масса атома сосредоточена в его ядре, так как масса электрона составляет всего лишь 1/1836 часть массы протона. Плотность вещества в ядре фантастически велика – порядка 1013 - 1014 г/см3.
Электроны, протоны и нейтроны являются главными "строительными деталями" атомов и называются субатомными частицами.
Сумма тяжелых частиц (нейтронов и протонов) в ядре атома какого-либо элемента называется массовым числом и обозначается буквой А. Из названия этой величины видно, что она тесно связана с округленной до целого числа атомной массой элемента.
A = Z + N
Здесь A – массовое число атома (сумма протонов и нейтронов), Z – заряд ядра (число протонов в ядре), N – число нейтронов в ядре.
Природа устроена так, что один и тот же элемент может существовать в виде двух или нескольких изотопов. Изотопы отличаются друг от друга только числом нейтронов в ядре (числом N). Поскольку нейтроны практически не влияют на химические свойства элементов, все изотопы одного и того же элемента химически неотличимы.
Изотопами называются вещества, состоящие из атомов с одинаковым зарядом ядра (то есть с одинаковым числом протонов), но с разным числом нейтронов в ядре. Изотопы отличаются друг от друга только массовым числом. Все элементы состоят из одного или нескольких изотопов.
Электронные оболочки изотопов одинаковые, поэтому они имеют одинаковы химические свойства и располагаются в одной ячейке периодической системы Менделеева.
Например, изотопы водорода 11Н, 21Н, 31Н.
Неустойчивые изотопы, которые не могут существовать сколь угодно долго называются радионуклидами.
В настоящее время известно примерно 2000 изотопов 108 химических элементов.
Из них к естественным относятся все стабильные (их 280) и входящие в состав радиоактивных семейств(46). Остальные получены в результате ядерных реакций.
43А. Явление радиоактивности. Виды превращения ядер изотопов
Радиоактивность- самопроизвольное превращение неустойчивого 1 химического элемента в изотоп другого элемента, сопровождаемое испусканием элементарных частиц или ядер.
Радиоактивность:
Естественная
Искусственная
Было выяснено, что радиоактивные ядра могут испускать частицы трех видов: положительно и отрицательно заряженные и нейтральные. Эти три вида излучений были названы α-, β- и γ-излучениями. Эти три вида радиоактивных излучений сильно отличаются друг от друга по способности ионизировать атомы вещества и, следовательно, по проникающей способности. Наименьшей проникающей способностью обладает α-излучение. В воздухе при нормальных условиях α-лучи проходят путь в несколько сантиметров. β-лучи гораздо меньше поглощаются веществом. Они способны пройти через слой алюминия толщиной в несколько миллиметров. Наибольшей проникающей способностью обладают γ-лучи, способные проходить через слой свинца толщиной 5–10 см.
Исследования показали, что α-лучи представляют поток α-частиц – ядер гелия , β-лучи – это поток электронов, γ-лучи представляют собой коротковолновое электромагнитное излучение с чрезвычайно малой длиной волны λ < 10–10 м и вследствие этого – ярко выраженными корпускулярными свойствами, т. е. является потоком частиц – γ-квантов.
Альфа-распад. Альфа-распадом называется самопроизвольное превращение атомного ядра с числом протонов Z и нейтронов N в другое (дочернее) ядро, содержащее число протонов Z – 2 и нейтронов N – 2. AZX→A-4Z-2Y+42α(42He)
При этом испускается α-частица – ядро атома гелия . Примером такого процесса может служить α-распад радия: 22688Ra→22686+42He
Бета-распад.
При бета-распаде из ядра вылетает
электрон. Внутри ядер электроны
существовать не могут, они возникают
при β-распаде в результате превращения
нейтрона в протон. Этот процесс может
происходить не только внутри ядра, но
и со свободными нейтронами. Среднее
время жизни свободного нейтрона
составляет около 15 минут. При распаде
нейтрон
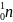 превращается в протон
превращается в протон
 и электрон
и электрон
 .
.
Измерения
показали, что в этом процессе наблюдается
кажущееся нарушение закона сохранения
энергии, так как суммарная энергия
протона и электрона, возникающих при
распаде нейтрона, меньше энергии
нейтрона. В 1931 году В. Паули высказал
предположение, что при распаде нейтрона
выделяется еще одна частица с нулевыми
значениями массы и заряда, которая
уносит с собой часть энергии. Новая
частица получила название нейтрино
(маленький нейтрон). Из-за отсутствия у
нейтрино заряда и массы эта частица
очень слабо взаимодействует с атомами
вещества, поэтому ее чрезвычайно трудно
обнаружить в эксперименте. В настоящее
время известно, что существует несколько
разновидностей нейтрино. В процессе
распада нейтрона возникает частица,
которая называется электронным
антинейтрино. Она обозначается символом
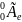 поэтому реакция распада нейтрона
записывается в виде
поэтому реакция распада нейтрона
записывается в виде
→ + + .
43 Б
Аналогичный процесс происходит и внутри ядер при β-распаде. Электрон, образующийся в результате распада одного из ядерных нейтронов, немедленно выбрасывается из «родительского дома» (ядра) с огромной скоростью, которая может отличаться от скорости света лишь на доли процента. Так как распределение энергии, выделяющейся при β-распаде, между электроном, нейтрино и дочерним ядром носит случайный характер, β-электроны могут иметь различные скорости в широком интервале значений.
При β-распаде зарядовое число Z увеличивается на единицу, а массовое число A остается неизменным. Дочернее ядро оказывается ядром одного из изотопов элемента, порядковый номер которого в таблице Менделеева на единицу превышает порядковый номер исходного ядра. Типичным примером β-распада может служить превращение изотона тория 23490Th , возникающего при α-распаде урана 23892U в палладий 23491Pa .
Наряду
с электронным β-распадом обнаружен так
называемый позитронный β+-распад,
при котором из ядра вылетают позитрон
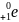 и нейтрино
и нейтрино
 .. Позитрон – это частица-двойник
электрона, отличающаяся от него только
знаком заряда. Существование позитрона
было предсказано выдающимся физиком
П. Дираком в 1928 г. Через несколько лет
позитрон был обнаружен в составе
космических лучей. Позитроны возникают
в результате реакции превращения протона
в нейтрон по следующей схеме:
.. Позитрон – это частица-двойник
электрона, отличающаяся от него только
знаком заряда. Существование позитрона
было предсказано выдающимся физиком
П. Дираком в 1928 г. Через несколько лет
позитрон был обнаружен в составе
космических лучей. Позитроны возникают
в результате реакции превращения протона
в нейтрон по следующей схеме:
→
+
 +
.
+
.
Также существует электронный захват(к-захват)
AZX+-1e0→AZ-1Y+V
Гамма-распад. В отличие от α- и β-радиоактивности, γ-радиоактивность ядер не связана с изменением внутренней структуры ядра и не сопровождается изменением зарядового или массового чисел. Как при α-, так и при β-распаде дочернее ядро может оказаться в некотором возбужденном состоянии и иметь избыток энергии. Переход ядра из возбужденного состояния в основное сопровождается испусканием одного или нескольких γ-квантов, энергия которых может достигать нескольких МэВ.
Радиоактивный распад- спонтанное изменение состава нестабильных атомных ядер путем испускания элементарных частиц или ядерных фрагментов.
ЗАКОН ЯДЕРНОГО РАСПАДА: за единицу времени распадается всегда одна и та же доля наличных (нераспавшихся) ядер данного элемента.
Активность радиоактивного элемента – число распадов в единицу времени.
