
- •Медична генетика (5 курс)
- •Завдання для самопідготовки і самокорекції вихідного рівня умінь
- •Основні теоретичні питання теми:
- •Короткі методичні вказівки до роботи на практичному занятті.
- •Технологічна карта проведення заняття
- •Граф логічної структури теми «Основи екологічної генетики, фармакогенетики»
- •Додаток 1. Екогенетичні патологічні реакції
- •Додаток 2. Фармакогенетика.
- •Приклади фармакогенетичних реакцій
- •Фармакогенетичні аспекти антикоагулянтної терапії
Технологічна карта проведення заняття
|
№ п/п |
Етап |
Час, хви-лини |
Навчальні посібники |
Місце проведення заняття |
|
|
Засоби навчання |
Обладнання |
||||
|
1. |
Визначення початкового рівня підготовки здатності визначення екогенетичних факторів, як причини вродженої патології |
15 |
Задачі |
|
Навчальна кімната |
|
2. |
Тематичний розбір сімей з обтяженим генетичним анамнезом, що планують дітонародження, а також пробандів з фармакогенетичними реакціями |
45 |
Генетичні карти, алгоритми обстеження сімей |
|
Навчальна кімната |
|
3. |
Підведення підсумків |
10 |
Задачі |
|
Навчальна кімната |
Граф логічної структури теми «Основи екологічної генетики, фармакогенетики»
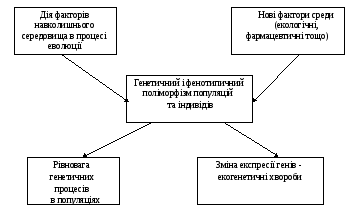
Важливість проблем екогенетікі людини та фармакогенетики з часом буде зростати відносно та абсолютно. По-перше, відносна значимість екогенетичної патології буде збільшуватися по мірі поліпшення медичної допомоги та боротьби із широко поширеними хворобами. Звичайні медичні заходи профілактики в даному випадку не будуть знижувати частоту екогенетичних хвороб. По-друге, в абсолютному вираженні можна очікувати збільшення екогенетічної патології з часом, оскільки внаслідок науково-технічного прогресу в середовищі існування людини будуть з'являтися все нові фактори, буде підвищуватися специфічність нових факторів виробництва і т.п.
Додаток 1. Екогенетичні патологічні реакції
Будь-який організм розвивається і існує в тісній взаємодії з навколишнім середовищем. Реакція людського організму на різні агенти навколишнього середовища є предметом екогенетики. Концепція екогенетики вперше була запропонована Брюером в 1971 р.
Екогенетика — розділ генетики, що вивчає вплив факторів середовища мешкання на спадковість.
Екогенетика вивчає 2 типи ефектів:
1) зміну прояву дії визначених алелей при впливі на організм специфічних факторів — екогенетичні синдроми;
2) зміну генетичного матеріалу під дією факторів зовнішнього середовища (індукований мутагенез).
Впродовж еволюції середовище мешкання людини поступово змінювалося. До цих змін організм пристосовувався за рахунок широкої норми реакції, з одного боку, і зміни генотипів в результаті мутацій і подальшого відбору, з іншого боку. В процесі еволюції виникла відносна відповідність умов середовища і видових характеристик людини.
У популяціях під впливом відбору сформувався широкий спадковий поліморфізм генів, що забезпечують взаємодію з середовищем. Не менше 25 % генів, що детермінують антигени, ферменти, рецептори, представлено поліморфними системами, які мають більш ніж 2 алелі. Багато які з них розповсюдились у певних популяціях через якусь селективну перевагу, інші — в результаті дрейфу генів. Частина з них не виявляється фенотипічно.
Сучасний період характеризується великим темпом і інтенсивністю зміни середовища мешкання. У навколишнє середовище надходить величезна кількість хімічних речовин, які входять до складу продуктів (смакові добавки, консерванти, барвники та ін.), предметів побутової хімії, є відходами виробництва. З багатьма з них людина в процесі еволюції не зустрічалася. У зв'язку з появою нових факторів середовища гени, які були такими, що «мовчать», у колишніх умовах, починають виявлятися фенотіпічно в нових умовах і піддаються дії природного відбору.
У деяких випадках ці реакції можуть бути патологічними і обумовлюють так звані екогенетичні хвороби. Екогенетичними патологічними реакціями, або екогенетичними хворобами називаються генетично обумовлені патологічні реакції на фактори навколишнього середовища (табл. 1.). Потенційно токсичні фактори навколишнього середовища діють не на все населення, а тільки на його частину, генетично схильну до такої дії.
Таблиця 1.
Приклади екогенетичних патологічних реакцій
|
Фактори зовнішнього середовища |
Генетична схильність |
Захворювання |
|
УФ-промені |
Дефекти ферментів репарації ДНК |
Рак шкіри |
|
Пил |
Дефіцит антитрипсину |
Емфізема легенів |
|
Харчові агенти |
|
|
|
Кінські боби |
Дефіцит Г6ФДГ |
Фавізм |
|
Сіль |
Дефект К-Nа насоса |
Гіпертонія |
|
Молоко |
Дефіцит лактази |
Непереносність лактози |
|
Жири |
Гіперхолестеринемія |
Атеросклероз |
|
Шоколад |
Зниження активності моно- |
Мігрень |
|
|
аміноксидази |
|
|
Алкоголь |
Атипова алкогольдегідро-геназа |
Алкоголізм |
Приклади екогенетичних патологічних реакцій
Недостатність α1-антитрипсину. Класичним прикладом екогенетичної реакції є реакція на забруднення атмосферного повітря при недостатності осі-антитрипсину, що є інгібітором протеїназ. При навіть незначних пошкодженнях легеневої тканини, виникаючих при курінні і вдиханні запорошеного повітря, протеолітичні ферменти починають руйнувати пошкоджені ділянки. У нормі одразу ж включається синтез інгібітора протеїназ, який нейтралізує дію протеолітичних ферментів і зупиняє руйнування легеневої тканини. При мутантному генотипі інгібітори протеїназ не синтезуються, протеолітичні ферменти повністю руйнують пошкоджені ділянки, що призводить до емфіземи легенів.
Локус сімейства генів антитрипсину представлений генами альфа-1-антитрипсину і альфа-1-антихімотрипсину (ААТ). Нині відомо більше 100 генних алель-них варіантів ААТ. Генетичні варіанти білка відрізняються за антитрипсиновою активністю, електрофоретичною рухливістю і, як правило, функціонально менш активні (алелі М, S,Z). Неактивність білка («нульовий алель») найчастіше обумовлена рецесивним алелем Z. У європейській популяції частота гомозигот за цим алелем становить 0,05 %, гетерозигот — 4,5 %. Рецесивні гомозиготи за цим алелем схильні до розвитку хронічних запальних процесів і емфіземи легенів (у 30 разів частіше, ніж у середньому в популяції). Гетерозиготи практично здорові, але при високому рівні забруднення вдихуваного повітря у них швидко розвиваються хронічні бронхо-легеневі і професійні захворювання. Аналіз системи антитрипсину рекомендований у хворих з хронічними обструктивними захворюваннями легенів, емфіземою, бронхіальною астмою, при професійних оглядах і відборах на роботу на відповідні виробництва.
Поліморфізм ферменту параоксанази. Екогенетичні реакції можуть бути пов'язані з особливостями метаболізму хімічних агентів, які надходять ззовні. Так, широко використовуваний інсектицид паратіонін перетворюється в печінці на параоксон, який далі окислюється параоксоназою сироватки. У європейців спостерігається чіткий розподіл на осіб з високим і низьким рівнем активності цього ферменту. Рецесивний алель, який кодує низьку активність ферменту, зустрічається в популяції з частотою 0,7. Гомозиготи за низькою активністю мають більш високий ризик отруїтися паратіоніном.
Екогенетичні патологічні реакції у носіїв генів цистинозу і анемії Фанконі. Гетерозиготні носії цистинозу і анемії Фанконі можуть бути схильні до токсичної дії металів (свинець, ртуть, кадмій). Підвищений, але такий, що не доходить до токсичного, рівень свинцю може бути причиною гіперреактивної поведінки у дітей із спадковою схильністю.
Поліморфізм генів метаболізму канцерогенів. Принципи екогенетики справедливі і для потенційно канцерогенних речовин. Канцерогенна дія хімічних агентів виявляється частіше у людей з певними особливостями метаболізму. Так, наприклад, полі-циклічні вуглеводні, яких багато в сигаретному димі, під дією ферменту арилгідроксилази перетворюються на більш канцерогенні активні епоксиди. До 30 % хворих з раком легенів належать до групи з високим вмістом ферменту (гомозиготи), тоді як у загальній популяції ця ознака зустрічається дуже рідко. Фермент GSТМ1 бере участь в кон'югації глутатіону з електрофільними сполуками , включаючи такий канцероген, як бензпирен. Нульовий алель глутатіон-S-трансферази (GSТМ1) асоціюється з підвищеною частотою аденокарциноми легенів.
Екогенетичні реакції на продукти харчування. Найяскравішим прикладом генетичних розбіжностей в реакції на харчові продукти є гіполактазія у дорослих. У всіх дітей в кишечнику є фермент лактаза, необхідний для всмоктування лактози. У більшості людей кишкова лактаза зникає після припинення харчування грудним молоком. Існує мутація, при якій здатність всмоктувати лактозу зберігається. Ця мутація має селективну перевагу в сільськогосподарських районах, де молоко є звичайним продуктом харчування (Центральна і Північна Європа, скотарські популяції Африки і Азії).
При вживанні в їжу молока або інших продуктів, які містять лактозу, люди не здатні до її засвоєння, страждають на метеоризм, кишкові розлади.
Мігрень може спричинятися "катехоламінами сиру у осіб із зниженою кон'югацією тираміну.
При низькій активності моноаміноксидази мігрень може провокувати шоколад.
Специфічна реакція на малі дози алкоголю у вигляді негайного почервоніння обличчя, тахікардії, печіння в шлунку, м'язової слабкості часто спостерігається у осіб в монголоїдних популяціях і пов'язана з відсутністю ізоформи-1 печінкового ферменту алко-гольдегідрогенази, що розщеплює спирт.
