
- •Конспект лекций по физике
- •Раздел 2 Молекулярная физика и термодинамика
- •Основы молекулярно-кинетической теории. Термодинамика
- •Основы молекулярно-кинетической теории. Основные положения молекулярно-кинетической теории. Сила и энергия взаимодействия молекул. Шкалы измерения температуры
- •Сила и энергия взаимодействия молекул
- •Контрольные вопросы:
- •Идеальный газ. Давление газа. Основное уравнение молекулярно-кинетической теории идеального газа
- •Контрольные вопросы:
- •Зависимость давления газа от температуры при постоянном объеме. Температура как мера средней кинетической энергии движения молекул
- •Связь между абсолютной температурой и кинетической энергией поступательного движения молекул
- •Контрольные вопросы:
- •Уравнение Клапейрона - Менделеева. Закон Дальтона
- •Количество молекул в 1 моле любого вещества одинаково и называется числом Авогадро:
- •2. 1 Моль любого газа при нормальных условиях занимает объём 22,4 дм3. (закон Авогадро).
- •Контрольные вопросы:
- •Изопроцессы и их графики
- •Контрольные вопросы:
- •Выберете правильный ответ на поставленный вопрос
- •Закон Максвелла о распределении молекул идеального газа по скорости и энергии теплового движения
- •Контрольные вопросы:
- •Барометрическая формула. Распределение Больцмана
- •Контрольные вопросы:
- •Реальные газы. Уравнение Ван-дер-Ваальса
- •Изотермы Ван-дер-Ваальса и их анализ. Критическое состояние вещества
- •Контрольные вопросы:
- •Среднее число столкновений и средняя длина свободного пробега молекул
- •Контрольные вопросы:
- •Выберите правильный ответ на поставленный вопрос
- •Основы термодинамики Число степеней свободы молекулы. Закон равномерного распределения энергии по степеням свободы
- •Изменение внутренней энергии тела в процессе теплообмена и совершения работы. Уравнение теплового баланса
- •Уравнение теплового баланса
- •Контрольные вопросы:
- •Первое начало термодинамики. Адиабатный процесс
- •Контрольные вопросы:
- •Выберите правильный ответ на поставленный вопрос
- •Работа газа. Круговой процесс. Кпд кругового процесса Работа газа при изменении объема
- •Контрольные вопросы:
- •Принцип действия тепловой машины. Цикл Карно
- •Кпд тепловой машины
- •Контрольные вопросы:
- •Необратимые процессы. Понятие о втором начале термодинамики
- •Контрольные вопросы:
- •Явления переноса в термодинамически неравновесных системах
- •Контрольные вопросы:
- •Выберите правильный ответ на поставленные вопросы:
- •Агрегатные состояния вещества и фазовые переходы
- •Свойства паров. Влажность воздуха. Способы определения влажности воздуха. Парообразование
- •Влажность воздуха. Точка росы. Способы определения влажности
- •Приборы для определения влажности воздуха
- •Контрольные вопросы:
- •Кипение.
- •Контрольные вопросы:
- •Характеристика жидкого состояния вещества.
- •Молекулярное давление поверхностного слоя жидкости
- •Энергия поверхностного слоя жидкости.
- •Поверхностное натяжение
- •Смачивание
- •Капиллярность
- •Контрольные вопросы:
- •Кристаллическое состояние вещества. Типы связей в кристаллах, виды кристаллических структур
- •Полиморфизм
- •Применение кристаллов
- •Жидкие кристаллы
- •Контрольные вопросы:
- •Механические свойства твердых тел
- •Закон Гука. Модуль упругости
- •Диаграмма растяжения твердого тела
- •Контрольные вопросы:
- •Тепловое расширение твердых тел.
- •Плавление и кристаллизация. Диаграмма фазовых состояний
- •Контрольные вопросы:
Капиллярность
Если в воду опустить тонкую стеклянную
трубку, то вода втягивается в трубку и
ее уровень поднимается на высоту
![]() .
.
Рисунок 29. Капиллярные сосуды в
смачивающей и не смачивающей жидкости
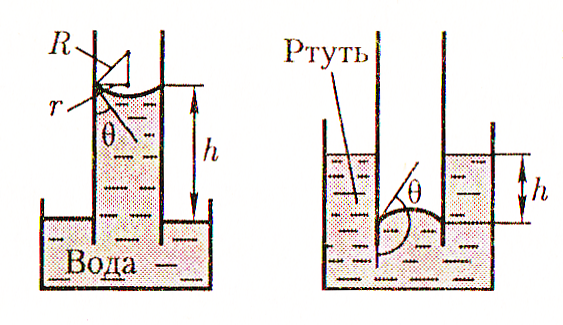
На очень большую высоту поднимается жидкость в трубке, диаметр которой меньше диаметра волоса. Такие трубки называют капиллярными трубками, от греческого “капиллярис” - волос, тонкий. Смачивающая жидкость поднимается по трубке вверх, а не смачивающая опускается вниз (рисунок 29). Это объясняется тем, что давление Лапласа РЛ в случае смачивающей жидкости направлено вверх. Оно втягивает воду до тех пор, пока гидростатическое давление РГ столба воды высотой h не уравновесит систему.
При этом
![]() ;
;
![]() ;
;
![]()
Отсюда:
Отсюда:
![]() и высота подъема жидкости
и высота подъема жидкости
![]() ,
где:
,
где:![]() =9,81
=9,81
![]() ,
а
,
а
![]() -
плотность жидкости.
-
плотность жидкости.
Высота подъема жидкости тем больше,
чем меньше радиус трубки
![]() .
.
Формула
![]() справедлива при краевом угле Θ=0. Если
Θ отличается от нуля, то
справедлива при краевом угле Θ=0. Если
Θ отличается от нуля, то
![]()
![]() .
.
Высота подъема жидкости h
в капилляре зависит от температуры. Чем
выше температура, тем меньше
![]() ,
а значит и h.
,
а значит и h.
Капиллярные явления играют большую роль в природе и технике. Мельчайшие капилляры имеются в растениях. По ним влага поднимается из почвы до вершины. В почве тоже есть капилляры, осушающие почву. В домах между фундаментом и стеной обязательно укладывают слой материала, не обладающего капиллярной структурой. Тогда вода из земли не попадает в стены здания.
Контрольные вопросы:
-
Дайте определение жидкого состояния вещества.
-
Расскажите о молекулярном давлении поверхностного слоя жидкости.
-
Расскажите об энергии поверхностного слоя жидкости. Что такое коэффициент поверхностного натяжения?
-
Что такое смачивающая и не смачивающая жидкость? Что служит мерой смачиваемости?
-
Что такое мениск и под действием какого давления он образуется?
-
Что такое капиллярная трубка и как вычислить высоту, на которую поднимается жидкость по капиллярной трубке?
Кристаллическое состояние вещества. Типы связей в кристаллах, виды кристаллических структур
Вещество называется твердым, если оно сохраняет объем и форму.
В физике твердыми телами называются только такие вещества, у которых имеется кристаллическое строение.
Многие твердые тела в природе имеют гладкие плоские поверхности, расположенные под определенными углами. Такие тела называют монокристаллами. Частицы в монокристаллах (атомы, молекулы или ионы) имеют правильное расположение, т.е. образуют пространственную кристаллическую решетку. Точки в кристаллической решетке, соответствующие наиболее устойчивому положению равновесия частиц твердого тела, называются узлами решетки. Узлы решетки имеют правильное расположение, которое периодически повторяется внутри кристалла. Правильное расположение частиц в узлах решетки кристалла называется дальним порядком в расположении частиц.
Дальний порядок является причиной анизотропии кристаллов – зависимости свойств кристаллов от направления. Очень сильно от направления зависит механическая прочность кристаллов.
Большинство твердых веществ имеет поликристаллическое строение, т.е. они состоят из множества очень мелких кристаллов (кристаллитов), расположенных хаотично. Поэтому тело в целом является изотропным, т.е. имеет одинаковые свойства по всем направлениям.
В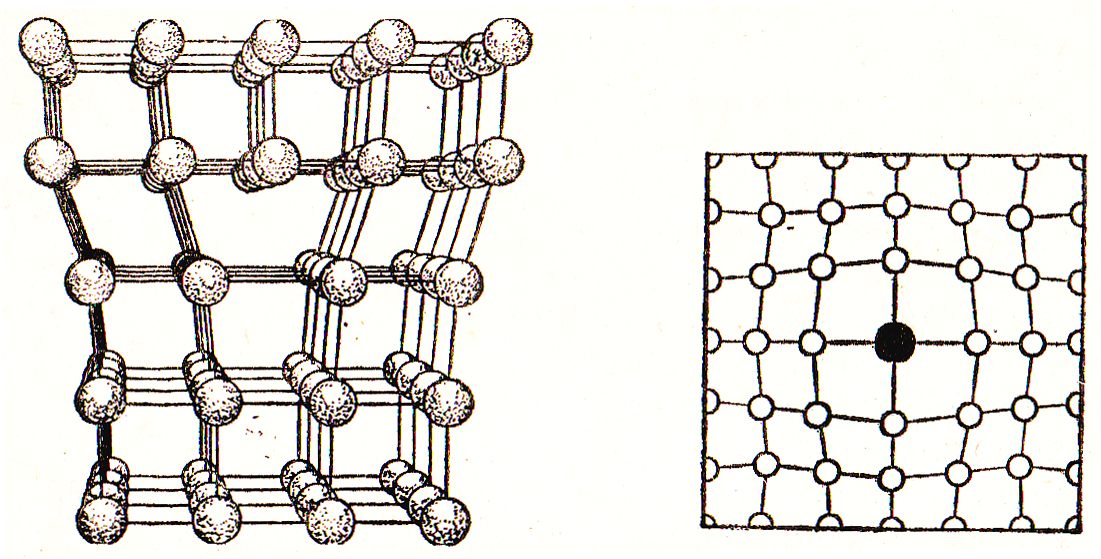 кристаллических веществах всегда
имеются дефекты (дислокации, трещины,
включения инородных атомов (рисунок
30) и т.д.)
кристаллических веществах всегда
имеются дефекты (дислокации, трещины,
включения инородных атомов (рисунок
30) и т.д.)
Дефекты влияют на физические свойства кристаллических веществ: прочность, электропроводность и т.п.
В
Дислокации Включение инородного атома
Рисунок 30. Дефекты кристаллической
решетки
Ионная кристаллическая структура характеризуется наличием положительных и отрицательных ионов в узлах решетки. Силами, удерживающими ионы в узлах, являются силы электрического притяжения и отталкивания между этими ионами. Эти силы относительно слабые. Расплавы и растворы таких веществ являются хорошими проводниками электрического тока. Примером могут служить кристаллы поваренной соли.
Атомная кристаллическая структура характеризуется наличием нейтральных атомов в узлах решетки, между которыми имеется ковалентная связь. При ковалентной связи каждые 2 атома удерживаются силами притяжения, возникающими при взаимном обмене двумя валентными электронами между этими атомами. Ковалентная связь создает весьма прочные кристаллы: алмаз, кварц.
Молекулярная кристаллическая структура характеризуется наличием в узлах решетки нейтральных молекул вещества. Силы, удерживающие молекулы в узлах решетки, являются силами межмолекулярного взаимодействия. Эти силы слабые. Примером может служить нафталин.
Металлическая кристаллическая структура отличается наличием в узлах решетки положительно заряженных ионов металла. Валентные электроны металлов слабо связаны с атомами. Эти электроны легко отрываются от атомов и образуют облака, перекрывающие сразу много атомов в кристаллической решетке. Они называются еще электронным газом, при расчетах которого можно использовать формулы для идеального газа. Электронный газ обуславливает высокую теплопроводность и электропроводность металлов. Отрицательно заряженный электронный газ удерживает ионы в узлах решетки и придает большую прочность металлу.
