
- •7) Теория электролитической диссоциации
- •9) Правила написания уравнений реакций в ионном виде
- •10) По химическим свойствам оксиды подразделяют на следующие типы:
- •13) Классификация и свойства солей
- •25) Серная кислота - h2so4
- •28) Оксиды азота
- •35) Основные положения теории химического строения а.М. Бутлерова
- •47) Получение предельных одноатомных спиртов
- •50) Альдегиды
- •52) Карбоновые кислоты
- •55) Сложные эфиры
- •57) Углеводы
50) Альдегиды
Альдегидами
называются органические соединения,
содержащие карбонильную группу, в
которой атом углерода связан с радикалом
и одним атомом водорода, то есть общая
формула альдегидов
![]() . Исключение составляет муравьиный
альдегид
. Исключение составляет муравьиный
альдегид
![]() , в котором, как видно, карбонильная
группа соединена с атомом Н.
, в котором, как видно, карбонильная
группа соединена с атомом Н.
Физические свойства
Простейший альдегид – муравьиный – газ с весьма резким запахом. Другие низшие альдегиды – жидкости, хорошо растворимые в воде. Альдегиды обладают удушливым запахом, который при многократном разведении становится приятным, напоминая запах плодов. Альдегиды кипят при более низкой температуре, чем спирты с тем же числом углеродных атомов. Это cвязано с отсутствием в альдегидах водородных связей. В то же время температура кипения альдегидов выше, чем у соответствующих по молекулярной массе углеводородов, что связано с высокой полярностью альдегидов.
Физические свойства некоторых альдегидов представлены в таблице.
Химические свойства
Альдегиды характеризуются высокой реакционной способностью. Большая часть их реакций обусловлена наличием карбонильной группы. Атом углерода в карбонильной группе находится в состоянии sp2 -гибридизации и образует три s- связи (одна из них – связь С–О), которые расположены в одной плоскости под углом 120° друг к другу.
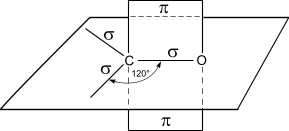
Схема строения карбонильной группы
Двойная связь карбонильной группы по физической природе сходна с двойной связью между углеродными атомами, т. е. это сочетание s- и p- связей, последняя из которых образована р- электронами атомов углерода и кислорода. Ввиду большей электроотрицательности атома кислорода по сравнению с атомом углерода, связь С=О сильно поляризована за счет смещения электронной плотности p- связи к атому кислорода, в результате чего на атоме кислорода возникает частичный отрицательный (d-), а на атоме углерода – частичный положительный (d+) заряды: .
![]()
Благодаря поляризации атом углерода карбонильной группы обладает электрофильными свойствами и способен реагировать с нуклеофильными реагентами. Важнейшими реакциями альдегидов являются реакции нуклеофильного присоединения по двойной связи карбонильной группы.
альдегиды способны вступать в реакции присоединения. Однако, им характерны только реакции гидрирования и гидратации.
СН3-СОН + Н2 → СН3-СН2-ОН
Реакция гидратации характерна преимущественно формальдегиду:
Н-СОН + Н2О → НО-СН-ОН - гидратная форма в растворе
Реакция серебряного зеркала".
CH3-COH + Ag2O → CH3-COOH + 2Ag↓
51) Метаналь HCOH (формальдегид, муравьиный альдегид) – бесцветный газ с резким запахом, хорошо растворим в воде, очень ядовит.
Применяется для производства фенолформальдегидных пластмасс и многих лекарственных препаратов, например уротропина.
40%-й раствор формальдегида – формалин, его используют для хранения биопрепаратов, протравливания семян перед посевом, дубления кож.
Получение
-
Основной способ получения формальдегида — окисление метанола:
2CH3OH + O2 → 2HCOH+ 2H2O
Окисление метанола в формальдегид проводится с использованием серебряного катализатора при температуре 650 °C и атмосферном давлении. Это хорошо освоенный технологический процесс, и 80 % формальдегида получается именно по этому методу.
-
Существует также промышленный способ получения формальдегида окислением метана:
CH4 + O2 → HCOH + H2O
Этаналь CH3COH (ацетальдегид, уксусный альдегид)- летучая жидкость, хорошо растворимая в воде, с характерным запахом. Основное количество получаемого в промышленности ацетальдегида используют для производства уксусной кислоты, а также различных пластмасс и ацетатного волокна. Уксусный альдегид ядовит!
Основной способ получения — окисление этилена
2 CH2=CH2 + O2 → 2 CH3CHO
Также получают уксусный альдегид гидратацией ацетилена в присутствии солей ртути (реакция Кучерова), с образованием менола, который изомеризуется в альдегид.
CH≡CH + H2O → CH3-CHO
Этот метод раньше доминировал до появления процесса окислением или дегидрированием этилового спирта, на медном или серебряном катализаторе.
t, Ag
CH3CH2OH → CH3CHO + H2
t, Ag
2 CH3CH2OH + O2→ 2 CH3CHO+2 H2O
В частности, ацетальдегид образуется в организме человека после принятия алкоголя. Им и обусловлен запах «перегара».
Получение
-
Р.Кучерова
Hg2+
C2H2 + H2O → CH3 – CОН
2) Окисление спиртов Сu, t
2 CH3 - CH2 – OH + O2 → 2 CH3 – CОН + 2 H2O
