
Предлучевой период:
1. Детальное обследование больного (клинические, лабораторные, рентгенологические исследования, УЗИ, КТ, МРТ и др.).
2. Определение гистологической формы заболевания (морфологическая или гистологическая верификация).
-
Определение показаний к лучевому лечению.
-
Исключение противопоказаний к лучевому лечению.
-
Выбор вида и метода лучевой терапии и дополнительных нелучевых лечебных мероприятий.
-
Определение топографо-анатомических взаимоотношений опухоли с окружающими здоровыми органами и тканями (топометрическая подготовка больного).
-
Выбор оптимальной разовой и суммарной доз облучения.
-
Выбор оптимального режима облучения (однократное, фракционированное, непрерывное).
-
Технология облучения.
-
Подготовка кожи к облучению, психологическая подготовка больного.
Лучевой период:
1. Проведение облучения по утвержденным протоколам.
2. Применение дополнительных методов лечения (радиомодифицирующая и сопровождающая терапия).
3 Уход за больными, при необходимости коррекция плана лечения.
4 Наблюдение за возможными местными лучевыми реакциями.
Послелучевой период:
1 Наблюдение за состоянием больных.
2 Оценка эффективности лечения.
3 Наблюдение за возможными местными лучевыми реакциями и повреждениями.
4 Диспансерное наблюдение за больным 2 раза в год. Если через 10 лет не возникает рецидив, пациента снимают с онкологического реестра.
При планировании облучения важно знать, какие ионизирующие излучения могут быть использованы. Таковыми могут быть: рентгеновское излучение, гамма-излучение, тормозное излучение высоких энергий, пучки электронов, поток тяжелых заряженных высокоэнергетических частиц, в частности протонов, и радиоизотопные источники бета-излучения.
Рентгеновское излучение, возникающее при анодном напряжении 200 кв, в значительной мере поглощается на поверхности тела человека. Итак, больше всего облучается кожа. При удалении от поверхности доза непрерывно уменьшается. Так, на глубине 10 см остается 20% дозы. При этом возникает рассеяние лучей, что приводит к облучению расположенных вокруг здоровых тканей. Рентгенотерапию преимущественно применяют при лечении опухолей с поверхностной локализацией. Толерантная доза для кожи (максимальная доза, которая не вызывает повреждений кожи больного) составляет 35 Гр.
Пучок гамма-лучей практически имеет однородный характер, максимум поглощения которого смещается на 0,5 см вглубь. На глубине 10 см остается 50% поверхностной дозы. Поэтому относительные глубинные дозы выше, чем при рентгеновском излучении. Применяется для лечения глубоко расположенных опухолей.
Использование тормозного излучения высоких энергий (25 МеВ), производится на линейных ускорителях, позволяет получить максимум поглощенной дозы на глубине 4-6 см от поверхности тела. Но существенным недостатком тормозного излучения является медленное уменьшение дозы после достижения ее максимума. Поэтому значительно облучаются ткани, расположенные за опухолью.
На линейных ускорителях образуется пучок электронов высокой энергии. При этом максимум поглощенной дозы достигается на глубине 1-3 см. Затем доза резко снижается. На глубине 10 см ткани практически не облучаются. Пучки электронов, получаемых на линейных ускорителях, используются для лечения опухолей, расположенных на глубине 1-3 см.
Протоны высокой энергии в тканях движутся прямолинейно и равномерно замедляют ход. При этом линейная потеря энергии возрастает, достигая максимума в конце пробега, и там же создается максимальная поглощенная доза. Поскольку протоны практически не рассеиваются в тканях, то облучение можно проводить узким пучком, что позволяет разрушать в теле человека участки объемом менее 1 кубического сантиметра.
Радионуклидные источники ионизирующих излучений - это источники излучений непрерывного действия, в которых содержится радиоактивное вещество.
В зависимости от технологического назначения различают закрытые и открытые источники ИИ
Закрытый источник ионизирующего излучения - это радионуклидный источник ионизирующего излучения, конструкция которого исключает попадание радиоактивного вещества (которое содержится в нем) во внешнюю среду (например, радиоактивные иглы, бусины, гамма-терапевтические аппараты для статического и динамического облучения).
Открытый источник ионизирующего излучения - это радионуклидный источник излучения, при использовании которого возможно попадание радиоактивного вещества во внешнюю среду (растворы и суспензии РФП).
Нерадионуклидный источники ионизирующих излучений - это технические устройства, которые не содержат в себе радиоактивных веществ, но при определенных условиях способны генерировать ионизирующее излучение за счет ускорения и торможения заряженных частиц. Это генераторы рентгеновского излучения (рентгеновские аппараты для близкодистанционной и дальнедистанционной рентгенотерапии), генераторы тормозного и корпускулярного излучений высоких энергий (линейные ускорители электронов, бетатроны, микротроны, синхрофазотроны, синхроциклотроны и др.).
В зависимости от пространственного расположения источника излучения по отношению к телу больного осуществляют внешнее облучение - со стороны кожи или внутреннее облучение - источник излучения располагают в теле больного. Для лучевой терапии используют закрытые (60Сo, 137Сs,252Сf, 192Іr и др..) и открытые (32Р, 99Sr-хлорид, 131І, 198Аu и др..) источники.
Для внешнего облучения используют закрытые источники излучений (чаще 60Сo) в гамма-терапевтических и хирургических аппаратах (АГАТ-Р, АГАТ-С, РОКУС, Терагам, Тератрон, COBALT60-F, гамма-нож) и электрофизические установки (рентгентерапевтические аппараты, линейные ускорители, кибер-нож и др.).
Г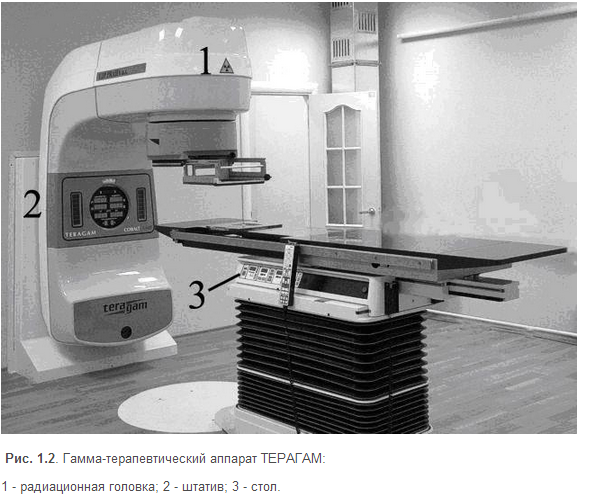 амма-установка
состоит из радиационной головки, штатива
и стола для размещения больного (рис.1.2).
В радиационной головке (рис.1.3) в защитном
свинцовом корпусе расположен источник 60Со
активностью 150-250 ТБк (в зависимости от
типа аппарата), с периодом полураспада
5,3 года.
амма-установка
состоит из радиационной головки, штатива
и стола для размещения больного (рис.1.2).
В радиационной головке (рис.1.3) в защитном
свинцовом корпусе расположен источник 60Со
активностью 150-250 ТБк (в зависимости от
типа аппарата), с периодом полураспада
5,3 года.
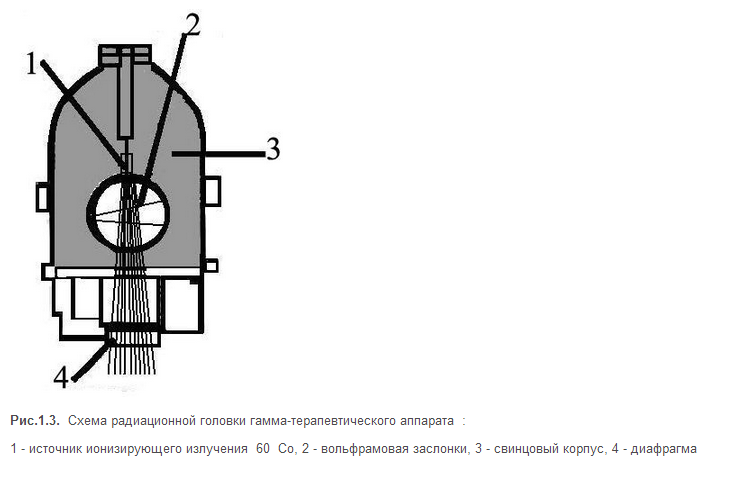
Выход пучка излучения возможен только через окно в корпусе головки, которое закрывается заслонками из вольфрама. Специальная конструкция аппаратов позволяет осуществлять статическое и динамическое облучение.
Электрофизические установки - это: генераторы рентгеновского излучения (рентгенотерапевтические установки), генераторы тормозного излучения высоких энергий, генераторы корпускулярных излучений высоких энергий (бетатроны, линейные ускорители электронов, синхрофазотроны, синхроциклотроны, циклотроны).
Ядерные реакторы малых размеров и циклотроны позволяют получить поток нейтронов, пригодный для проведения нейтронотерапии. Для внешнего облучения исп. медленные нейтроны с энергией 10-25 КеВ.
Для получения терапевтического эффекта необходимо предварительно насытить ткани, подлежащие облучению, элементами, легко захватывающими нейтроны, например, 10В (борнейтронзахватная терапия). При ядерной реакции, происходящей в результате захвата нейтронов атомами бора, выпускаются альфа-частицы, которые создают высокую плотность ионизации. Это дает возможность подвести к опухоли высокую дозу облучения.
Для внутреннего облучения используют открытые и закрытые источники ионизирующих излучений.
При планировании лучевой терапии очень важно выяснить топографическую анатомию участка, подлежащего облучению, то есть провести топометрию. Ее можно провести с помощью рентгенограмм в прямой и боковой проекциях или сонограмм. Но лучшими способами определения локализации опухоли является компьютерная томография и магнитно-резонансная томография. При этом, используя специальные программы, можно получить трехмерную картину дозного поля и имитацию дозиметрического плана лечения с суммарной погрешностью не более 5%.
Отношение дозы на заданной глубине к дозе в коже называют относительной или процентной глубинной дозой.
Распределение глубинной энергии различных видов излучений можно представить в виде кривых, в каждой точке которых один и тот же процент кожной дозы. Линии, соединяющие точки с одинаковым процентом глубинных доз, называют изодозными кривыми.
Изодозные кривые, нанесенные на прозрачную пленку (изодозные линейки), используют на практике для определения поглощенных глубинных доз в организме человека.
На изготовленном схематическом сечении тела больного с нанесенным на нем местоположением патологического очага лучевой терапевт вместе с физиком-дозиметристом планируют программу облучения, определяют объем зоны облучения.
Оптимальный объем облучения выбирают индивидуально для каждого больного. Необходимо выбрать наиболее рациональное распределение дозного поля, при котором бы доза равномерно распределялась в очаге поражения и распространялась на пути регионарного лимфотока.
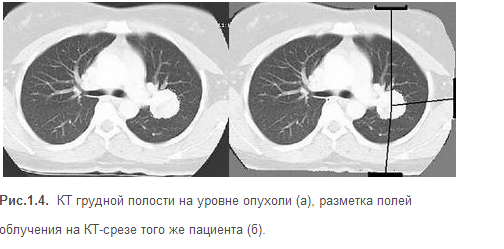
Затем выбирают вид излучения и метод облучения, размеры и форму полей облучения, направление пучков лучей и наносят их на топографо-анатомический эскиз. Топографо-анатомический эскиз в наше время выполняют на поперечном КТ или МРТ срезе (рис. 1.4, а) на уровне центра опухоли.
После нанесения полей облучения через центры намеченных полей проводят перпендикулярные линии, которые перекрещиваются в центре опухоли (рис. 1.4, б). В направлении центрального пучка лучей прикладывают изодозные линейки и определяют процентную глубинную дозу в очаге поражения с каждого поля облучения. Количество полей облучения определяют с учетом уровня толерантности облучаемых тканей.
При составлении плана лучевого лечения используют одну из известных типовых наиболее рациональных схем фракционирования, разработанных в клинической практике.
Схему фракционирования подбирают таким образом, чтобы суммарная поглощенная доза была достаточной для разрушения опухоли и одновременно была сохранена репарационная способность нормальных клеток.
Степень поражения нормальных тканей зависит от режима фракционирования, ритма облучения, размеров полей облучения, вида облучения, числа фракций, длительности лечения (в днях).
Величина дозы облучения, которую подводят к опухоли с каждого поля облучения, ограничивается толерантностью нормальных тканей.
Толерантная доза - это предельная доза ионизирующего излучения, которая не приводит к необратимым изменениям тканей.
В настоящее время есть томотерапевтические аппараты, которые сами определяют топографию опухоли и соответственно направляют на нее излучение.
С уществуют
стандартные
карты изодоз,
которые показывают распределение
поглощенной энергии в тканях при условии,
что пучок излучения падает на облученную
поверхность перпендикулярно к ней
(рис.1.5).
уществуют
стандартные
карты изодоз,
которые показывают распределение
поглощенной энергии в тканях при условии,
что пучок излучения падает на облученную
поверхность перпендикулярно к ней
(рис.1.5).
Рис. 1.5 . Распределение энергии различных видов излучений в тканях.
Проведение лучевой терапии, как правило, сопровождается теми или иными лучевыми реакциями.
Они бывают общими и местными. Их выраженность зависит от многих факторов. Среди них: интегральная поглощенная доза, ритм облучения, объем облучения (всего тела или какого-то одного места), локализация облучения.
Общие лучевые реакции проявляются различными нейроциркуляторными и гематологическими расстройствами. При этом может быть повышенная раздражительность, бессонница или сонливость, головокружение, расстройства деятельности сердечно-сосудистой и пищеварительной систем и др. Объективным критерием является снижение количества лейкоцитов в периферической крови.
С целью предупреждения или уменьшения выраженности общих реакций больным назначают питание, богатое витаминами, с достаточным количеством жидкости. Из медикаментозных средств показаны стимуляторы кроветворения, особенно лейкопоэза, препараты антитоксического и антигистаминного действия. Нередко больным во время курса лучевой терапии приходится переливать небольшие объемы крови или лейкоцитарной массы.
Из местных лучевых реакций, прежде всего, необходимо отметить изменения на коже и слизистых оболочках. На коже после облучения появляется покраснение (эритема) и сухой радиодерматит. Некоторое покраснение кожи проявляется уже в первые часы и дни после облучения вследствие вазомоторных расстройств. Стойкая эритема появляется через 1-2 недели после облучения и сопровождается небольшой болезненностью. После прекращения облучения эритема, как правило, уменьшается, появляется мелкое шелушение, а затем пигментация, которая может сохранятся длительное время. В ряде случаев при длительном и интенсивном облучении может развиться сухой радиодерматит, проявляющийся выраженной отечностью, яркой эритемой, истончением эпидермиса, который затем отторгается пластами. Кожа очень долго после лучевой терапии шелушится, сохраняется сухой и пигментированной.
При правильном проведении лучевой терапии мокнущий (влажный) радиодерматит, как правило, не развивается. Признаками его являются инфильтрация кожи, на которой появляются пузырьки с серозной жидкостью. Затем эпидермис отторгается и определяется мокнущая поверхность ярко розового цвета со скудным отделяемым. Она постепенно епителизуется, но кожа долго шелушится и остается неравномерно пигментированной.
Для уменьшения лучевых реакций поля облучения присыпают пудрой, а при появлении эритемы их смазывают рыбьим жиром или маслом облепихи, различными индифферентными маслами.
Слизистые оболочки на облучение отвечают покраснением и отечностью, которые усиливаются с ростом дозы. Слизистая оболочка становится мутной и уплотненной. Постепенно наступает десквамация эпителия, появляются единичные эрозии, покрытые пленкой - некротическим налетом. Это фаза пленочного радиоепителиита. Затем появляется эрозированная поверхность, покрытая белым фибринозным налетом, - фаза сливного пленочного эпителиита. Через 10-15 дней после прекращения лучевого лечения наступает эпителизация эрозий, после чего еще некоторое время наблюдается гиперемия и отечность слизистой оболочки.
В ряде случаев при облучении возникают признаки поражения внутренних органов. Так, при облучении глотки или пищевода может развиться дисфагия. При облучении гортани наблюдается охриплость. Слизистая оболочка тонкой кишки очень чувствительна к ионизирующим излучениям, поэтому облучение живота нередко сопровождаются тенезмами, частым жидким стулом со слизью. Облучение мочевого пузыря приводит к болезненному и частому мочеиспусканию.
Для предупреждения и лечения лучевых реакций слизистой оболочки запрещают употреблять раздражающую пищу, алкогольные напитки, курить. Полости промывают слабыми дезинфицирующими растворами и вводят в них витаминизированные масла. Попеременно проводят орошения с 1% раствором новокаина и 5-10% раствором димексида.
В ряде случаев лучевая терапия приводит к лучевым повреждениям, которые в отличие от лучевых реакций вызывают необратимые изменения в тканях организма пациента. Повреждения бывают ранние и поздние.
Ранние лучевые повреждения развиваются в процессе лечения или в течение 3 месяцев после окончания облучения.
Поздние лучевые повреждения возникают в любые сроки свыше 3 месяцев после завершения лучевой терапии. Нередко лучевые повреждения проявляются некрозом с последующим образованием язвы. Они отличаются стойкостью, и в некоторых случаях требуется хирургическое лечение с пересадкой кожи.
К лучевым повреждений также относятся лучевые склерозы, пневмониты, колиты, ректосигмоидиты, дистрофические изменения костей, индуративный отек, миелит, лучевой рак и др.
