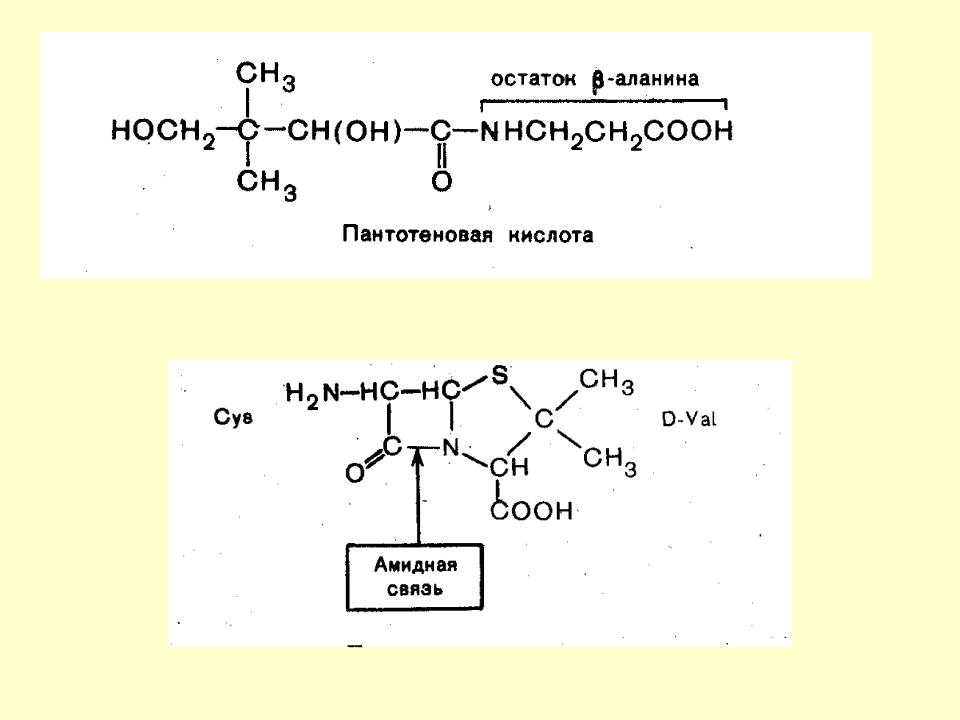
- ••АМИНОКИСЛОТЫ
- ••Классификация
- •Классификации аминокислот
- •CH2 CH COOH
- •По пищевой ценности для человека
- ••Изомерия
- •Стереохимия аминокислот
- •Стереохимия аминокислот
- •Стереохимия аминокислот
- •Физические и химические свойства
- •Физические и химические свойства
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- ••Взаимодействие по обеим группам – образование хелатных комплексов
- ••Реакции по аминогруппе
- ••Реакции по карбоксильной группе
- •• Поведение аминокислот при нагревании
- •-аминокислоты при нагревании отщепляют воду
- •- и -аминокислоты при нагревании отщепляют воду, циклизуются с образованием лактамов – циклических
- •Биологически важные химические реакции
- •КАЧЕСТВЕННЫЕ РЕАКЦИИ
- •КАЧЕСТВЕННЫЕ РЕАКЦИИ
- •КАЧЕСТВЕННЫЕ РЕАКЦИИ
- •ПЕПТИДЫ
- •пептиды
- •УЧАСТИЕ БЕЛКОВ В ПРОЦЕССАХ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- ••первичная структура –
- •Пептиды и белки
- •ВТОРИЧНАЯ СТРУКТУРА БЕЛКА
- •ВТОРИЧНАЯ СТРУКТУРА БЕЛКА
- •ВТОРИЧНАЯ СТРУКТУРА БЕЛКА
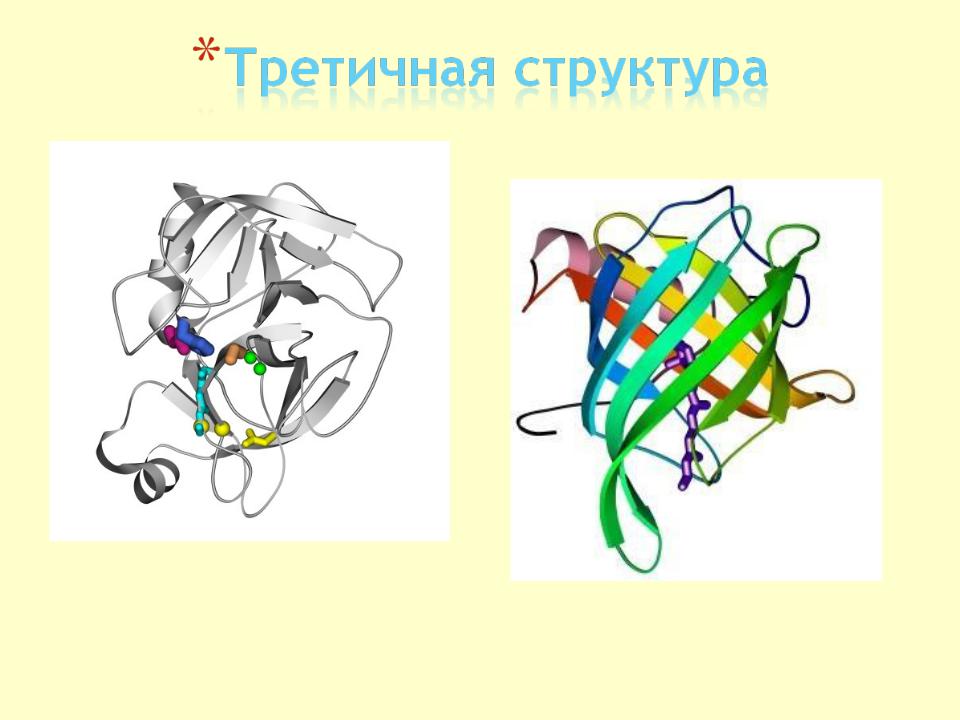
- •ТРЕТИЧНАЯ СТРУКТУРА БЕЛКА
- •Структура лизоцима.
- •Сериновая протеаза - трипсинРодопсин
- •ЧЕТВЕРТИЧНАЯ СТРУКТУРА БЕЛКА
- •Пептиды и белки
- •Пептиды и белки
- •Пептиды и белки
- •СЛОЖНЫЕ БЕЛКИ
- •NH2 CH2 CH2 CH2 COOH

Структура лизоцима.
Дисульфидные связи показаны пунктиром
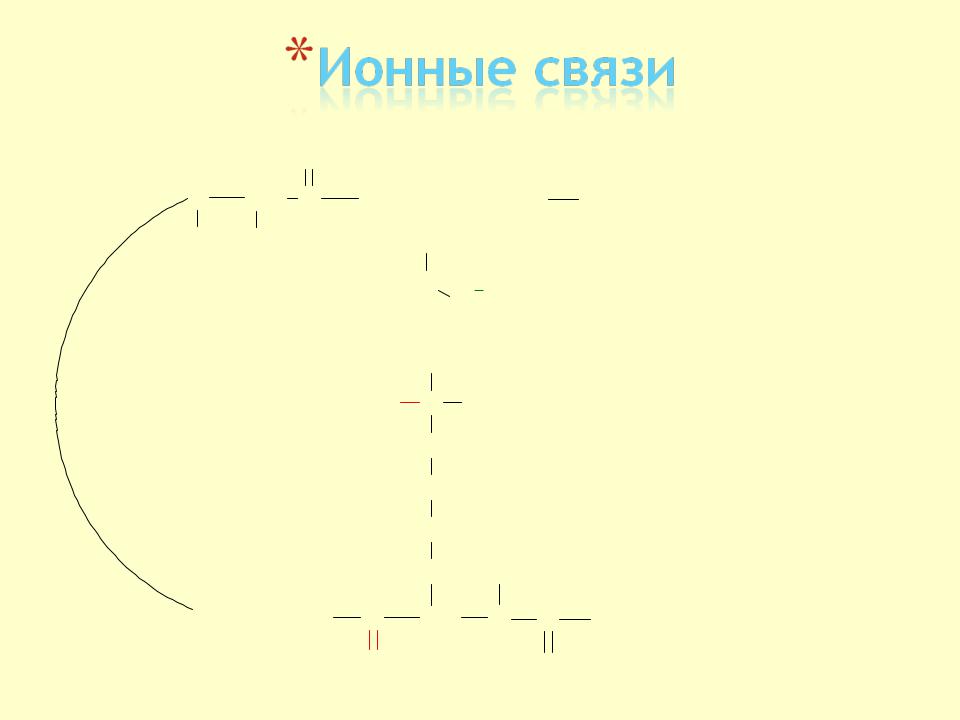
O N CH C
HR
Асп
Лиз
|
|
|
|
R |
|
H |
||
C |
|
|
|
|
||||
|
|
|
|
|
|
|||
|
CH |
|
N |
|||||
|
|
|||||||
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
||
|
|
|
|
|
|
O |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
CH |
|
C |
|
N |
|||||
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
CH2 |
|
H |
|||||||
O C O
C O
H
HN+ H
CH2 CH2 CH2
CH2 H
C |
CH N C |
O |
O |
|
|
|
O |
|
|
|
|
|
|
|
|
||
CH |
|
|
|
|
|
|
|
|
CH |
|
COOH |
||
|
C |
|
N |
|
|
||||||||
|
|
|
|||||||||||
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
H |
|
R |
|||||||||
R |
|
H |
|
|
|
|
|
R |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
N |
|
|
C |
|
CH |
|
NH2 |
||||
|
|
|
|
||||||||||
|
|
|
|
||||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
||
Сериновая протеаза - трипсинРодопсин

ЧЕТВЕРТИЧНАЯ СТРУКТУРА БЕЛКА
…ВЫСШИЙ УРОВЕНЬ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКА. ПОСТРОЕНЫ ИЗ АГРЕГАТОВ ИЛИ КОМПЛЕКСОВ (называемых также субъединицами). Каждая субъединица имеет свою первичную, вторичную
и третичную структуры. Но проявляется биологическая активность только в комплексе, т.е при наличии всех субъединиц.
БЕЛКИ: гемоглобин (4 субъединицы), глутамат дегидрогеназа (6 субъединиц), вирус табачной мозаики.
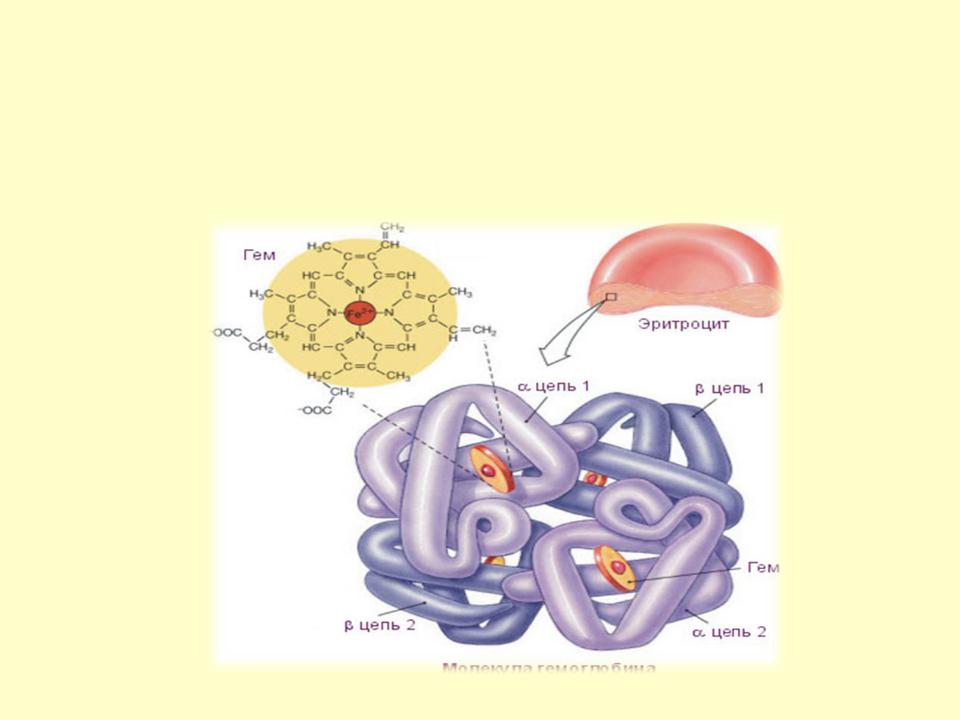
Пептиды и белки
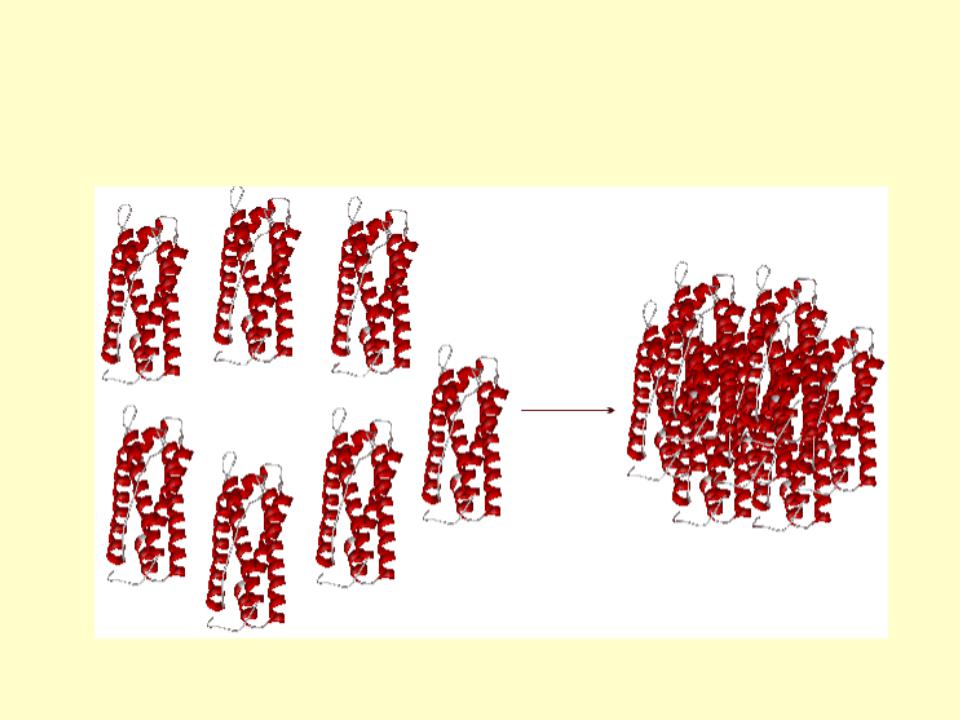
Четвертичная структура белков
ОБРАЗОВАНИЕ ЧЕТВЕРТИЧНОЙ СТРУКТУРЫ ГЛОБУЛЯРНОГО БЕЛКА ферритина при объединении молекул 47
в единый ансамбль
Пептиды и белки
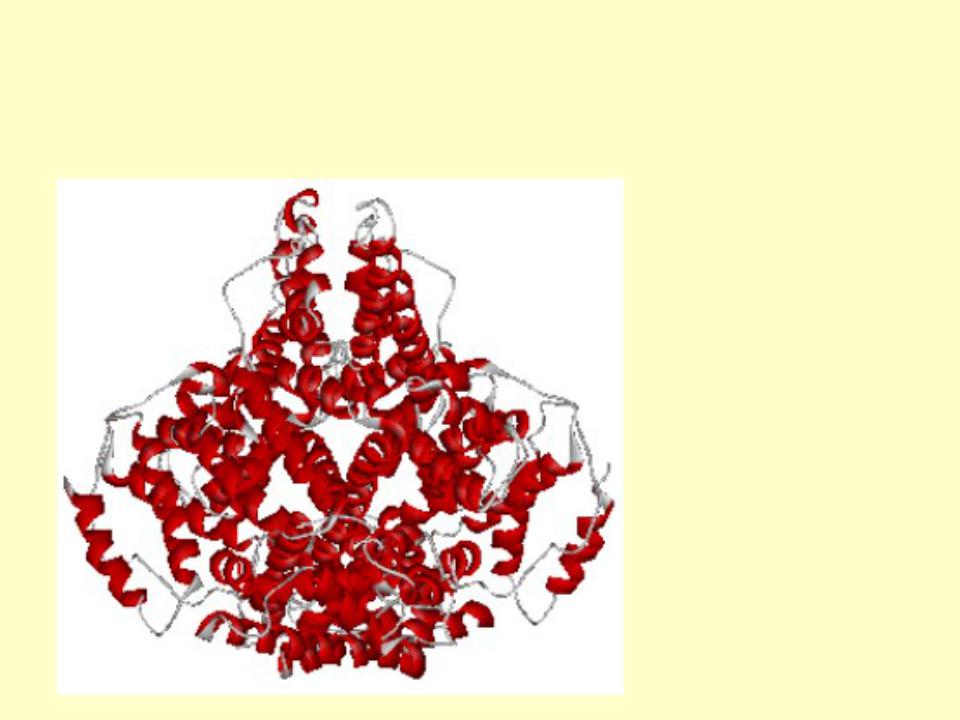
Глобулярные белки
ГЛОБУЛЯРНАЯ
СТРУКТУРА АЛЬБУМИНА (белок куриного яйца). В структуре помимо дисульфидных мостиков присутствуют свободные сульфгидридные HS- группы цистеина, которые в процессе разложения белка легко образуют сероводород – источник запаха тухлых яиц. Дисульфидные мостики намного 48 более устойчивы и при
Пептиды и белки
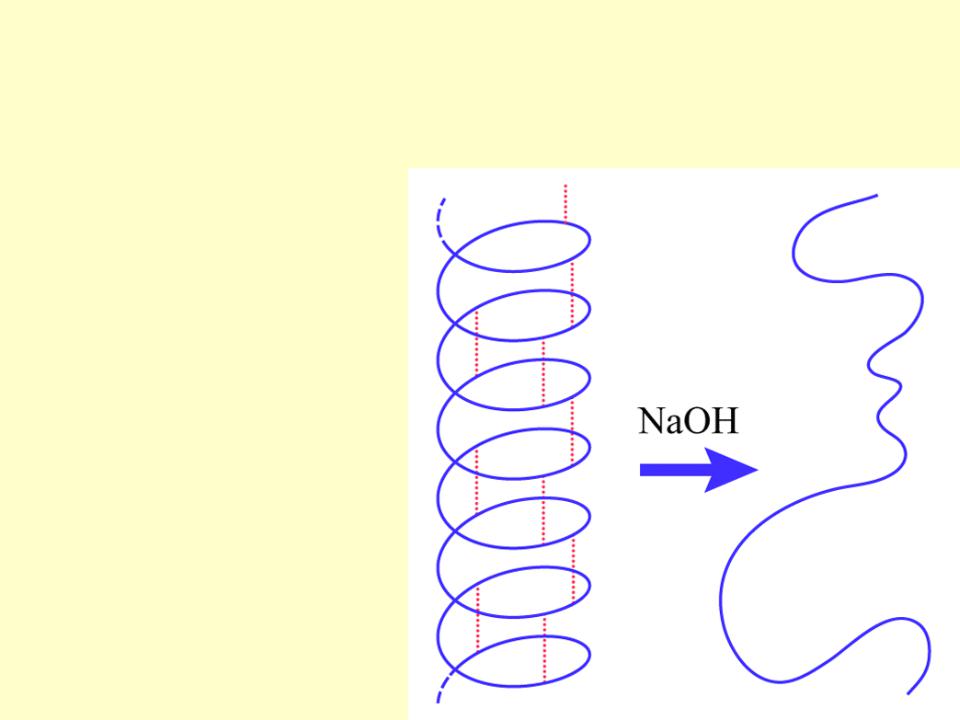
Денатурация белков
Денатурация белков
— это разрушение их
природной
(нативной)
пространственной
структуры с
сохранением
первичной
структуры

СЛОЖНЫЕ БЕЛКИ
НУКЛЕОПРОТЕИНЫ – смешанные биополимеры, включающие белки и нуклеиновые кислоты.
Примеры: рибосомы, вирусы растительные, животные, вирус табачной мозаики.
ПРОТЕОГЛИКАНЫ – углеводно- белковые биополимеры (гепарин, гепаринсульфат).
ГЛИКОПРОТЕИНЫ - углеводно- белковые биополимеры (иммуноглобулины, гормоны, группоспецифические вещества крови).
• ЛИПОПРОТЕИНЫ –липидно-белковые биополимеры (хиломикроны, α, β – липопротеины).
50