
Журнал неврологии и психиатрии / 2009 / NEV_2009_02_04
.pdf
ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
Коррекция нарушений ходьбы у пациентов с болезнью Паркинсона и сосудистым паркинсонизмом
Д.В. ПОХАБОВ, В.Г. АБРАМОВ, Ю.В. НЕСТЕРОВА
Rehabilitation of gait disorders in patients with Parkinson’s disease and vascular parkinsonism
D.V. POKHABOV, V.G. ABRAMOV, YU.V. NESTEROVA
Кафедра нервных болезней Красноярского государственного медицинского университета; Центр неврологии и нейрореабилитации
Енисейской клинической больницы, Красноярск
Обследованы 30 пациентов с болезнью Паркинсона и 30 с сосудистым паркинсонизмом. Получены результаты исследования ходьбы у здоровых лиц и больных. С учетом необходимости объективной оценки ходьбы и для решения диагностических и экспертных задач создан оригинальный программно-аппаратный компьютерный комплекс «Дорожка», позволяющий синхронизировать длину каждого шага и осуществлять динамическое наблюдение за больными при оценке эффективности реабилитации нарушений ходьбы. Благодаря введению авторского показателя — коэффициента вариабельности шага — установлены достоверные различия между группами больных, что важно в диагностическом плане. Разработан метод темпоритмовой коррекции ходьбы, основанный на синхронизации шага с темпом экзогенной звуковой стимуляции. Результатами исследования с применением комплекса «Дорожка» подтверждена эффективность метода темпоритмовой коррекции ходьбы в реабилитационном процессе без увеличения дозы леводопы и в плане улучшения качества жизни.
Ключевые слова: диагностика и реабилитация нарушений ходьбы при болезни Паркинсона и сосудистом паркинсонизме,
метод темпоритмовой коррекции ходьбы, программно-аппаратный компьютерный комплекс «Дорожка», коэффициент
вариабельности шага, качество жизни.
Thirty patients with Parkinson’s disease (PD) and 30 — with vascular parkinsonism (VP) have been studied. A soft-hardware- controlled complex “Dorozhka” elaborated previously by the authors was used to assess objectively the step length. The coefficient of step length variability (CSLV) which normal value is about 1 has been calculated. A method of tempo-rhythmic correction of gait including the synchronization of step with the rate of individually tailored exogenic sound stimulation has been applied. The dose of antiparkinsonian drugs was not changed during the rehabilitation. The decrease of mean step length and CSLV in patients with PD and VP was found. There were differential-diagnostic differences between individual gait profiles of PD and VP patients: patients with PD had the relatively even decrease of the length of all steps and in patients with VP the initiation of gait with the following increase of step length was affected. The significant increase of step length and CSLV (p<0,01), improvement on GABS and PDQ-39 scales were observed during and after the tempo-rhythmic correction of gait. The improvement of gait was correlated mostly with the increase of CSLV (two-fold in PD and 3-fold in VP). Therefore, the assessment of step variability allows to objectively differentiate the gait in patients with PD and VP and the method of tempo-rhythmic correction of gait with sound stimulation allows to improve significantly parameters of gait and patient’s quality of life without changing the dose of antiparkinsonian drugs.
Key words: Parkinson’s disease, vascular parkinsonism, gait disturbances, coefficient of step length variability, tempo-rhythmic correction.
Паркинсонизм различного генеза в силу высокой распространенности является предметом многочисленных эпидемиологических исследований [8]. Разброс показателей его распространенности, по данным различных исследований [8, 20], достаточно велик — от 384 случаев на 100 000 населения до 15% у лиц старше 65 лет.
На долю болезни Паркинсона (БП) приходится около 80% случаев синдрома паркинсонизма, который в сочета-
© Коллектив авторов, 2009
Zh Nevrol Psikhiatr Im SS Korsakova 2009;109:2:20
нии с другими синдромами может отмечаться и при других заболеваниях [3, 5, 8]. БП встречается повсеместно, ее частота варьирует от 100 до 250 случаев на 100 000 населения, заметно увеличиваясь с возрастом, достигая 1700 случаев на 100 000 населения старше 65 лет [20]. В 2007 г. в мире насчитывалось 6,3 млн человек с диагнозом БП, где 1 из 10 пациентов был моложе 50 лет.
Одним из наиболее значимых двигательных нарушений у больных БП является нарушение ходьбы, которое в значительной степени определяет тяжесть состояния и качество жизни больного. Авторы многочисленных исследований, проведенных за последние годы, приходят к выводу, что нарушение ходьбы служит самостоятельным
20 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 2, 2009 |

КОРРЕКЦИЯ НАРУШЕНИЙ ХОДЬБЫ
проявлением БП, которое имеет особый патогенез, требует специфического подхода в лечении и, по-видимому, может считаться пятым кардинальным признаком БП наряду с гипокинезией, ригидностью, тремором покоя и постуральными расстройствами [1, 6, 9].
Цереброваскулярные заболевания (ЦВЗ), по данным многочисленных исследований [5, 8, 20], являются причиной от 1 до 15% случаев развития паркинсонизма. В отечественной неврологии сложилась тенденция к гипердиагностике сосудистого паркинсонизма (СП), связанная с нечеткостью клинических критериев диагностики с переоценкой диагностической значимости сосудистых факторов риска, часто встречающихся у пожилых пациентов.
Клиническими проявлениями СП являются отсутствие тремора покоя, преобладание симптомов в нижних конечностях — паркинсонизм нижней части тела, раннее развитие нарушений ходьбы и постуральных нарушений, двустороннее начало заболевания, низкая эффективность дофаминергических средств [2, 4, 7, 17].
Походка при СП очень похожа на таковую при БП, однако при СП в большей степени страдает инициация ходьбы, отсутствует «семенящая» походка, отмечается большая вариабельность шага, особенно когда пациент выходит на ровную, широкую, без препятствий поверхность [2, 4, 7, 17].
Применяемые сегодня критерии клинической диагностики нарушений ходьбы при БП и СП во многом описательны и не несут объективной оценки, подкрепленной использованием медицинской техники при рассмотрении данной патологии, что в свою очередь обусловливает недостаток научной информации по этому вопросу [17].
Актуальность изучения особенностей феноменологии
ипатогенеза нарушений ходьбы при БП, СП и других заболеваниях, приводящих к изменению походки, стимулирует исследователей к созданию и совершенствованию инструментальных методов объективизации ходьбы, что помогает в диагностике данных нарушений, оценке динамики изменений походки при длительном наблюдении за больными, подборе медикаментозной и немедикаментозной терапии [4, 17].
Очень важный в практическом отношении вопрос немедикаментозной коррекции нарушений ходьбы при БП
иСП остается нерешенным, что связано с недостатком знаний о патогенезе и нейрохимическом субстрате изменений походки при БП и СП [6].
Так, на ранних стадиях БП могут быть эффективны различные противопаркинсонические средства вследствие того, что на данном этапе нарушения ходьбы преимущественно обусловлены ригидностью и гипокинезией [1, 2, 4, 6, 7, 17]. Однако по мере прогрессирования заболевания нарушения ходьбы в большей степени становятся обусловлены постуральными расстройствами. При этом ни один из противопаркинсонических препаратов не имеет достоверного влияния на данную симптоматику [10]. Что касается СП, то здесь ситуация осложняется еще и неэффективностью леводопы в большинстве случаев [2, 4, 7]. Неудовлетворенность традиционными методами лечения паркинсонизма, основывающихся, преимущественно, на возможностях фармакотерапии и пассивной позиции больных, требует применения новых подходов в лечении [10, 17].
Разрабатываемые методы нелекарственного лечения БП (пересадка эмбриональных тканей, электродов в экс-
трапирамидные структуры головного мозга, фототерапия, депривация сна и др.) при несомненных достоинствах имеют ряд недостатков — высокую стоимость, сложность выполнения, небезопасность, значимый процент рецидивов [11]. Используемые в последние годы зарубежными исследователями [15, 19] методы коррекции ходьбы для больных с БП и СП, построенные на использовании внешних аудиовизуальных стимулов, не учитывают индивидуальные особенности пациентов и не адаптированы к повседневной жизни.
Актуальность проблемы, несомненно, возрастает в связи с тенденцией к увеличению доли лиц пожилого возраста и, следовательно, распространенности БП, СП и других нейрогериатрических заболеваний [20]. Вместе с тем указанные заболевания часто поражают и людей трудоспособного возраста, что также определяет большую медико-социальную значимость проблемы паркинсонизма [14].
Таким образом, в настоящее время существует объективная необходимость как в комплексном инструментальном исследовании нарушений ходьбы при БП и СП для определения дифференциально-диагностических критериев, оценки влияния проводимой терапии, так и в разработке немедикаментозных методов коррекции нарушений ходьбы, учитывающих индивидуальные особенности походки пациентов и адаптированных к повседневной жизни.
Цель исследования заключалась в установлении особенностей феноменологии ходьбы при БП и СП на основании объективных параметров исследования походки, полученных с помощью созданного нами Устройства для определения шагоскоростных характеристик человека, называемого также программно-аппаратный комплекс «Дорожка»1, и определении эффективности разработанного нами метода темпоритмовой коррекции (ТРК)2 в коррекции нарушений ходьбы у больных с БП и СП.
Материал и методы
Обследовали две группы больных: 1-я группа включала 30 больных (18 мужчин и 12 женщин) БП II—III стадии по Хену и Яру, в возрасте от 55 до 75 лет (средний — 62,0±5,8 года); во 2-ю группу вошли 30 больных (16 мужчин и 14 женщин) СП, в возрасте от 57 до 74 лет (средний
— 70,0±4,6 года).
Совместно с окружной клинической больницей Горнохимического комбината г. Железногорска для объективизации длины шага был создан компьютерный программно-аппаратный комплекс «Дорожка»: контактная дорожка длиной 10 м с электрическими датчиками, реагирующими на замыкание специальным контактом — самоклеющимся диском из алюминиевой фольги диаметром 5 мм. В симметричные точки стопы прикрепляется по одному датчику. При ходьбе происходит замыкание контактов, соответствующая информация поступает в блок преобразования полученных данных при помощи стандартной лабораторной платы PC-LabCard; программ-
1 Патент на изобретение №2321345, зарегистрирован в Государственном реестре изобретений РФ 10 апреля 2008 г.
2 Патент на изобретение №2281695, зарегистрирован в Государственном реестре изобретений РФ 20 августа 2006 г.
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 2, 2009 |
21 |

ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
ное обеспечение данной установки позволяет анализировать длину каждого шага, а также сохранять и статистически обрабатывать полученные данные. К достоинствам установки следует отнести, во-первых, использование обследуемым привычной обуви и отсутствие влияния на походку контакта ввиду его незначительного веса и размера; во-вторых, быстроту получения и удобство сохранения полученных данных.
Известно, что ходьба человека в норме в стереотипных условиях достаточно стандартна по временнопространственным характеристикам, что позволяет снизить дополнительные энергетические затраты на преодоление неравномерных ускорений, инерции и т.д., которые возникают при высокой вариабельности ходьбы по темпу, ритму, длине шага. В связи с этим нами анализировался коэффициент вариабельности шага (КВШ), вычисляемый по формуле:
КВШ = (максимальная длина шага – минимальная длина шага) .
средняя длина шага
КВШ, по нашим данным, в значительной степени отражает степень нарушения ходьбы [12, 13].
Сравнительную оценку степени нарушений ходьбы в группах больных с БП и СП и эффективности проводимой терапии мы проводили с помощью специальных шкал и опросников.
Шкала нарушений ходьбы и равновесия (Gait and Balance Scale, GABS) — набор объективных тестов, которые проводятся наблюдателем и количественно оценивают выраженность нарушений передвижения у пациентов [18]. Отдельные пункты шкалы посвящены ходьбе, общей оценке независимости пациента от посторонней помощи, постуральной устойчивости, феномену застываний, содружественной работе рук. Изучение этих показателей в целом значительно усложнило бы статистическую обработку, поэтому в рамках нашего исследования проводилось изучение только пунктов 2, 3, 15—17.
С целью определения влияния нарушений походки и динамики ее восстановления на качество жизни больных с БП и СП мы использовали опросник PDQ-39 [16]. Поскольку прямое отношение к ходьбе имеют только пункты 4—8 данного опросника, то соответственно анализировались только они.
Разработанный нами метод ТРК заключается в синхронизации шага больного с темпом индивидуально подобранной экзогенной звуковой стимуляции [12]. Ходьбу пациента последовательно анализировали при различной частоте сигнала. Оптимальным считался ритм, при котором в большей степени улучшалась моторная функция пациента (увеличение длины шага при уменьшении количества шагов и комфортном самочувствии пациента). Таким образом, во время синхронизированной с темпом звуковой стимуляции ходьбы у пациентов изменялся двигательный стереотип. Эти положительные изменения двигательного стереотипа при самостоятельной ходьбе в произвольном темпе без подкрепления звукового сигнала с течением времени уменьшаются. С целью закрепления эффекта курса реабилитации каждому пациенту выдавали аудиокассету с записью индивидуального ритма звуковой стимуляции, которую он мог использовать при ходьбе (в том числе в быту, на улице и т.д.), прибегая к помощи портативного аудиоплеера и мини-наушников. Метод показал высокую эффективность при работе с больными и позволил значительному
количеству пациентов улучшить навыки ходьбы без увеличения дозы леводопы и даже уменьшить дозу препаратов на 10—15% [11, 12]. Проблема широкого внедрения данного метода без использования созданного нами устройства заключается в значительной трудоемкости определения оптимальной частоты стимуляции вручную и необходимости динамической коррекции реабилитационных программ, поскольку требует проведения регулярного тестирования пациентов.
Исследование для всех групп вначале проводили в режиме свободного темпа, соответствующего обычному режиму ходьбы испытуемого. Затем больных подвергали тестированию для подбора индивидуальной частоты стимуляции: пациенту предлагалось пройти под задаваемую звуком частоту в диапазоне от 40 до 120 сигналов в минуту (каждое последующее прохождение с увеличением частоты на 5 сигналов в минуту), синхронизируя свою ходьбу со звуковым сигналом. Во время каждого прохождения инструментально исследовали параметры длины шага и КВШ, рассматривали изменения двигательного стереотипа, субъективно оценивали самочувствие больного. Также учитывали частоту сердечных сокращений и показатели артериального давления больного с точки зрения адекватности физической нагрузки. Оптимальным считали ритм, при котором была наибольшая длина шага при меньшем количестве шагов и комфортном самочувствии больного. В ходе курса реабилитации ежедневно 5—6 раз в день по 5—20 мин в зависимости от состояния больного проводили индивидуальные занятия по восстановлению навыков ходьбы с синхронизацией шага с оптимальной частотой. По окончании курса реабилитации проводили повторное исследование длины шага и КВШ в режиме свободного темпа. На протяжении исследования дозы, принимаемые больными антипаркинсонических препаратов, не менялись.
Статистическую обработку полученных результатов осуществляли при помощи программы Statistica 6.0.
Результаты и обсуждение
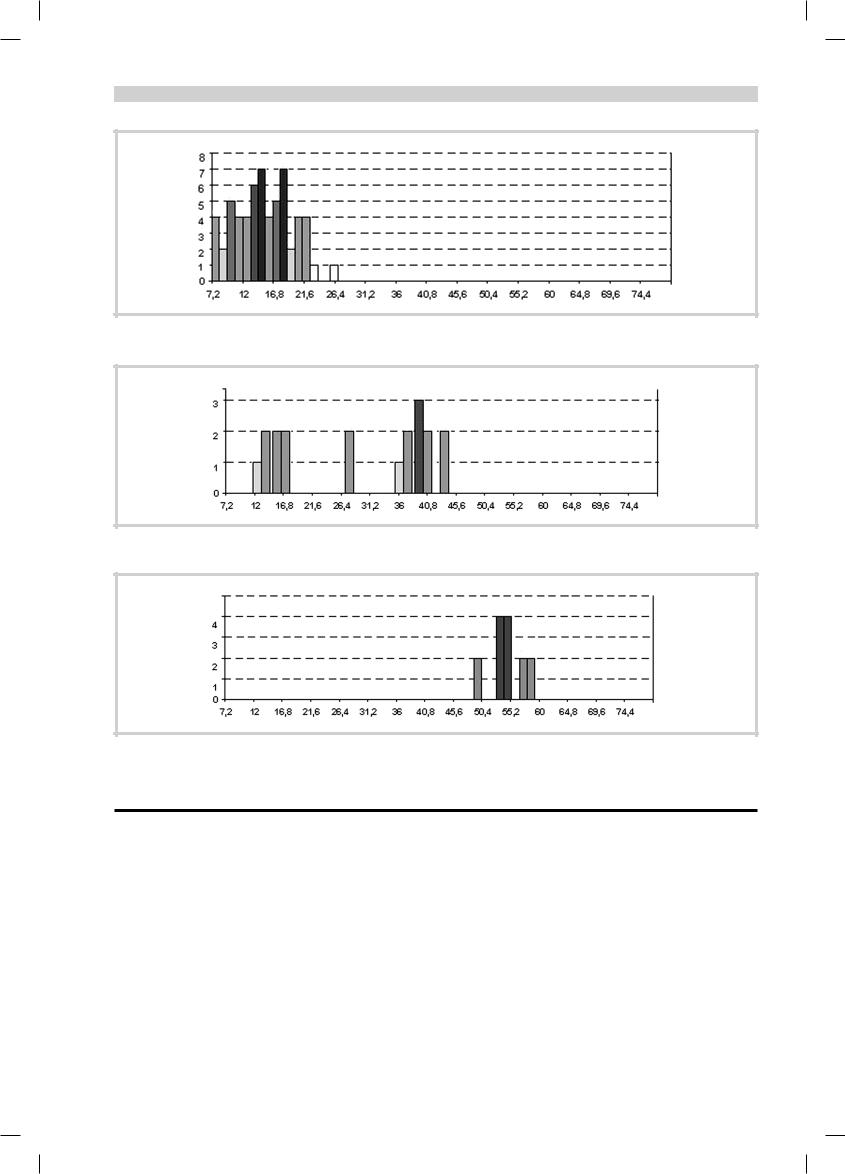
Типичные индивидуальные графики полученных результатов для каждой из групп отражены на рис. 1 (для пациентов с БП) и рис. 2 (для пациентов с СП). Для сравнения на рис. 3 представлены результаты исследования ходьбы у здоровых лиц пожилого возраста.
Из представленных графиков видно, что для больных БП и синдромом паркинсонизма характерно уменьшение средней длины шага и увеличение вариабельности его длины. Для больных БП характерно «топтание на месте» и относительно равномерное снижение длины всех шагов, что хорошо видно на рис. 1. У больных СП преимущественно страдает инициация ходьбы с наибольшим уменьшением длины первых шагов — порядка 12—14 см, с дальнейшим расхаживанием и значительным нарастанием длины шага, практически до нормальной длины. Полученные данные представлены в табл. 1.
При анализе результатов реабилитации нарушений ходьбы больных БП и СП обнаруживается объективное изменение в сторону увеличения длины шага как непосредственного в ходе занятия, так и в режиме свободного темпа, по окончании курса реабилитации.
Прирост длины шага у ряда пациентов составлял порядка 25—60%, что в первую очередь касалось пациентов с
22 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 2, 2009 |
КОРРЕКЦИЯ НАРУШЕНИЙ ХОДЬБЫ
Рис. 1. Типичные результаты исследования ходьбы больного БП.
Здесь и на рис. 2, 3: по оси абсцисс — длина шага (см), по оси ординат — количество шагов указанной длины.
Рис. 2. Типичные результаты исследования ходьбы больного с СП.
Рис. 3. Типичные результаты исследования ходьбы здоровых лиц в возрасте 56—75 лет.
Таблица 1. Средние значения исследуемых показателей ходьбы у больных с болезнью Паркинсона и сосудистым паркинсонизмом и их динамика в ходе курса темпоритмовой коррекции
|
Норма для |
|
Болезнь Паркинсона |
|
Сосудистый паркинсонизм |
|||
|
исходное |
в ходе занятия |
состояние |
исходное |
в ходе |
состояние |
||
Показатели |
пожилых, |
занятия с |
после |
|||||
состояние, |
с оптимальным |
после курса, |
состояние, |
|||||
«свобод- |
оптимальным |
курса, |
||||||
|
«свободный |
темпом стиму- |
«свободный |
«свободный |
||||
|
ный темп» |
темпом сти- |
«свободный |
|||||
|
темп» |
ляции |
темп» |
темп» |
||||
|
|
муляции |
темп» |
|||||
|
|
|
|
|
|
|||
Средняя дли- |
56,9±5 |
42,03±11,4 |
47,6±9,05 |
50,09±6,94*** |
44,14±6,35* |
49,7±5,1** |
53,6±8,4*** |
|
на шага, см |
||||||||
|
|
|
|
|
|
|
||
КВШ |
0,165 |
0,651* |
0,254** |
0,29*** |
1,064±0,166* |
0,254** |
0,31*** |
|
Примечание. Достоверные различия между группами: * — р<0,01 между нормой и исходным состоянием; ** — р<0,01 между исходным состоянием и в ходе занятия; *** — р<0,01 между состоянием после курса реабилитации и исходным.
БП со значительным снижением исходной длины шага. |
сколько с достоверным уменьшением (приближением к |
Однако улучшение ходьбы, отмеченное у всех больных, в |
норме) показателя КВШ в обеих группах (уменьшается в |
большей степени коррелирует не столько с длиной шага, |
среднем в 2 раза при БП и более чем в 3 раза при СП). |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 2, 2009 |
23 |

ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
Таблица 2. Средние значения GABS и PDQ-39 до и после курса темпоритмовой коррекции ходьбы
Шкала (баллы) |
Болезнь Паркинсона |
Сосудистый паркинсонизм |
|||
до курса |
после курса |
до курса |
после курса |
||
|
|||||
GABS сумма средних значений пунктов 2, 3, 15, 16, 17 |
6,93±3,76 |
4,40±2,22 |
10,79±3,67 |
6,33±3,92 |
|
PDQ-39, сумма средних значений пунктов 4—8 |
8,87±4,09 |
3,31±3,05 |
11,68±4,48 |
5,07±5,38 |
|
В табл. 2 представлены результаты по Шкале нарушений ходьбы и равновесия (GABS) и опросника качества жизни PDQ-39 до и после курса реабилитации.
Из табл. 2 видно, что курс реабилитации с использованием ТРК позволяет существенно улучшить показатели ходьбы (данные по шкале GABS) и качество жизни пациентов (по опроснику PDQ-39), что представляется чрезвычайно актуальным, учитывая то, что на протяжении исследования дозы антипаркинсонических препаратов не менялись. В дальнейшем мы планируем проведение дополнительных исследований для сравнения возможностей коррекции качества жизни при помощи только фармакологических схем лечения и комплексной терапии, включающей метод ТРК ходьбы и фармакологическое лечение.
Таким образом, созданный нами программноаппаратный комплекс «Дорожка» позволяет объективно оценить длину шага, а введенный КВШ — достоверно сравнивать ходьбу у различных групп испытуемых. Полученные результаты у клинически здоровых испытуемых могут использоваться как нормативные. Оценка вариабельности шага (КВШ) позволяет объективно отличить ходьбу больного БП от таковой при СП, что чрезвычайно важно в дифференциально-диагностическом аспекте. Данные исследования актуальны для составления индивидуальных программ реабилитации, в первую очередь темпоритмовой коррекции ходьбы, применение которой значительно облегчается в связи с быстротой и относительно небольшой трудоемкостью исследования при использовании программно-аппаратного комплекса «Дорожка». Применение данного комплекса подтвердило высокую эффективность методики ТРК у больных БП и СП. Это особенно важно для больных СП, так как у большинства из них ни одно противопаркинсоническое средство не имеет выраженного и стойкого эффекта. Вероятно, в дальнейшем комплекс может использоваться при исследовании влияния на функцию ходьбы других методов ле-
чения, в том числе фармакологических, а также при решении экспертных вопросов.
Эффективность методики можно связать с мобилизацией дополнительных компенсаторных механизмов в виде коркового контроля ходьбы, реализуемого через премоторную кору, а также, возможно, дополнительного вовлечения мозжечковых путей, компенсирующего дисфункцию базальных ганглиев и связанной с ними дополнительной моторной корой.
Внешние стимулы для коррекции ходьбы при БП использовали многие исследователи [13, 15, 19]. Однако применение визуальных стимулов, несмотря на их высокую эффективность в лабораторных условиях, не адаптировано к повседневной жизни больного, а значит эффект после курса будет существенно снижаться с течением времени.
Аудиостимуляция с учетом существования различных портативных звуковоспроизводящих устройств более доступна для последующего ее применения больным. M. Тhaut и соавт. [19] предложили использовать единую частоту аутостимуляции для пациентов, а предлагаемый нами способ подразумевает предварительное тестирование пациента на разных частотах с определением максимально эффективной индивидуально для него частоты (для наибольшего увеличения длины шага, уменьшения КВШ и сохранения комфортного самочувствия пациента), что обеспечивает бóльшую эффективность воздействия на походку. Поскольку в зависимости от приема препаратов состояние моторных функций больного может заметно изменяться («on-off» феномен), подбор темпоритма может осуществляться в различных состояниях, для каждого из которых характерен свой оптимальный ритм, что также способствует лучшему восстановлению ходьбы. Кроме того, возможно использование ритма, «встроенного» в музыку. Однако, хотя психологически он воспринимается лучше, чем простая звуковая ритмическая стимуляция, это в определенной степени затрудняет четкую синхронизацию шага и ритма.
ЛИТЕРАТУРА
1.Антоненко Л.М., Дамулин И.В. Особенности нарушений равновесия и ходьбы при болезни Паркинсона, прогрессирующем надъядерном параличе и мультисистемной атрофии. Неврол журн 2005; 3: 41—50.
2.Брыжахина В.Г., Дамулин И.В., Яхно Н.Н. Нарушения ходьбы и равновесия при дисциркуляторной энцефалопатии. Неврол журн 2004; 2: 11—16.
3.Гашилова Ф.Ф. Клинические и параклинические аспекты паркинсонизма в Томске: Дис. ... канд. мед. наук. Новосибирск 2006.
4.Дамулин И.В., Брыжахина В.Г., Шашкова Е.В., Яхно Н.Н. Нарушения ходьбы и равновесия при дисциркуляторной энцефалопатии. Неврол журн 2004; 4: 13—18.
5.Иллариошкин С.Н., Загоровская Т.Б., Иванова-Смоленская И.А., Маркова Е.Д. Генетические аспекты болезни Паркинсона. Неврол журн 2002; 5: 47—52.
6.Левин О.С. Нарушения ходьбы, механизмы, классификация, принципы диагностики и лечения. В кн.: В.Н. Штока, И.А. ИвановойСмоленской, О.С. Левина (ред.). Экстрапирамидные расстройства: Руководство по диагностике и лечению. М: МЕДпресс-информ 2002; 473—495.
7.Левин О.С. Экстрапирамидные синдромы при цереброваскулярных заболеваниях. В кн.: В.Н. Штока, И.А. Ивановой-Смоленской, О.С. Левина (ред.). Экстрапирамидные расстройства: Руководство по диагностике и лечению. М: МЕДпресс-информ 2002; 503—527.
8.Левин О.С., Докадина Л.В. Эпидемиология паркинсонизма и болезни Паркинсона. Неврол журн 2005; 5: 41—50.
9.Левин О.С., Юнищенко Н.А. Влияние пирибедила (пронорана) на нарушения ходьбы при болезни Паркинсона. Неврол журн 2005; 6: 38—43.
24 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 2, 2009 |

КОРРЕКЦИЯ НАРУШЕНИЙ ХОДЬБЫ
10.Левин О.С., Федорова Н.В. Болезнь Паркинсона. М: Лев Толстой 2006; 15. Azulay J.-P., Mesure S., Amblard B. et al. Visual control of locomotion in
26—27. |
Parkinson’s disease . Brain 1999; 122: 111—120. |
11.Похабов Д.В., Руднев В.А., Прокопенко С.В. Опыт снижения дозы до16. DeBoer A.G.E.M., Wijker W., Speelman J.D. et al. Quality of life in patients
фаминсодержащих препаратов в схеме лечения болезни Паркинсона на фоне темпо-ритмовой коррекции ходьбы. Журн неврол и психиат 2003; 8: 76—77.
12.Похабов Д.В., Абрамов В.Г. Нарушения ходьбы при болезни Паркинсона и сосудистом паркинсонизме и их восстановление методом темпоритмовой коррекции. Практическая неврология и нейрореабилитация 2006; 2: 9—15.
13.Похабов Д.В., Абрамов В.Г. Диагностика и лечение сосудистого паркинсонизма с использованием метода темпоритмовой коррекции ходьбы. Неврол журн 2007; 3: 26—31.
14.Шток В.Н., Федорова Н.В. Болезнь Паркинсона. В кн.: В.Н. Штока, И.А. Ивановой-Смоленской, О.С. Левина (ред.). Экстрапирамидные расстройства: Руководство по диагностике и лечению. М: МЕДпрессинформ 2002; 87—124.
with Parkinson’s disease: Development of a questionnaire. J Neurol Neurosurg Psychiat 1996; 61: 70—74.
17.Fahn S., Jancovic J. (eds.) Principiles and practice of movement disorders. USA, Philadelphia 2007; 290—291.
18.Ruzicka E., Jankovic J.J. Disorders of gait. Parkinson’s Disease and Movement Disorders. Philadelphia: Lippincott, Williams & Wilkins 2002; 409— 437.
19.Thaut M.H., McIntosh G.C., Rice R.R. et al. Rhythmic auditory stimulation in gait training for Parkinson’s disease patients. Mov Disord 1996; 11: 193— 200.
20.Walters E.C., van Laar T., Berendse H.W. (eds.) Parkinsonism and related disorders. VU University Press Amsterdam 2007; 154.
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 2, 2009 |
25 |
