
- •Тема 3. Альдегиды и кетоны 36
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Основные направления реакционной способности углеводородов в зависимости от их электронного строения
- •Циклоалканы
- •Циклопропан с3н6
- •Транс-1,4-диметилциклогексан цис-1,4-диметилциклогексан
- •1. Гидрирование
- •Пропен пропан
- •2. Галогенирование
- •3. Гидрогалогенирование:
- •6. Полимеризация:
- •Алкадиены Это углеводороды, содержащие две двойные связи. Общая формула Сn h2n-2.
- •1. Гидрирование:
- •2. Гидрогалогенирование:
- •Ароматические углеводороды (арены)
- •Химические свойства
- •Заместители 2 рода ( -cooh, -so3h, -cho, -no2 и др.) – электроноакцепторы, уменьшают электронную плотность в кольце, затрудняют реакцию se и ориентируют электрофил в мета-положение.
- •Тема 2. Спирты. Фенолы. Нафтолы. Тиолы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •Кислотность и основность органических соединений
- •Кислоты тон
- •Одноатомные спирты
- •Дегидрирование альдегид
- •Дегидрирование кетон
- •Многоатомные спирты
- •Спирты высшей атомности
- •Свойства фенолов как ароматических соединений. Реакции электрофильного замещения
- •Нафтолы
- •Ароматические спирты
- •Химические свойства
- •Глоссарий
- •Тема 3. Альдегиды и кетоны
- •Пиридоксаль пиридоксальфосфат
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •I. Реакции нуклеофильного присоединения
- •4. Взаимодействие с галогенсодержащими реагентами
- •II. Реакции за счет -сн2-звена
- •1. Галогенирование:
- •III. Реакции, характерные только для альдегидов
- •Глоссарий
- •Тема 4. Карбоновые кислоты и их функциональные производные
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Содержание этапов занятия
- •Этановая кислота 2-метилпропановая бутен-3-овая кислота
- •Высшие жирные кислоты (вжк)
- •Изомерия
- •Малеиновая фумаровая кислота
- •Линолевая кислота
- •Химические свойства
- •2. Реакции нуклеофильного замещения (sn ):
- •Двухосновные карбоновые кислоты
- •Трехосновные кислоты
- •Ноос–сн2–с–сн2–соон лимонная 3-гидрокси – 3-карбокси -
- •Специфические реакции двухосновных кислот
- •Тема 5. Липиды
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Омыляемые липиды
- •Омыляемые липиды
- •Жирные кислоты
- •Простые омыляемые липиды
- •Сложные омыляемые липиды
- •Фосфолипиды
- •Глицерофосфо- сфингофосфо-
- •Гликолипиды
- •Стероиды
- •Классификация стероидов
- •Эстрадиол
- •Глоссарий
4. Взаимодействие с галогенсодержащими реагентами

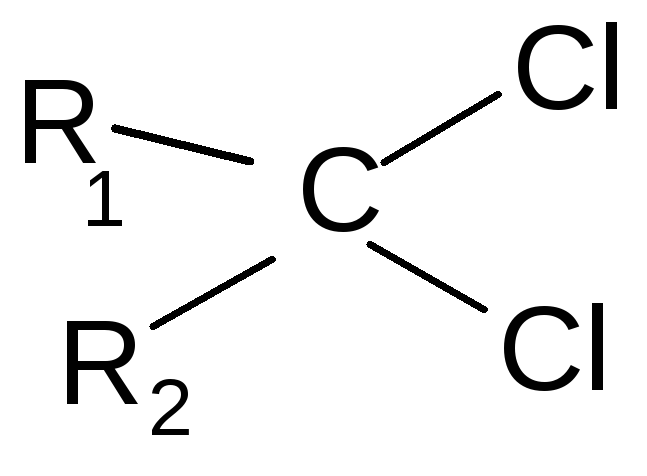
 +PCl5+POCl3
+PCl5+POCl3
хлорокись фосфора
5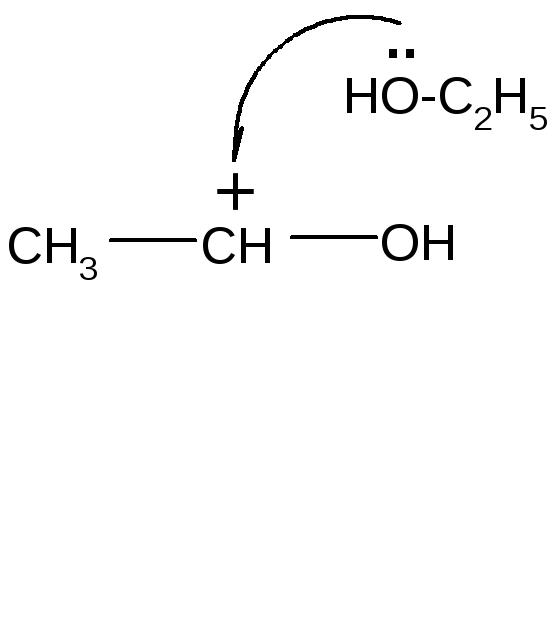 .
Взаимодействие со спиртами.Оксосоединения,
преимущественно альдегиды, взаимодействуют
с одной или двумя молекулами спирта,
образуя соответственно полуацетали и
ацетали. Реакция катализируется
кислотами. Кетоны в этих условиях в
реакции не вступают.
.
Взаимодействие со спиртами.Оксосоединения,
преимущественно альдегиды, взаимодействуют
с одной или двумя молекулами спирта,
образуя соответственно полуацетали и
ацетали. Реакция катализируется
кислотами. Кетоны в этих условиях в
реакции не вступают.
П
![]() олучение
полуацеталя. Механизм:
олучение
полуацеталя. Механизм:
H+
+
![]()
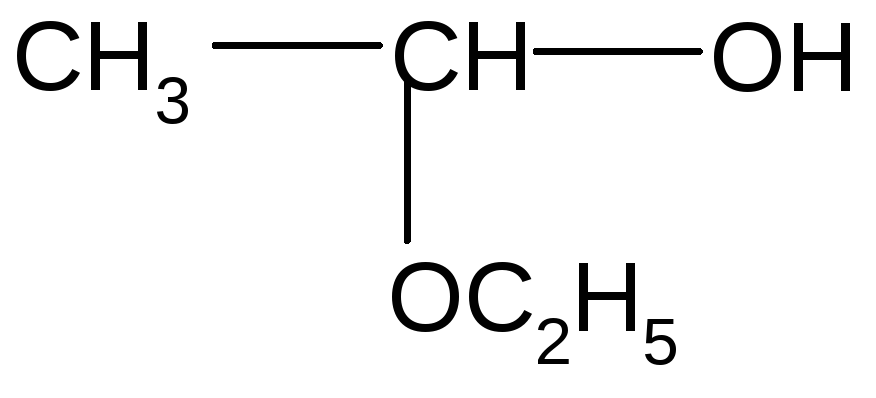
 -H+
-H+
![]()
![]()
Получение ацеталя:
H+, -H2O
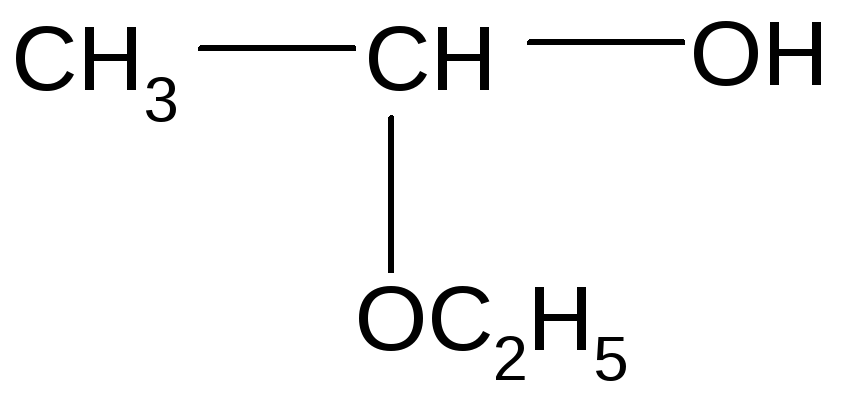
![]()
 +
+![]()
Образование полуацеталей и ацеталей имеет большое значение в химии углеводов: моно-, ди- и полисахаридов. Циклическая форма моносахаридов строится по принципу полуацеталей. Связь между моносахаридами в ди – и полисахаридах – ацетальная. В виде ацеталей происходит выделение из организма чужеродных соединений. Так глюкуроновая кислота (циклический полуацеталь) образует с фенолом ацеталь и в таком виде выводит его.
6 .
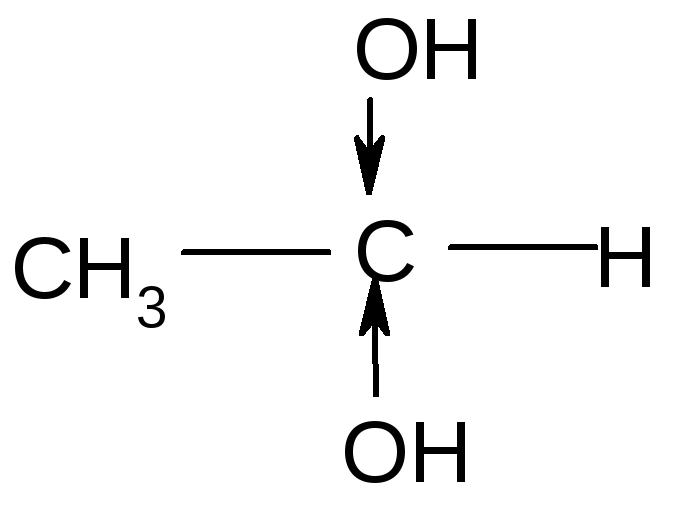
Реакция с водой (гидратация). Альдегиды
и в значительно меньшей степени кетоны
обратимо присоединяют воду:
.
Реакция с водой (гидратация). Альдегиды
и в значительно меньшей степени кетоны
обратимо присоединяют воду:
Н+

 +H2O
+H2O
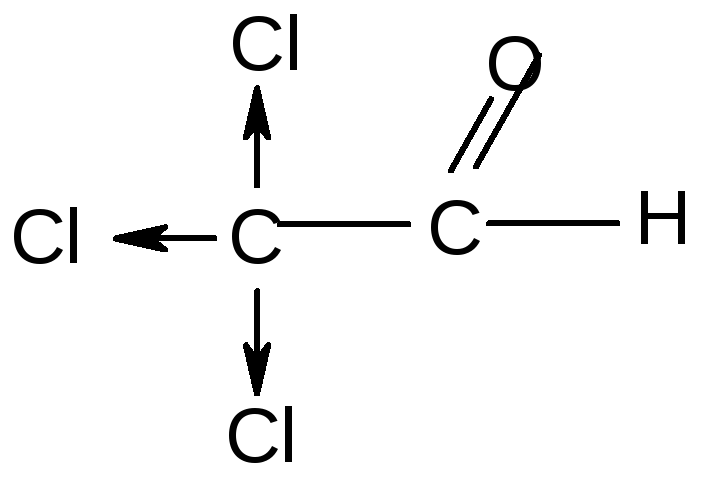
Полученный двухатомный спирт (диол) неустойчив. Прочность связывания воды, т.е. степень гидратации, зависит от строения и характера радикала в различных альдегидах. Например, трихлоруксусный альдегид (хлораль) хорошо гидратируется благодаря присутствию в радикале трех атомов хлора.
Н+
 + Н-ОН
+ Н-ОН
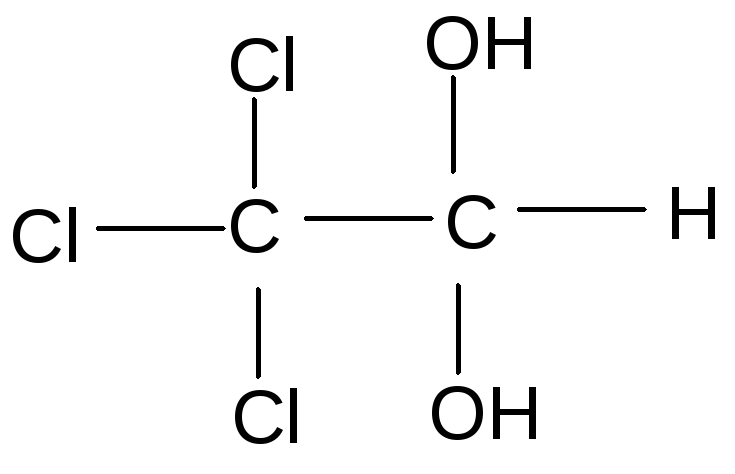
хлоральгидрат
Хлоральгидрат – один из немногочисленных примеров прочных гидратов альдегидов. Хлоральгидрат – лекарственный препарат снотворного и противосудорожного действия. Галогены усиливают снотворное действие, а гидратация уменьшает токсичность.
II. Реакции за счет -сн2-звена
1. Галогенирование:


 +Cl2
+Cl2
-HCl
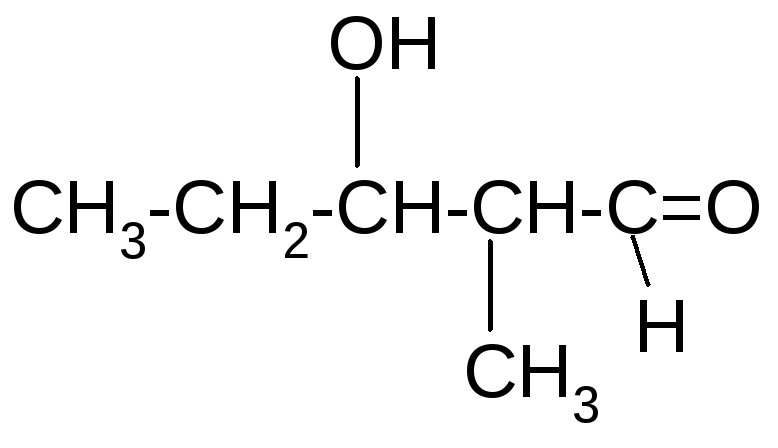
2. Реакция альдольной конденсации обусловлена подвижностью водорода в -положении в радикале и осуществляется в присутствии разбавленных щелочей. Ее можно рассматривать как реакцию нуклеофильного присоединения одной молекулы альдегида к другой:
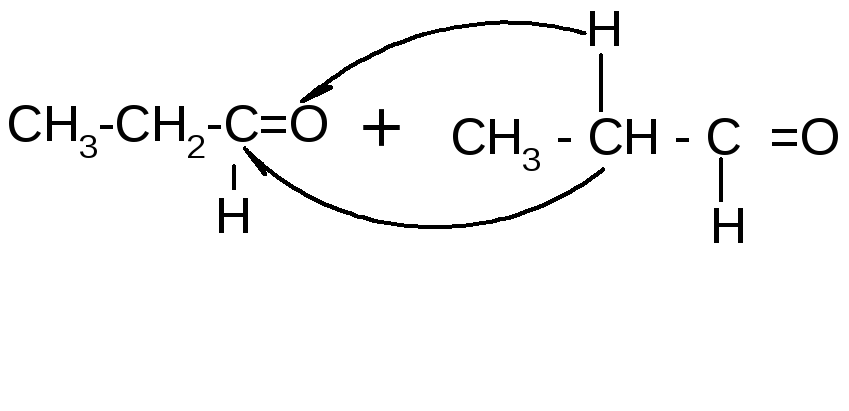
+![]() -
OH-
5 4 3 2 1
-
OH-
5 4 3 2 1











2-метил-3- гидроксипентаналь
Поскольку продукт реакции содержит в молекуле гидроксильную (-ол) и альдегидную (-аль) группы, его называют альдоль, а сама реакция получила название альдольной конденсации. Реакции этого типа имеют место в природе, например биосинтез лимонной кислоты в цикле трикарбоновых кислот, нейраминовой кислоты и т. д.
