
- •Тема 3. Альдегиды и кетоны 36
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Основные направления реакционной способности углеводородов в зависимости от их электронного строения
- •Циклоалканы
- •Циклопропан с3н6
- •Транс-1,4-диметилциклогексан цис-1,4-диметилциклогексан
- •1. Гидрирование
- •Пропен пропан
- •2. Галогенирование
- •3. Гидрогалогенирование:
- •6. Полимеризация:
- •Алкадиены Это углеводороды, содержащие две двойные связи. Общая формула Сn h2n-2.
- •1. Гидрирование:
- •2. Гидрогалогенирование:
- •Ароматические углеводороды (арены)
- •Химические свойства
- •Заместители 2 рода ( -cooh, -so3h, -cho, -no2 и др.) – электроноакцепторы, уменьшают электронную плотность в кольце, затрудняют реакцию se и ориентируют электрофил в мета-положение.
- •Тема 2. Спирты. Фенолы. Нафтолы. Тиолы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •Кислотность и основность органических соединений
- •Кислоты тон
- •Одноатомные спирты
- •Дегидрирование альдегид
- •Дегидрирование кетон
- •Многоатомные спирты
- •Спирты высшей атомности
- •Свойства фенолов как ароматических соединений. Реакции электрофильного замещения
- •Нафтолы
- •Ароматические спирты
- •Химические свойства
- •Глоссарий
- •Тема 3. Альдегиды и кетоны
- •Пиридоксаль пиридоксальфосфат
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •I. Реакции нуклеофильного присоединения
- •4. Взаимодействие с галогенсодержащими реагентами
- •II. Реакции за счет -сн2-звена
- •1. Галогенирование:
- •III. Реакции, характерные только для альдегидов
- •Глоссарий
- •Тема 4. Карбоновые кислоты и их функциональные производные
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Содержание этапов занятия
- •Этановая кислота 2-метилпропановая бутен-3-овая кислота
- •Высшие жирные кислоты (вжк)
- •Изомерия
- •Малеиновая фумаровая кислота
- •Линолевая кислота
- •Химические свойства
- •2. Реакции нуклеофильного замещения (sn ):
- •Двухосновные карбоновые кислоты
- •Трехосновные кислоты
- •Ноос–сн2–с–сн2–соон лимонная 3-гидрокси – 3-карбокси -
- •Специфические реакции двухосновных кислот
- •Тема 5. Липиды
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Омыляемые липиды
- •Омыляемые липиды
- •Жирные кислоты
- •Простые омыляемые липиды
- •Сложные омыляемые липиды
- •Фосфолипиды
- •Глицерофосфо- сфингофосфо-
- •Гликолипиды
- •Стероиды
- •Классификация стероидов
- •Эстрадиол
- •Глоссарий
Химические свойства
Карбоксильная группа карбоновых кислот имеет сложное строение: она состоит из карбонильной группы С=О и гидроксильной группы –ОН, которые влияют друг на друга.
Благодаря +M–эффекту ОН-группы в карбоксильной группе возникает р-сопряжение, происходит выравнивание электронной плотности в ней и сведение полярности карбонильной группы до минимума. Этим объясняется инертность карбонильной группы в кислотах. +М –эффект гидроксильной группы объясняет также смещение электронной плотности в ней в сторону более электроотрицательного атома кислорода и диссоциацию кислот.
( -I) – эффект гидроксильной
группы поляризует связь СОН
и делает возможным ее отщепление: группа
ОН может отщепляться, что обусловливает
реакции нуклеофильного замещения. Таким
образом, главные реакции идут либо за
счет замещения ОН - группы, либо за счет
водорода этой группы.
-I) – эффект гидроксильной
группы поляризует связь СОН
и делает возможным ее отщепление: группа
ОН может отщепляться, что обусловливает
реакции нуклеофильного замещения. Таким
образом, главные реакции идут либо за
счет замещения ОН - группы, либо за счет
водорода этой группы.
Кислотные свойстваСила карбоновых кислот зависит от стабильности аниона, образующегося после отрыва протона. Стабильность аниона определяется, прежде всего, степенью делокализации отрицательного заряда: чем выше степень делокализации, тем стабильнее анион.
В карбоксилат-анионе заряд делокализуется по сопряженной системе, т. е. равномерно распределяется между двумя атомами кислорода карбоксилат–аниона, что придает ему стабильность:
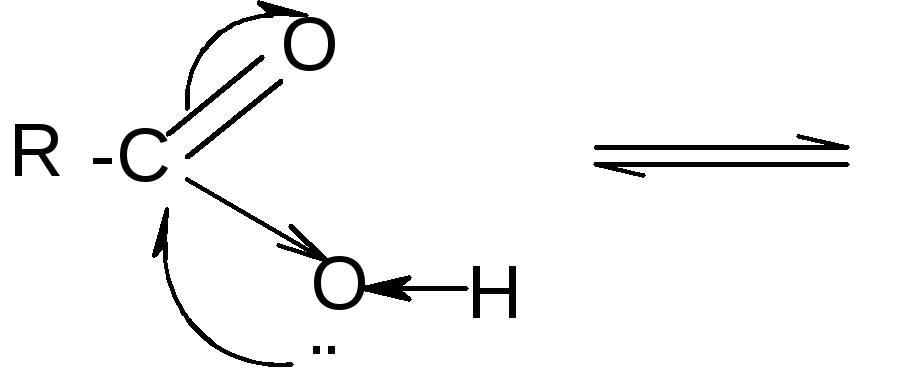

+ Н+
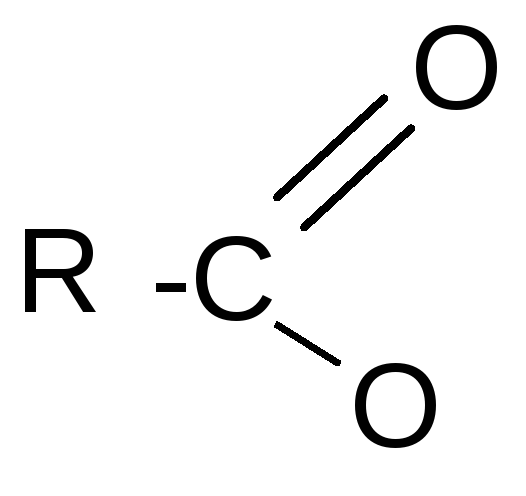
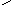
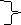 O
O
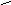
![]()
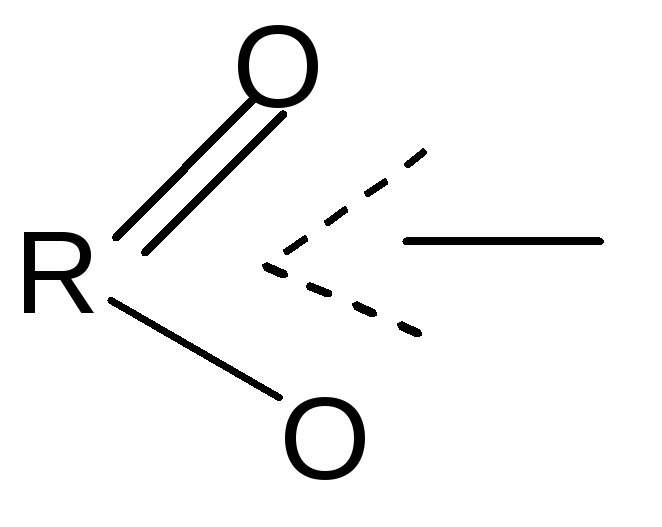 R–C
R–C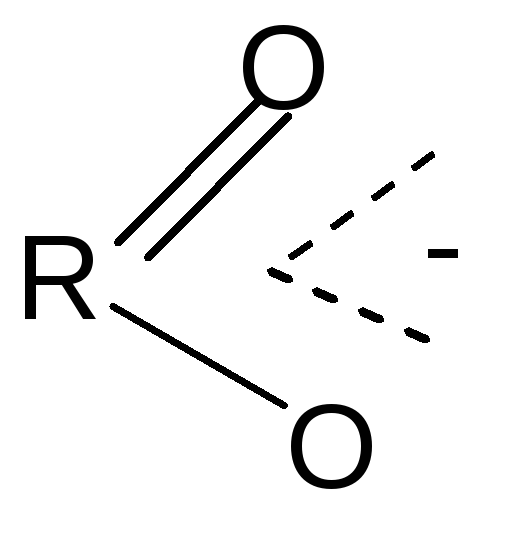 (-)
(-)
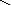
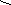 (–)
O
(–)
O
В рамках класса сила кислот зависит от строения углеводородных радикалов и заместителей в них. Электронодонорные заместители ослабляют кислотные свойства, так как дестабилизируют карбоксилат–анион; электроноакцепторные заместители, оттягивая электронную плотность, способствуют делокализации заряда в карбоксилат – анионе и тем самым стабилизируют его, т.е. усиливают кислотные свойства.
Так, при введении в углеводородный радикал уксусной кислоты атомов хлора кислотность будет увеличиваться за счет электроноакцепторных свойств атома хлора:
Cl
СН3СООНСН2СООНСlСНСООНСlССООН
СlClCl
рКа 4,76 2,85 1,25 0,66
Ароматические кислоты имеют более сильные кислотные свойства, чем незамещенные алифатические (для бензойной кислоты С6Н5-СООН рКа=4,19) – сказывается электронное влияние фенильного радикала (-I).
Кислотные свойства проявляются в реакции нейтрализации:
СН3– СООН +NaOH![]() CH3COONa+H2O
CH3COONa+H2O
2. Реакции нуклеофильного замещения (sn ):
а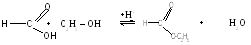 )
реакция этерификации:
)
реакция этерификации:
этилформиат
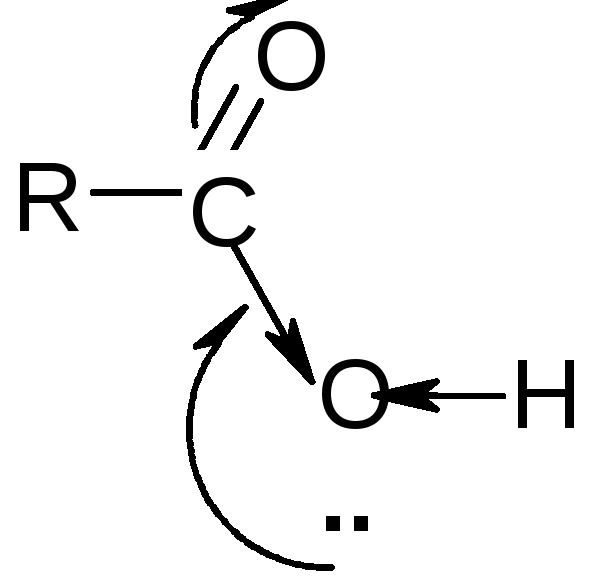
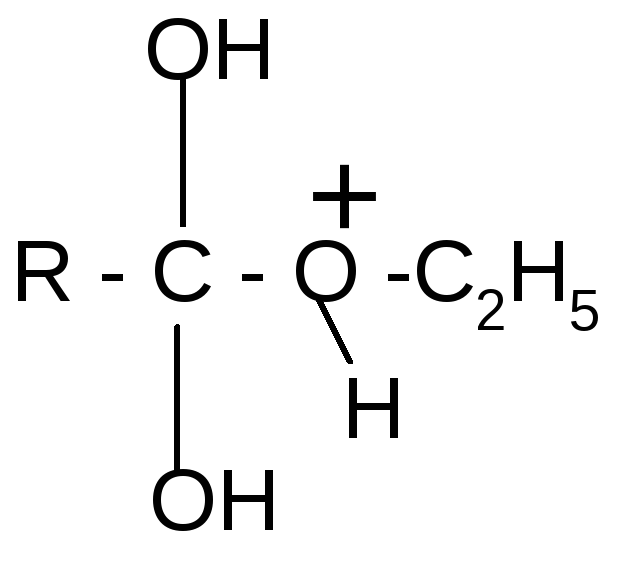 Механизм реакции:
Механизм реакции:
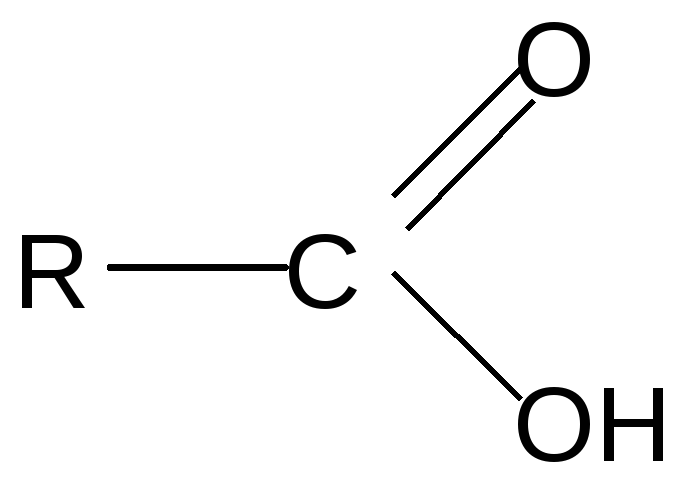
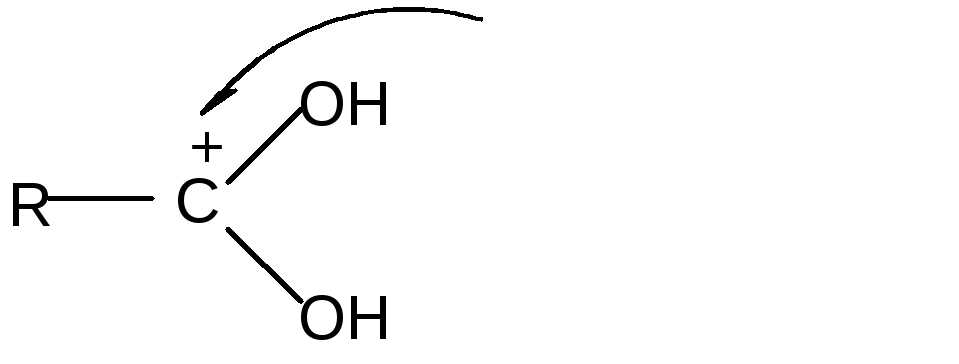 ..
..
НОС2Н5 -Н2О
 + Н+
+ Н+
![]()
![]()
![]()

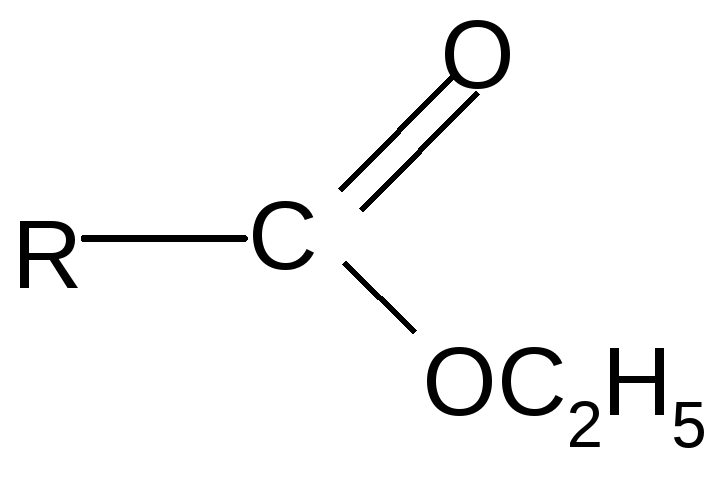
-Н+
![]()
![]()
Реакция этерификации – обратимый процесс: прямая реакция – образование сложного эфира, обратная – его кислотный или щелочной гидролиз. Чтобы сдвинуть равновесие вправо, необходимо из реакционной смеси удалить воду
б) образование галогенангидридов:
Среди галогенангидридов наибольшее значение имеют хлорангидриды, которые получают при действии хлоридов фосфора (III) или фосфора (V):
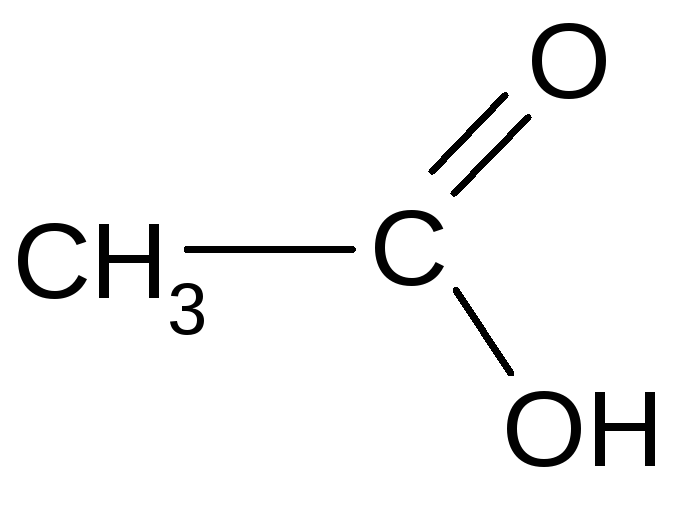
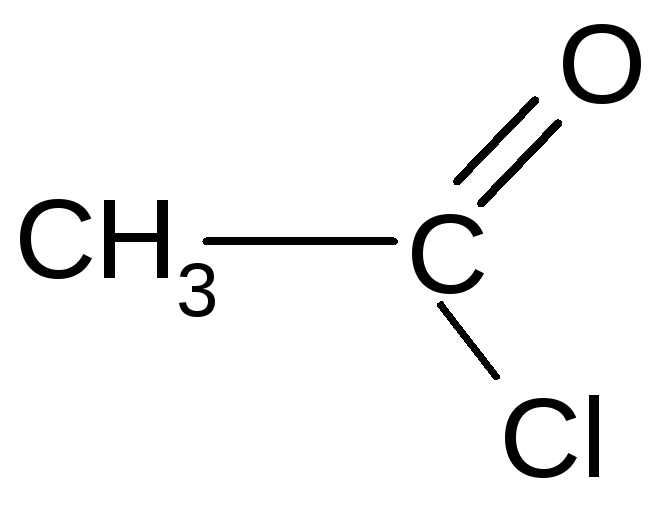
 + PCl5
+ POCl3
+ HCl
+ PCl5
+ POCl3
+ HCl
хлористый ацетил
в) образование ангидридов кислот:
При действии сильных водоотнимающих агентов (P2O5, Al2O3) образуются ангидриды кислот:
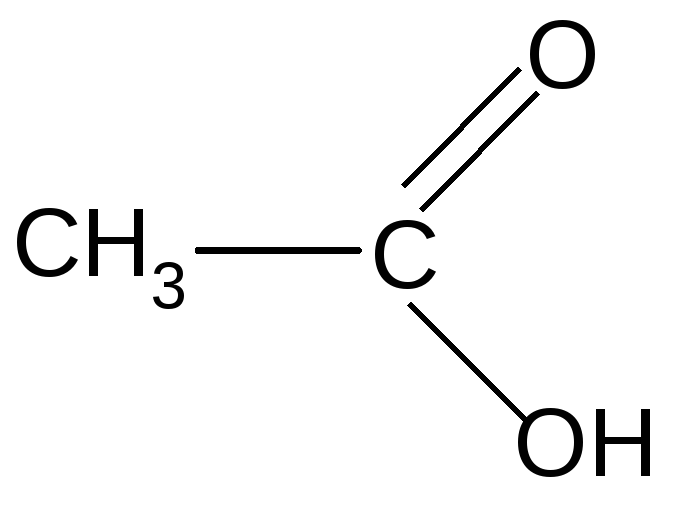
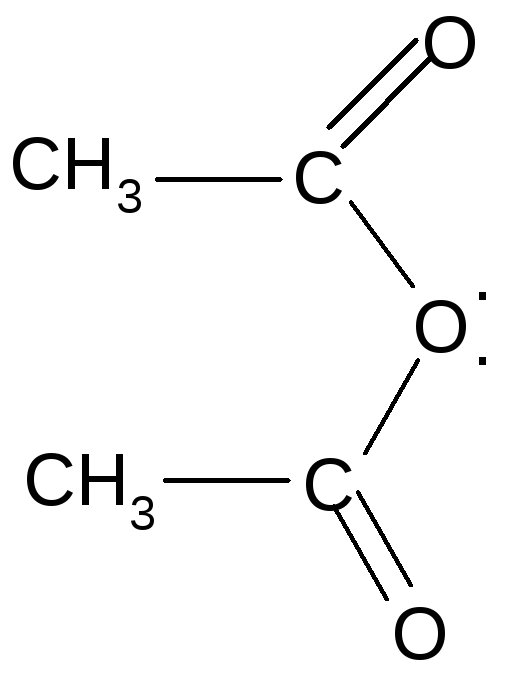
___
Al2O3 + H2O


Большое практическое значение имеет уксусный ангидрид, используемый для получения волокон (ацетатный шелк), многих лекарственных веществ. Применяется также для ацетилирования соединений.
Галогенангидриды и ангидриды очень реакционноспособны. При взаимодействии галогенангидридов с соединениями, содержащими атом металла или активный атом водорода, происходит замена его кислотным остатком. Подобные реакции называются ацилированием, в частности ацетилированием, если в молекулу входит ацетил, остаток уксусной кислоты.
В организме ацетилирующим реагентом является ацетилкофермент А - ключевой метаболит всех видов обмена в клетке.
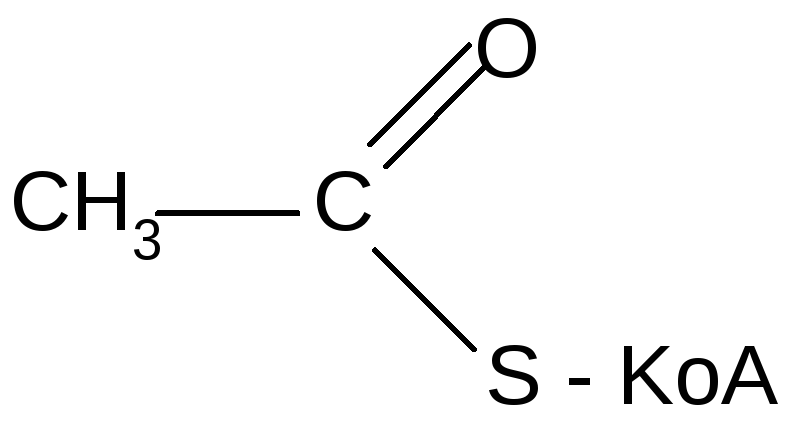
г) образование амидов:
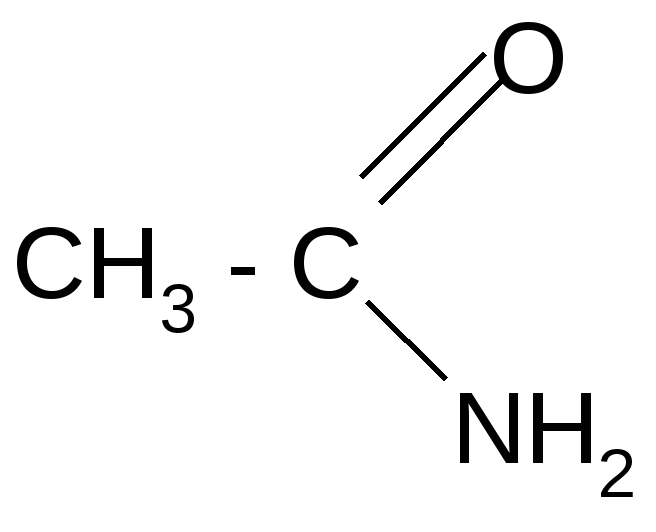
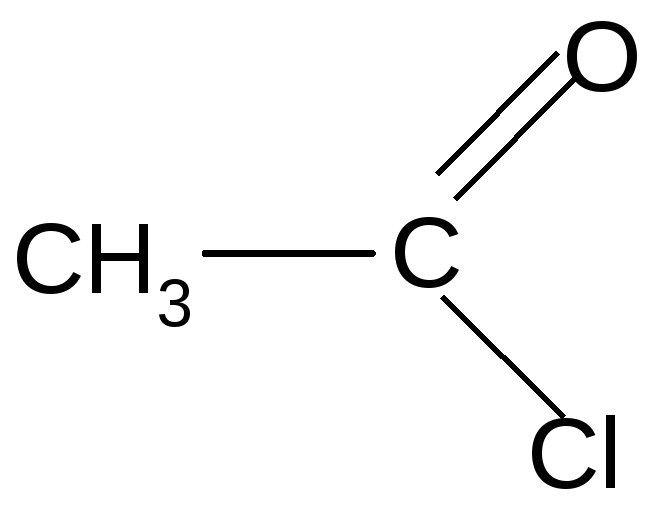
 + NH3+HCl
+ NH3+HCl
(амид уксусной
кислоты)


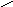 O
t° С
O
t° С


 + NH3
CH3
– C + H2O
+ NH3
CH3
– C + H2O
 ONH4
ONH4
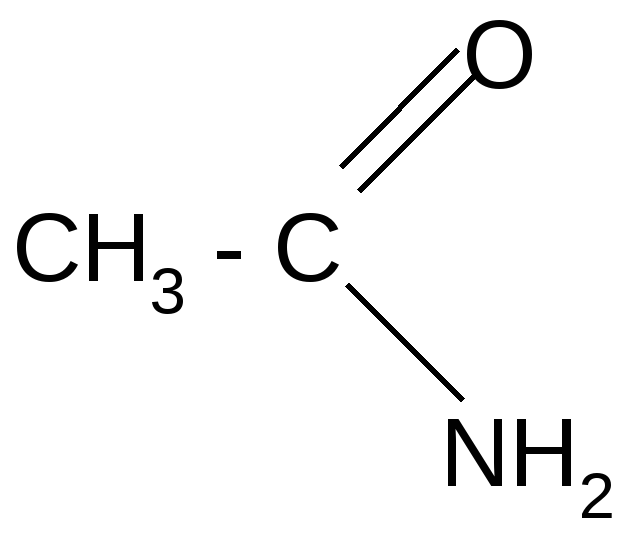
Амиды можно получить взаимодействием карбоновых кислот с аммиаком. Вначале образуются аммонийные соли, которые при нагревании теряют воду и превращаются в амиды. Амиды кислот подвержены различным превращениям. При нагревании с Р2О5отщепляется вода и образуются нитрилы кислот:
 __
__
t°, P2O5
 CH3–C=N
+ H2O
CH3–C=N
+ H2O
нитрил
уксусной
кислоты
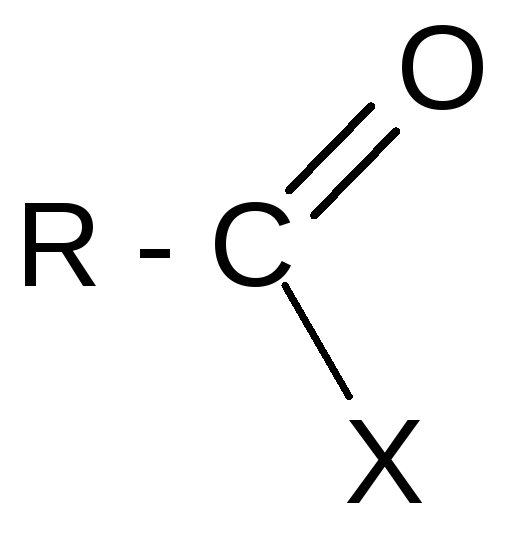
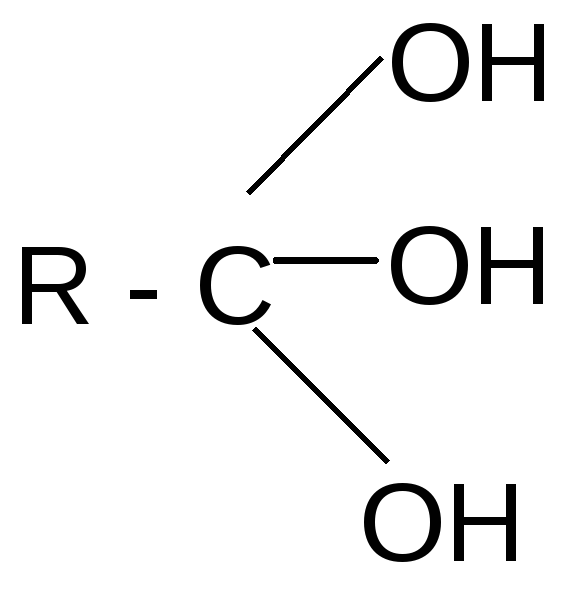
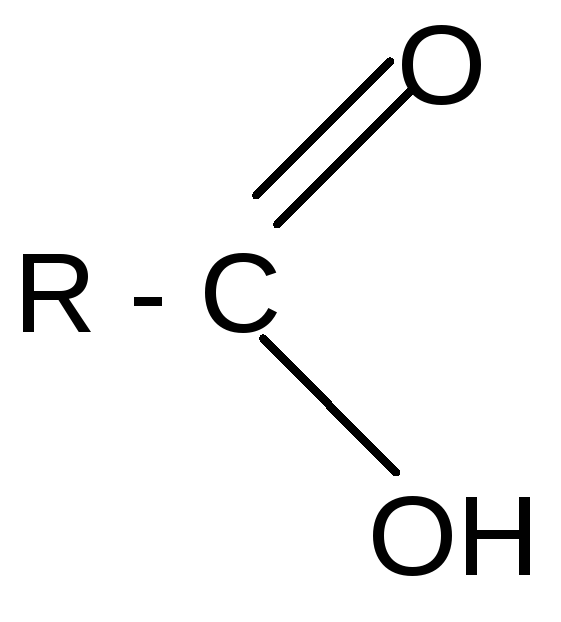
Все функциональные производные способны гидролизоваться с образованием карбоновых кислот:

 + Н2О
+ НХ
+ Н2О
+ НХ
 ___
___
 ______
______
HOH
R
 -C=
N + HOH
___
-C=
N + HOH
___
HOH-NH3-H2O
При образовании функциональных производных карбоновых кислот мы сталкиваемся с двумя видами кислотных радикалов:

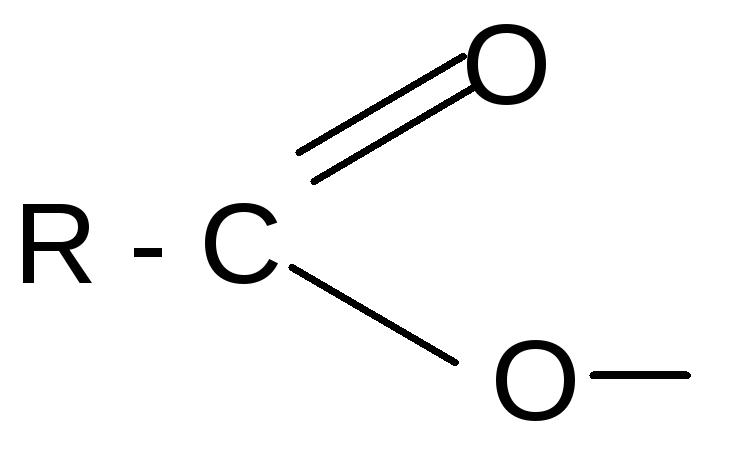
ацил ацилат
-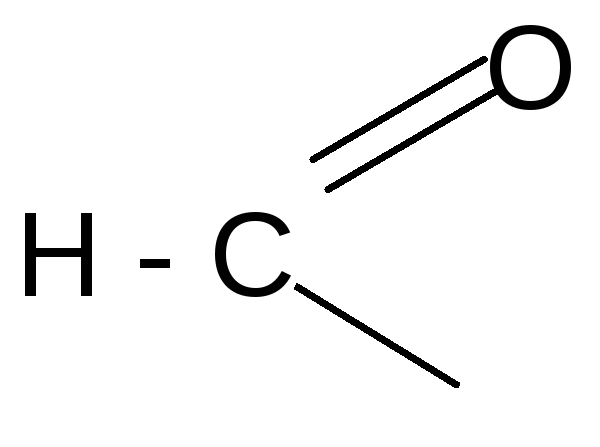 ---------------------------------------------------------------------------------------------
---------------------------------------------------------------------------------------------
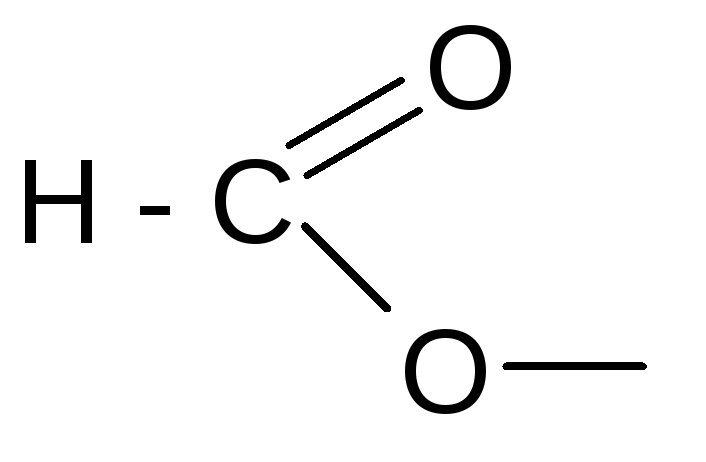
формил формиат

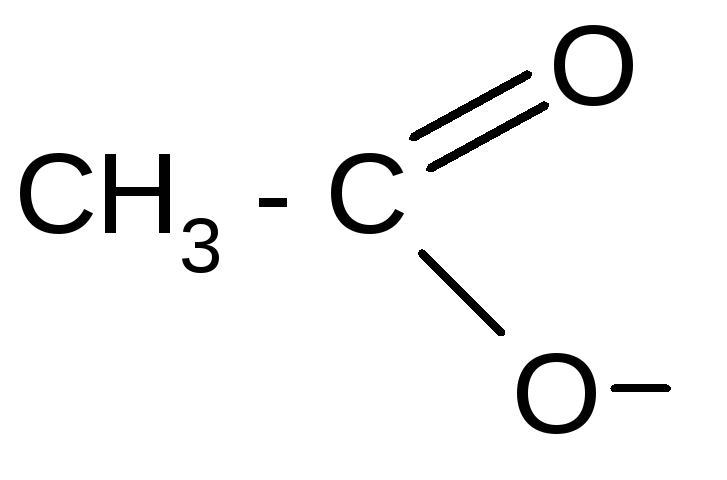
ацетил ацетат
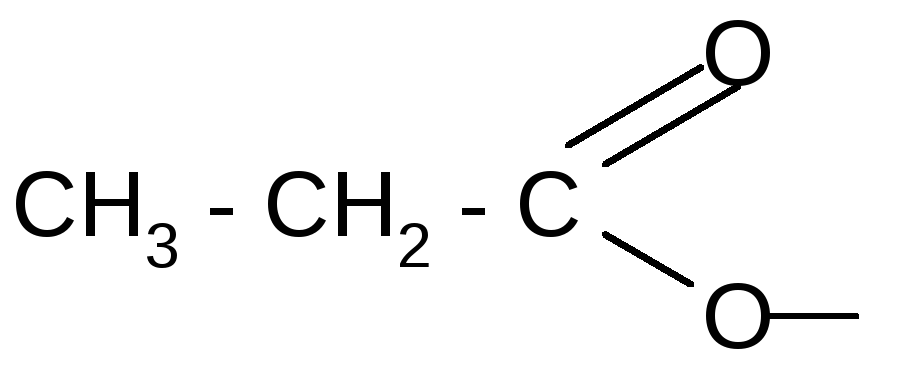
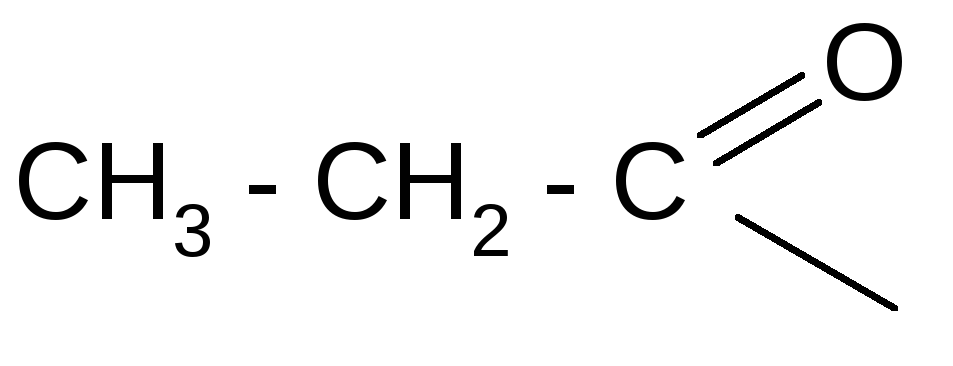
пропионил пропионат

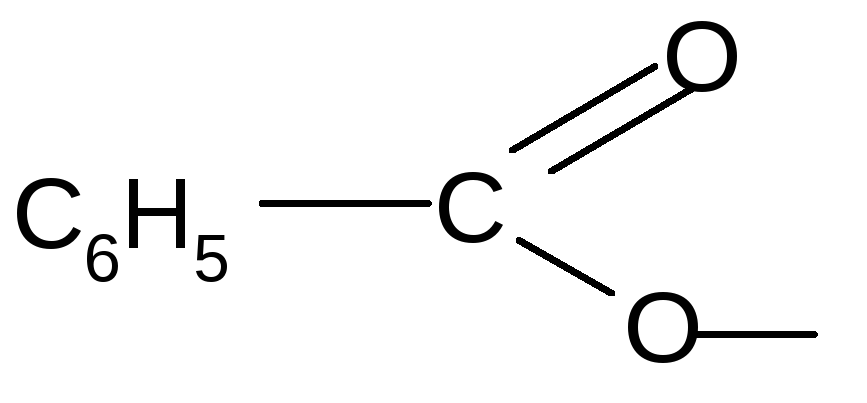
бензоил бензоат
Названия функциональных производных строятся по названию кислотных радикалов.
3. Реакции с участием радикалов монокарбоновых кислот. Углеводородные радикалы в карбоновых кислотах проявляют типичные химические свойства, соответствующие их природе: замещение – в насыщенных и ароматических углеводородных остатках кислот; присоединение, окисление, полимеризация – в ненасыщенных. При этом указанныереакцииимеют некоторые особенности, обусловленные наличием карбоксильной группы:
а) галогенирование насыщенных алифатических кислот:
t°
С Н3–СH2–СH–СООН
+Br2 CH3–CH2 –CH–COOH+HBr
Н3–СH2–СH–СООН
+Br2 CH3–CH2 –CH–COOH+HBr
HBr
Замещение под действием галогенов идет избирательно у - углеродного атома. Это объясняется появлением СН – кислотного центра у- атома углерода под действием –Iэффекта карбоксильной группы. Реакция используется для получения гетерофункциональных кислот --окси и-аминокислот;
б) реакции присоединения к ненасыщенным кислотам:если в ненасыщенных кислотах карбоксильная группа вступает во взаимодействие с двойнойсвязью, образуя систему сопряжения, то благодаря –М эффекту СООН – группы вся-система смещена в сторону СООН – группы,что приводит к нарушению правила Марковникова в реакциях присоединения по двойной связи в углеводородном радикале:
+
![]() -
-
 СH2==CH
COOH
+ HBr CH2
– CH – COOH
СH2==CH
COOH
+ HBr CH2
– CH – COOH
Br H
в) реакции окисления и полимеризации ненасыщенных кислот: эти реакции
протекают аналогично тем же реакциям алкенов:
KMnO4,H2O
 СН2= СН – СООН СН2–
СН - СООН
СН2= СН – СООН СН2–
СН - СООН
ОН ОН
пропеновая 2,3 –дигидроксипропановая
 (акриловая)
(акриловая)
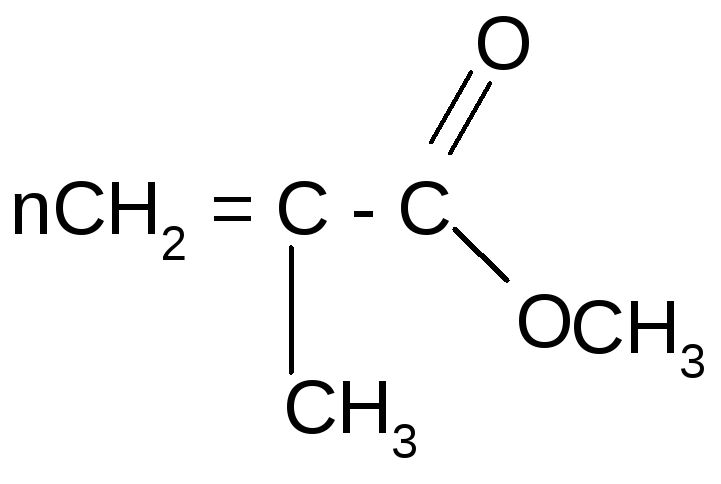

метиловый эфир метакриловой полиметилметакрилат
кислоты (плексиглас, органическое стекло)
г) реакции электрофильного замещения в ароматических кислотах:
К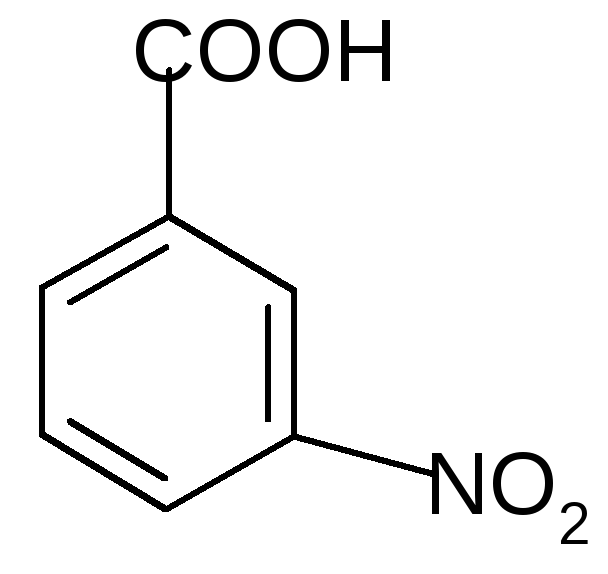 арбоксильная
группа за счет (–М) и (–I)
- эффектов смещает электронную плотность
бензольного кольца и направляет вновь
поступающие электрофильные группы
преимущественно в мета-положение.
Например:
арбоксильная
группа за счет (–М) и (–I)
- эффектов смещает электронную плотность
бензольного кольца и направляет вновь
поступающие электрофильные группы
преимущественно в мета-положение.
Например:

t0
 -+ HO – NO2+ Н2О
-+ HO – NO2+ Н2О
3–нитробензойная кислота
