
- •1. Кинематическое описание движения (формулы для описания поступательного и вращательного движения).
- •Поступательным называется такое движение твердого тела, при котором любая прямая, проведенная в этом теле, перемещается, оставаясь параллельной своему начальному направлению.
- •Движение тела по окружности с постоянной по модулю скоростью - это движение, при котором тело за любые равные промежутки времени описывает одинаковые дуги.
- •Ускорение при движении тела по окружности с постоянной по модулю скоростью (центростремительное ускорение)
- •2. Законы Ньютона для поступательного и вращательного движения.
- •Поэтому форма записи второго закона Ньютона для прямолинейной формы движения с учетом сказанного должна выглядеть иначе, а именно:
- •При неравномерном вращении тела запись второго закона Ньютона должна выглядеть так:
- •3. Постулаты специальной теории относительности и геометрия пространства времени.
- •4. Фундаментальные взаимодействия. Участники взаимодействия, переносчики взаимодействия, радиус взаимодействия, время взаимодействия.
- •5. Силы тяготения и электрические силы. Какие силовые поля называются потенциальными?
- •6. Силы упругости. Деформации, их виды.
- •7. Закон Гука и модуль Юнга.
- •8. Силы трения. Виды трения. Трение покоя. (График зависимости силы трения от величины внешней силы). Внутреннее трение, формула Стокса.
- •9. Закон сохранения импульса как фундаментальный закон природы.
- •10. Центр масс системы. Вычисление скорости центра масс.
- •12. Работа и кинетическая энергия. Мощность.
- •13. Закон сохранения полной механической энергии.
- •14. Момент инерции твердого тела. Момент импульса. Теорема Штейнера.
- •15. Уравнение движения и условия равновесия твердого тела.
- •16. Закон сохранения момента импульса. Кинетическая энергия вращения.
- •17.Формула ньютона для сил внутреннего трения. Коэффициент вязкости.
- •18. Колебания
- •Дифференциальное уравнение гармонических колебаний и его решение.
- •Получим
- •22. Амплитуда и фаза при вынужденных колебаниях. Резонансные кривые.
- •24. Поляризация волн. Три вектора, определяющих электромагнитную волну. Световой вектор. Виды поляризации.
- •25. Закон Брюстера.
- •30 Эффект Максвелла для поляризованного света.
- •31 Точечный источник волн. Плоская и сферическая волна.
- •32 Фазовая скорость волны. Длина волны, волновое число. Групповая скорость.
- •33 Когерентность, время когерентности, длина когерентности.
- •34 Интерференция плоских волн условия возникновения и наблюдения интерференционного максимума и минимума.
- •35. Интерференция в тонких пленках. Просветление оптики.
- •36. Полосы равного наклона.
- •37. Полосы равной толщины.
- •38. Изменение фазы волны при отражении от границы раздела двух сред.
- •39. Принцип Гюйгенса-Френеля.
- •40. Дифракция на круглом отверстии.
- •40. Дифракция на круглом отверстии.(это объяснение из учебника)
- •41. Дифракция Фраунгофера. Дифракционная решетка.
- •42. Условия возникновения дифракционного максимума и минимума.
- •43. Дифракция Фраунгофера и спектральное разложение. Разрешающая способность и дисперсия дифракционной решетки.
- •44.Дифракционные и дисперсионные спектры, их отличия.
- •45. Внешний фотоэффект. Законы Столетова.
- •46. Вольт-амперная характеристика фотоэлемента, ток насыщения и запирающее напряжение (от каких параметров они зависят).
- •47. Работа выхода при внешнем фотоэффекте, красная граница фотоэффекта.
- •48. Модели атома Томсона и Резерфорда.
- •49. Модель атома Бора, противоречия данной теории, все достоинства и недостатки.
- •50. Гипотеза де Бройля, свойства волн де Бройля.
- •51. Волновые свойства материи. Соотношения неопределенности Гейзенберга.
- •52. Гипотеза Борна, волновая функция. Весь ответ неправильный
- •53. Принцип неразличимости микрочастиц. Бозоны и фермионы.
- •56. Энергетическая диаграмма водородоподобного атома. Формула Ридберга.
- •57. Состав атомного ядра. Нуклоны.
- •58. Изотопы, изобары, изомеры
- •59. Дефект массы атомного ядра. Основы ядерной энергетики.
- •60. Закон радиоактивного распада в интегральной и дифференциальной форме.
- •Е м61. Закон Бугера
- •62. Характеристики излучения
- •63.Траектории движения α, β, γ излучения в электрическом, магнитном и гравитационном полях.
- •64. Способы регистрации радиоактивного излучения. Счетчик Гейгера и Камера Вильсона.
49. Модель атома Бора, противоречия данной теории, все достоинства и недостатки.
Боровская модель атома - полуклассическая модель атома, предложенная Нильсом Бором в 1913 г. За основу он взял планетарную модель атома, выдвинутую Резерфордом. Однако, с точки зрения классической электродинамики, в модели Резерфорда, двигаясь вокруг ядра, должен был бы излучать энергию непрерывно и очень быстро и, потеряв ее, упасть на ядро. Чтобы преодолеть эту проблему, Бор ввел допущение, суть которого заключается в том, что электроны в атоме могут двигаться только по определенным (стационарным) орбитам, находясь на которых они не излучают энергию, а излучение или поглощение происходит только в момент перехода с одной орбиты на другую. Причём, стационарными являются лишь те орбиты, при движении по которым момент количества движения электрона равен целому числу постоянных Планка:
![]()
Используя
это допущение и законы классической
механики, а именно равенство силы
притяжения электрона со стороны ядра
и центробежной силы, действующей на
вращающийся электрон, он получил
следующие значения для радиуса
стационарной орбиты
![]() и энергии
и энергии![]() находящегося на этой орбите электрона:
находящегося на этой орбите электрона:
![]()
Здесь
![]() — масса электрона,
— масса электрона,![]() — количество протонов в ядре,
— количество протонов в ядре,![]() — электрическая постоянная,
— электрическая постоянная,![]() — заряд электрона.
— заряд электрона.
Именно такое выражение для энергии можно получить, применяя уравнение Шрёдингера в задаче о движении электрона в центральном кулоновском поле.
Радиус
первой орбиты в атоме водорода
R0=5,2917720859(36)·10−11
м[2],
ныне называется боровским радиусом,
либо атомной единицей длины и широко
используется в современной физике.
Энергия первой орбиты
![]() эВ представляет собой энергию ионизации
атома водорода.
эВ представляет собой энергию ионизации
атома водорода.
Полуклассическая теория Бора Основана на двух постулатах Бора:
Атом может находиться только в особенных стационарных или квантовых состояниях, каждому из которых отвечает определённая энергия. В стационарном состоянии атом не излучает электромагнитных волн.
Излучение и поглощение энергии атомом происходит при скачкообразном переходе из одного стационарного состояния в другое, при этом имеют место два соотношения:
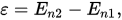 где
где
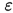 — излучённая (поглощённая) энергия,
— излучённая (поглощённая) энергия,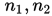 —
номера квантовых состояний. В
спектроскопии
—
номера квантовых состояний. В
спектроскопии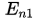 и
и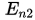 называются
термами.
называются
термами.Правило квантования момента импульса:
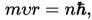
Далее исходя из соображений классической физики о круговом движении электрона вокруг неподвижного ядра по стационарной орбите под действием кулоновской силы притяжения, Бором были получены выражения для радиусов стационарных орбит и энергии электрона на этих орбитах:
![]()
![]() м
— боровский радиус.
м
— боровский радиус.
![]()
![]() —энергетическая
постоянная Ридберга (численно равна
13,6 эВ).
—энергетическая
постоянная Ридберга (численно равна
13,6 эВ).
Достоинства теории Бора:
Объяснила дискретность энергетических состояний водородоподобных атомов.
Теория Бора подошла к объяснению внутриатомных процессов с принципиально новых позиций, стала первой полуквантовой теорией атома.
Эвристическое значение теории Бора состоит в смелом предположении о существовании стационарных состояний и скачкообразных переходов между ними. Эти положения позднее были распространены и на другие микросистемы.
Объясняет границу таблицы Менделеева. Последний атом, способный существовать физически, имеет порядковый номер 137, так как, начиная со 138-го элемента 1s-электрон должен двигаться со сверхсветовой скоростью, что противоречит специальной теории относительности.
Недостатки теории Бора:
Не смогла объяснить интенсивность спектральных линий.
Справедлива только для водородоподобных атомов и не работает для атомов, следующих за ним в таблице Менделеева без экспериментальных данных (энергии ионизации или других).
Теория Бора логически противоречива: не является ни классической, ни квантовой. В системе двух уравнений, лежащих в её основе, одно — уравнение движения электрона — классическое, другое — уравнение квантования орбит — квантовое.
Теория Бора являлась недостаточно последовательной и общей. Поэтому она в дальнейшем была заменена современной квантовой механикой, основанной на более общих и непротиворечивых исходных положениях. Сейчас известно, что постулаты Бора являются следствиями более общих квантовых законов. Но правила квантования широко используются и в наши дни как приближённые соотношения: их точность часто бывает очень высокой.
