
- •Анализ лекарственных средств органического происхождения по функциональным группам
- •Введение
- •3. Прочие
- •2. Лекарственные вещества, содержащие фенольный гидроксил
- •3. Лекарственные вещества, содержащие карбонильную группу (альдегидную, кетонную)
- •4. Лекарственные вещества, содержащие карбоксильную группу
- •5. Лекарственные вещества, содержащие первичную ароматическую аминогруппу
- •6. Лекарственные вещества, содержащие ароматическую нитрогруппу
- •7. Лекарственные вещества, содержащие вторичную и третичную аминогруппы
- •8. Лекарственные вещества, содержащие сложноэфирную группу
- •9. Лекарственные вещества, содержащие амидную группу
- •10. Лекарственные вещества, содержащие имидную и сульфамидную группы
- •Эффект реакции барбитуратов с раствором меди сульфата
- •11. Лекарственные вещества, содержащие ковалентно связанный галоген
- •12. Лекарственные вещества, содержащие азометиновую группу, ковалентно связанную серу, пиридиновый цикл, ароматический радикал, непредельную связь
- •Специфические реакции
- •Литература
- •Содержание
3. Лекарственные вещества, содержащие карбонильную группу (альдегидную, кетонную)
Альдегидной называется группа, в которой карбонил связан с атомом водорода и углеводородным радикалом (алифатическим или ароматическим).
Кетонной называется группа, в которой карбонил связан с двумя углеводородными радикалами (алифатическими или ароматическими).
К карбонильным соединениям относятся вещества, содержащие α-кетольную группировку, которая включает связанные между собой кетонную и спиртовую группы.
Альдегидную группу содержат формальдегид, глюкоза, хлоралгидрат, пиридоксальфосфат. Ряд лекарственных веществ образует альдегид при гидролитическом разложении (гексаметилентетрамин, никодин, анальгин, гексамидин).
Кетогруппа входит в структуру кортикостероидов (дезоксикортикостерон ацетат, кортизон ацетат, гидрокортизон, преднизолон, дексаметазон), гестагенных гормонов (прегнин, прогестерон); андрогенных гормонов (тестостерон пропионат, метилтестостерон, метандростенолон); бициклических терпенов (камфора, бромкамфора, кислота сульфокамфорная, сульфокамфокаин).
α-кетольную группировку содержат гормоны коркового слоя надпочечников и их полусинтетические аналоги.
Химические свойства соединений, содержащих альдегидную группу, определяются её строением: дипольным моментом карбонила, эффективным положительным зарядом на атоме углерода карбонила, поляризуемостью двойной связи(электронная плотность смещается к кислороду и на нем возникает дробный отрицательный заряд), что обуславливает высокую реакционную способность альдегидов.
Типы реакций, используемых для идентификации альдегидов:
ОВР: альдегиды проявляют сильные восстановительные свойства в щелочной среде, окисляются до соответствующих кислот.
Реакции конденсации.
Реакции присоединения: взаимодействие с бисульфитом натрия, фуксинсернистой кислотой. Кетоны этой реакции не дают.
Реакции замещения: на атоме углерода расположен центр электрофильности. Альдегиды и кетоны реагируют с нуклеофильными реагентами. В эту группу входят реакции конденсации альдегидов с фенолами, реакции конденсации альдегидов и кетонов с аминами и гидразинами.
Реакции полимеризации: эти реакции характерны для альдегидов, но в качестве анализа не используются.
В анализе ЛВ, содержащих альдегидную группу, наибольшее значение имеют реакции окисления, конденсации с фенолами, аминами и их производными.
Кетоны менее реакционноспособны. В отличие от альдегидов они окисляются только в жёстких условиях. Наибольшее практическое значение для ЛВ, содержащих кетогруппу, имеют реакции конденсации с аминами и их производными.
Идентификация
3.1. Реакция окисления
Лекарственные вещества, содержащие альдегидную группу, окисляются до карбоновых кислот с тем же числом атомов углерода, что и исходный альдегид.
Окисление происходит даже под действием слабых окислителей: йода, растворов комплексных соединений серебра, меди, ртути в щелочной среде при нагревании. Ионы серебра (I), меди (II) и ртути (II) восстанавливаются до свободных металлов или их оксидов, образуя окрашенные осадки, раствор йода обесцвечивается.
а) Реакция с аммиачным раствором нитрата серебра (реакция серебряного зеркала)
AgNO3 + 2NH4OH → [Ag(NH3)2]NO3 +2H2O
НСОН + 2[Ag(NH3)2]NO3 + H2O → HCOONH4 + 2Ag↓+ 2NH4NO3+ NH3↑
Формальдегид, окисляясь до аммонийной соли муравьиной кислоты, восстанавливает до металлического серебра, которое осаждается на стенках пробирки в виде «зеркала» или серого осадка.
б) Реакция с реактивом Фелинга (комплексное соединение меди (II) с калий-натриевой солью винной кислоты). Альдегиды восстанавливают соединение меди (II) до оксида меди (I), образуется кирпично-красный осадок.
При сливании реактивов Феллинга 1 и 2 идут следующие реакции:

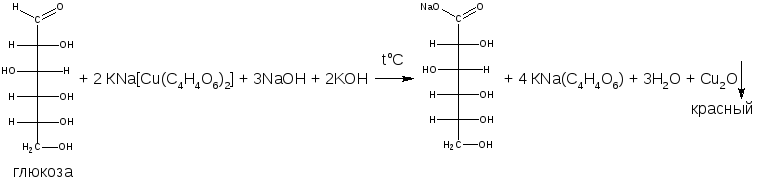
в) Реакция с реактивом Несслера (щелочной раствор тетрайодмеркурат (II) калия). Формальдегид восстанавливает ион до металлической ртути – осадок темно-серого цвета.
НСОН + K2[HgI4] + 3KOH → НСООК + Hg↓+ 4KI + 2H2O
Аналогичные реакции с перечисленными реактивами дают соединения с α-кетольной группировкой. Реакция протекает по схеме:
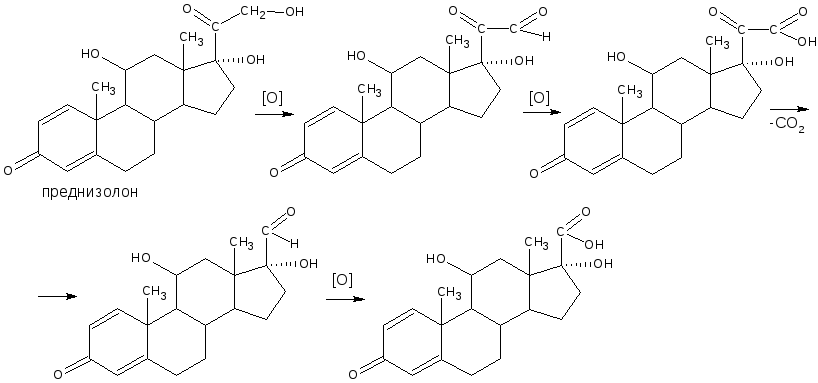
3.2. Реакции конденсации
3.2.1. C фенолами (характерна для альдегидов). В присутствии концентрированной серной кислоты образуется бесцветный продукт конденсации, при последующем окислении которого получаются интенсивно окрашенные соединения хиноидной структуры. В качестве реактивов используется салициловая или хромотроповая кислоты.
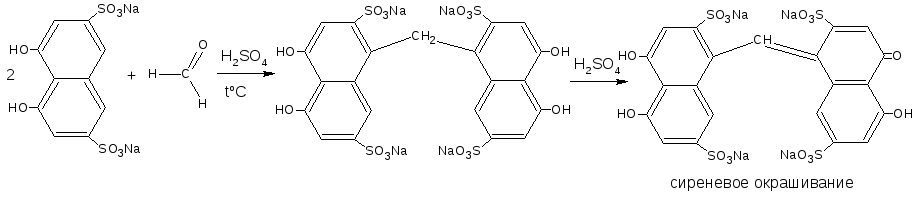
Реакция используется для доказательства раствора формальдегида и веществ, гидролизующихся с его образованием (никодин, анальгин, гексаметилентетрамин, гексамидин).
3.2.2. С аминами или их производными (характерны для ЛВ, содержащих как альдегидную, так и кетонную группы). В качестве реактивов используются соединения с первичной ароматической аминогруппой, производные гидразина – фенилгидразин, 2,4 – динитрофенилгидразин; гидроксиламин. При этом образуются соединения с азометиновой связью – основания Шиффа, гидразоны, оксимы, которые характеризуются определенной температурой плавления, разложения или окраской.

Реакция чаще используется для идентификации соединений с первичной ароматической аминогруппой (фенилгидразин).
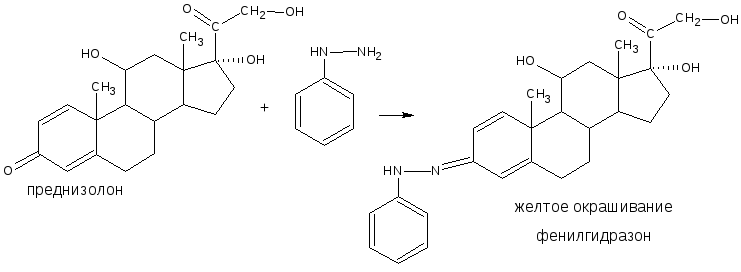
Реакция с фенилгидразином используется также для идентификации кортизона ацетата, преднизона, пиридоксальфосфата.
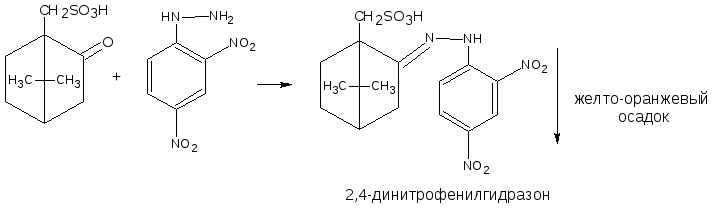
Реакция рекомендуется для подтверждения подлинности прогестерона, метандростенолона, кислоты сульфокамфорной.
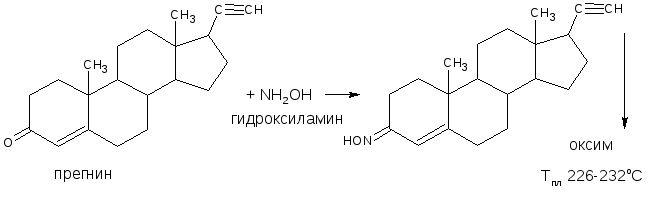
Реакция является фармакопейной для прегнина, метилтестостерона, тестостерона пропионата.
3.3. Реакции присоединения
К этой группе относится реакция с фуксинсернистой кислотой. Эта кислота бесцветна, но при добавлении вещества с альдегидной группой образуется хиноидная структура красно-фиолетового цвета, при подкислении окраска исчезает. Исключение составляет формальдегид, так как в его присутствии окраска сохраняется:
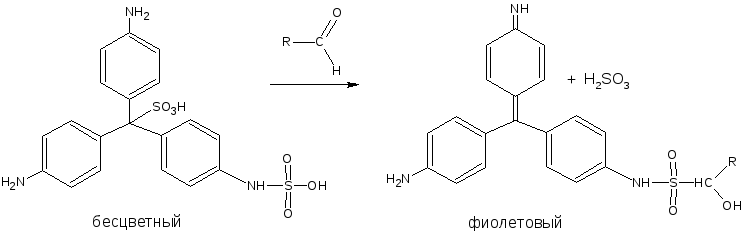
Количественное определение
3.4. Йодометрический метод обратного титрования (формальдегид, глюкоза, никодин).
Метод основан на свойстве альдегидов окисляться йодом в щелочной среде до кислоты. Йод взаимодействует с натрия гидроксидом с образованием натрия гипойодида, являющегося сильным окислителем.
I2 + 2NaOH → NaIO + NaI + H2O
Гипойодид натрия окисляет альдегид до кислоты.
HCOH + NaIO → HCOONa + NaI + H2O
Затем прибавляют избыток кислоты серной для выделения из непрореагировавшего гипойодида натрия йода, который оттитровывают раствором натрия тиосульфата.
NaIO + NaI + H2SO4 → I2 + Na2SO4 + H2O
Суммарно:
HCOH + I2 + 3NaOH → HCOONa + 2NaI + 2H2O
I2 + 2Na2S2O3 → 2NaI + Na2S4O6
M.э. = ½ М.м.
Никодин предварительно подвергают гидролизу и образующийся формальдегид определяют йодометрическим методом.
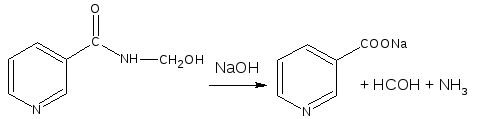
M.э. = ½ М.м.
3.5. Оксимный метод
Используется в двух вариантах. Метод основан на свойстве кетонов образовывать с гидроксиламина гидрохлоридом оксим с выделением эквивалентного количества кислоты хлористоводородной. Дальнейшее определение проводят по кислоте алкалиметрическим методом (косвенное определение) или по оксиму, осадок которого отфильтровывают, промывают, высушивают до постоянной массы и взвешивают (гравиметрия).
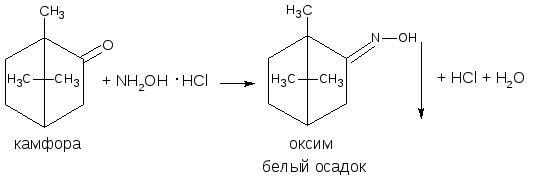
HCl + NaOH → NaCl + H2O
М.э.= М.м.
3.6. Фотоколориметрия и спектрофотометрия
Для получения окрашенных соединений используют реакцию конденсации с фенолами, 2,4-динитрофенилгидразином.
