- •2 Кислотно-основные методы
- •2.1 Краткие теоретические основы метода
- •2.1.1 Кислотно-основное взаимодействие
- •Классификация кислот и оснований в зависимости от величины их рКа
- •Величины рКа оснований в различных растворителях
- •2.1.2 Титрованные растворы
- •Титранты кислотно-основного метода
- •2.1.3 Установление конца титрования с помощью визуальных индикаторов
- •Интервал перехода окраски и показателя титрования кислотно-основных индикаторов
- •Данные для эмпирического выбора индикатора при кислотно-основном титровании
- •Интервалы рН и изменение цвета индикаторов (гф XI, вып.2, стр. 102)
- •2.1.4 Определение ингредиентов многокомпонентных лекарственных форм
- •2.1.5 Варианты и способы кислотно-основного титрования
- •2.2 Ацидиметрия
- •2.2.1 Вариант нейтрализации
- •2.2.2 Вариант вытеснения
- •2.2.3 Вариант гидролитического разложения
- •2.3.2 Вариант вытеснения
- •2.3.3 Вариант гидролитического разложения
- •2.3.4 Косвенное титрование
- •Соле- и комплексообразование
- •Конденсация
- •2.4 Титрование в неводных растворителях
- •Примеры дифференцирующего действия растворителя
- •Пример нивелирующего действия растворителя
- •2.4.1 Титрование в среде протогенных растворителей. Ацидиметрия
- •Определение кофеина
- •Определение изониазида
- •Определение дибазола
- •Определение атропина сульфата
- •2.4.2 Титрование в среде протофильных растворителей. Алкалиметрия
- •Определение теобромина
- •Определение фталазола
2.2 Ацидиметрия
2.2.1 Вариант нейтрализации
Вариант нейтрализации – основан на свойстве неорганических и органических оснований вступать во взаимодействии с кислотами с образованием солей.
По данному варианту определяют основания, например, аммиак, гексаметилентетрамин, кодеин, цитизин, этилендиамин в эуфиллине.
Способ титрования – прямой.Конец титрования устанавливают в случае определения слабых оснований (гексаметилентетрамин), используя смешанный индикатор (метиловый оранжевый + метиленовый синий), при анализе более сильных оснований применяют метиловый красный (кодеин, цитизин) или метиловый оранжевый (аммиак, этилендиамин в эуфиллине).
Примеры
Этот вариант используется для определения гексаметилентетрамина в лекарственных формах, который реагирует как однокислотное основание.
(CH2)6N4+HCl→ (CH2)6N4×HClЭ = М.м.
Вариант нейтрализации лежит в основе количественного определения этилендиамина – компонента эуфиллина:
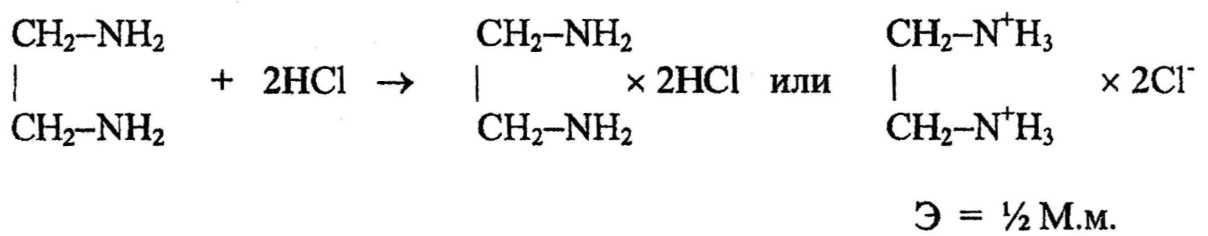
По способу обратного титрованиявозможно определение магния окиси:
MgO+ 2HCl→MgCl2+H2O
Э = ½ М.м.
HCl+NaOH→NaCl+H2O
Индикатор метиловый красный
2.2.2 Вариант вытеснения
Вариант вытеснения – основан на вытеснении сильной кислотой (титрант) слабой кислоты из её соли. Он применяется для определения солей слабых кислот и сильных оснований (неорганических и органических): натрия гидрокарбоната, натрия тетрабората, калия ацетата, натрия салицилата и бензоата, в том числе в составе кофеин-бензоата натрия, натриевых солей производных барбитуровой кислоты и сульфамидных препаратов, пара-аминосалицилат натрия и др.
Определение проводят по способу прямого титрования. В качестве индикатора используют метиловый оранжевый или смешанный индикатор.
Примеры
NaHCO3+HCl→NaCl+CO2↑ +H2OЭ = М.м.
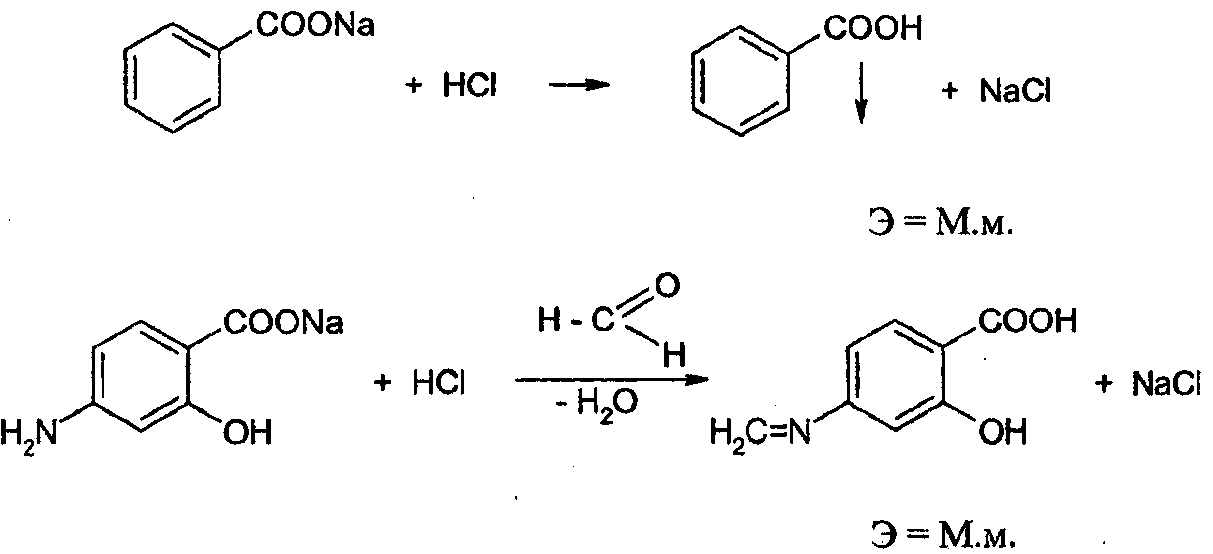
Формальдегид вводят с целью блокирования аминогруппы, проявляющей основные свойства.
Определение натрия бензоата и салицилата проводят в присутствии несмешивающегося с водой органического растворителя (эфир), который извлекает образующиеся кислоты и подавляет их диссоциацию.
Титрование натриевых солей барбитуровой кислоты (барбитал натрий, этаминал-натрий, гексенал) и сульфаниламинодов (соли более слабых кислот) проводят без добавления органических растворителей.
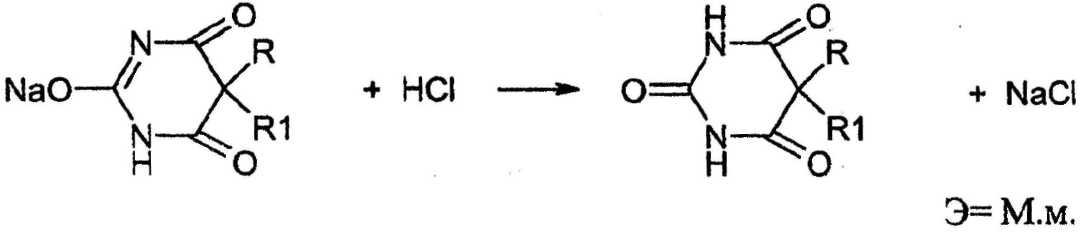
На результат титрования таких солей как барбитал-натрий, эуфиллин оказывает влияние углекислота, так как она может вытеснять из этих солей слабые кислоты. Поэтому вода, используемая для растворения навески, должна быть свободной от углекислоты (свежепрокипяченной).
2.2.3 Вариант гидролитического разложения
По этому варианту, согласно действующей ФС, определяют гексаметилентетрамин.
Способ титрования – обратный, индикатор метиловый красный.
Параллельно проводят контрольный опыт. Для этого отдельно титруют щелочью тот объем кислоты, который введен в реакцию с определяемым веществом. По разности в объемах щелочи, пошедший на контрольный и основной опыты определяют количество кислоты, связавшейся с анализируемым веществом.
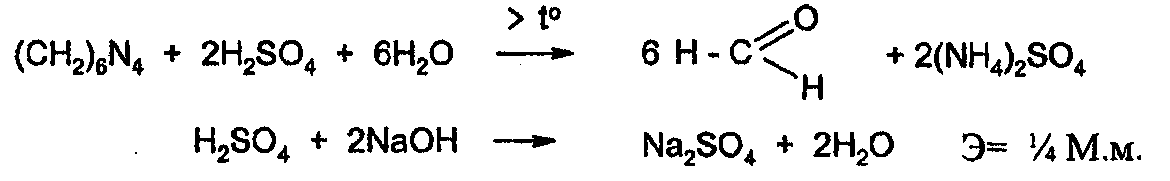
2.2.4 Косвенное титрование
Метод Къельдаля
К косвенному способу титрования следует отнести метод определения азотсодержащих лекарственных веществ, получивший название метода Къельдаля. Метод Къельдаля сочетает процесс получения из лекарственного вещества летучего амина, перегоняемого с водяным паром, который образует с борной кислотой соль, определяемую затем ацидиметрически (вариант вытеснения). Метод Къельдаля может осуществляться в классическом и модифицированном вариантах.
Подробно метод Къельдаля рассмотрен в разделе 8
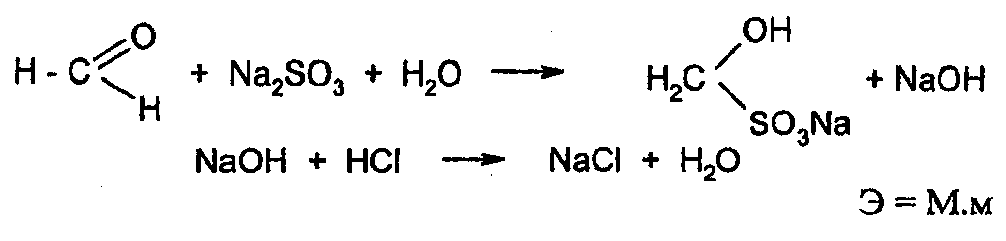
Вариант присоединения
Этот метод является специфичным для формальдегида. Метод основан на свойстве альдегидов вступать в реакции присоединения по карбонильной группе. Присоединение формальдегидом сульфида натрия протекает стехиометрично, в результате образуется сульфитное производное и эквивалентное количество щелочи, которую оттитровывают раствором кислоты хлористоводородной (индикатор – фенолфталеин).
2.3 Алкалиметрия
2.3.1 Вариант нейтрализации
Вариант нейтрализации основан на свойстве неорганических и органических кислот взаимодействовать со щелочами с образованием солей. Титрование, за редким исключением, прямое. Конец титрования устанавливают в случае определения слабых кислот (барбитураты, сульфаниламиды), используя тимолфталеин, более сильных – феноловый красный, фенолфталеин или метиловый оранжевый.
По этому варианту определяют:
Сильные неорганические кислоты,например, кислоту хлористоводородную:
HCl+NaOH→NaCl+H2OЭ = М.м.
Слабые неорганические кислоты, например, кислоту борную (КДисс= 5,75×10-10). При титровании этой кислоты щелочью образуются сильно гидролизующиеся соли и щелочная реакция в растворе появляется значительно раньше достижения точки эквивалентности.
H3BO3+NaOH→NaBO2+ 2H2O
NaBO2+ 2H2O
![]() NaOH+H3BO3
NaOH+H3BO3
Для усиления кислотных свойств кислоты борной используют её свойство реагировать с многоатомными спиртами с образованием более сильных, чем борная, комплексных кислот, которые можно точно титровать по фенолфталеину. С этой целью, как правило, используют нейтрализованный глицирин, при этом образуется более сильная глицероборная кислота:
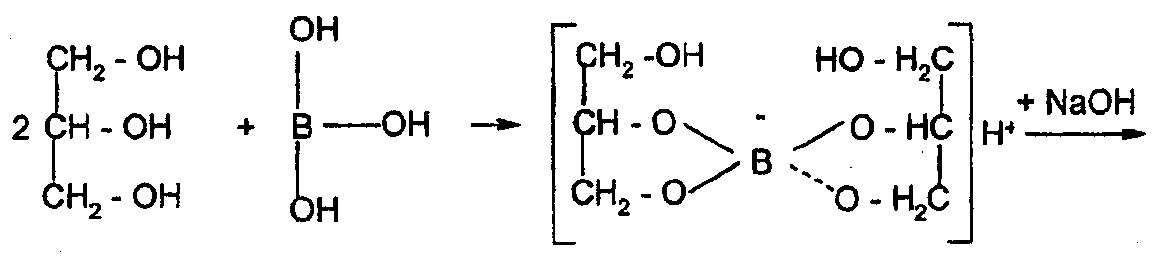
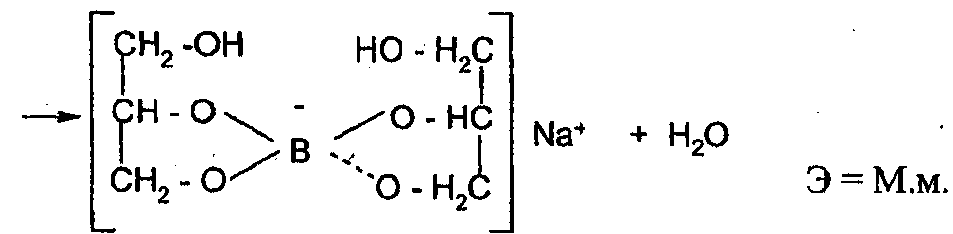
Глицерин вводится в избытке для связывания всей борной кислоты и подавления гидролиза натриевой соли глицероборной кислоты. При недостатке глицерина эта соль может гидролизоваться, вследствие чего среда становится щелочной раньше достижения точки эквивалентности. Учитывая это, в конце титрования после появления розовой окраски индикатора добавляют еще глицерин. Сохранение окраски свидетельствует о конце титрования. Если она исчезает, титрование продолжают до появления устойчивой розовой окраски.
Карбоновые кислотыв большинстве своем относятся к слабым кислотам ( Кдисс= 10-5– 10-4), как правило, нерастворимы в воде, поэтому их предварительно растворяют в спирте или ацетоне, нейтрализованных по применяемому в данном определении индикатору. Так, например, анализируют кислоты: салициловую, бензойную, никотиновую, мефенамовую, ацетилсалициловую, ибупрофен.
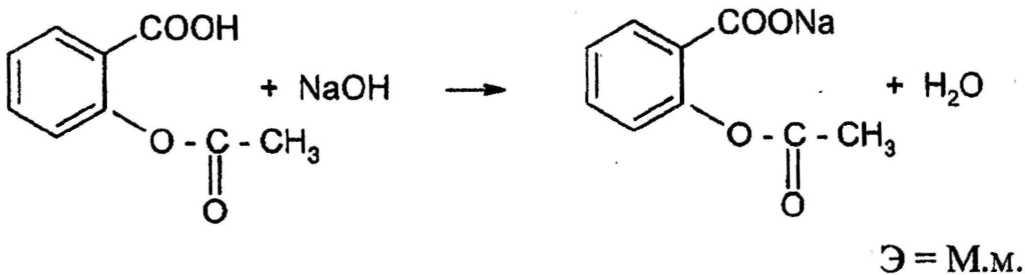
При определении кислоты ацетилсалициловой необходимо учитывать возможность гидролиза по сложноэфирной связи, для предупреждения которого титрование проводят быстро. Навеску растворяют в охлажденном до 8 - 10°С спирте.
Аминокислоты алифатического ряда.Они являются амфотерными соединениями, так как содержат карбоксильную группу, проявляющую кислотные свойства, и аминогруппу, обладающую основными свойствами. В водных растворах аминокислоты образуют внутренние соли за счет собственных амино- и карбоксильной группы (H3N+-CH2-COO-), поэтому алкалиметрическое определение затруднено. Для анализа аминокислот используют формольный метод Серенса, в котором для связывания (блокирования) аминогруппы к ним добавляют формалин. ОбразующеесяN-метиленовое производное титруют щелочью по фенолфталеину или тимолфталеину. Так определяют аминалон, метионин, цистеин, аминокапроновую кислоту.
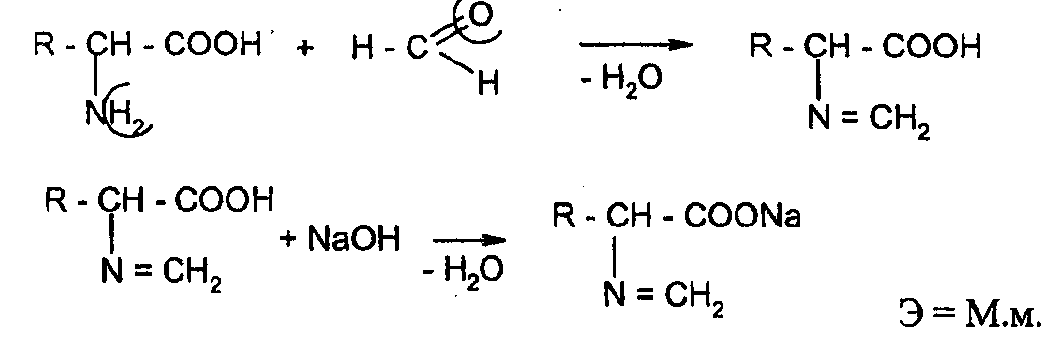
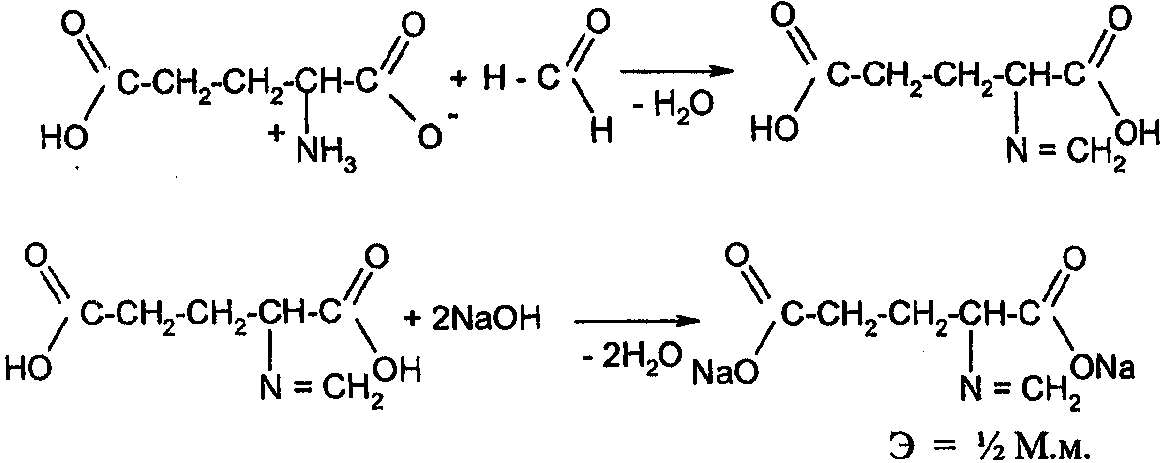
Кислота глютаминовая содержит две карбоксильные группы, поэтому в зависимости от условий анализа может титроваться как одноосновная или как двухосновная. При титровании раствором щелочи в присутствии бромтимолового синего или нейтрального красного (без формалина) во взаимодействие вступает только свободная карбоксильная группа, т.к. рКАэтой группы равен 4,25, рКАвторой карбоксильной группы равен 2,19.
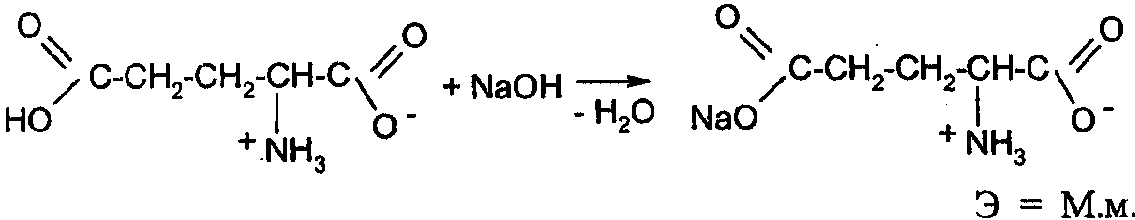
В присутствии формалина или органических растворителей (ацетон) глютаминовая кислота титруется как двухосновная по индикатору фенолфталеину:
Барбитураты, сульфаниламиды.Барбитураты (барбитал, фенобарбитал), вследствие наличия в структуре имидных групп, существуют в растворах в двух таутомерных формах имидной (I) и имидольной (II):
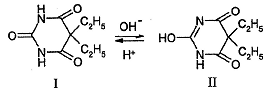
Имидольная форма обладает слабыми кислотными свойствами и может реагировать со щелочами с образованием соли.
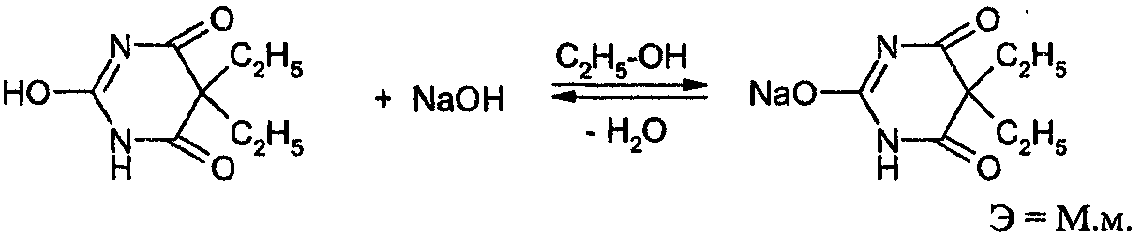
Кислотный характер сульфаниламидов (норсульфазол) обусловлен смещением электронной плотности в сторону электроотрицательных атомов кислорода сульфогруппы, которая приводит к тому, что водород при атоме азота становится подвижным, образуется таутомерная форма, обладающая слабыми кислотными свойствами.
![]()
![]()
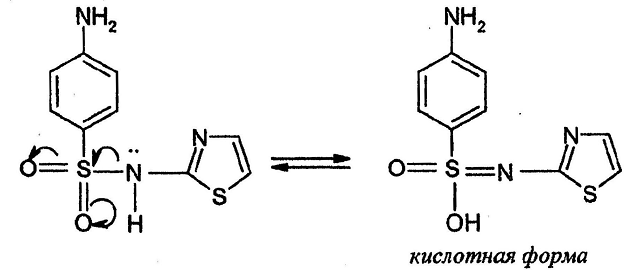
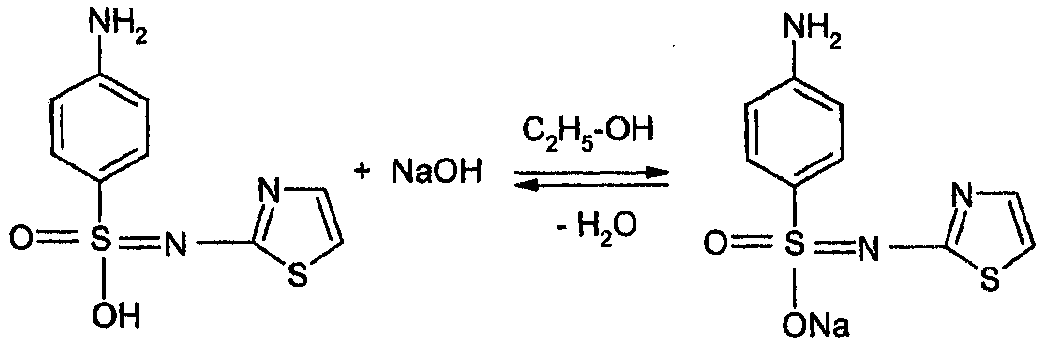
Э = М.м.
Так можно определить норсульфазол, сульфадимезин, сульфален, этазол.
При определении фталазола (обратное титрование) нейтрализация идет по сульфамидной и карбоксильной группам.
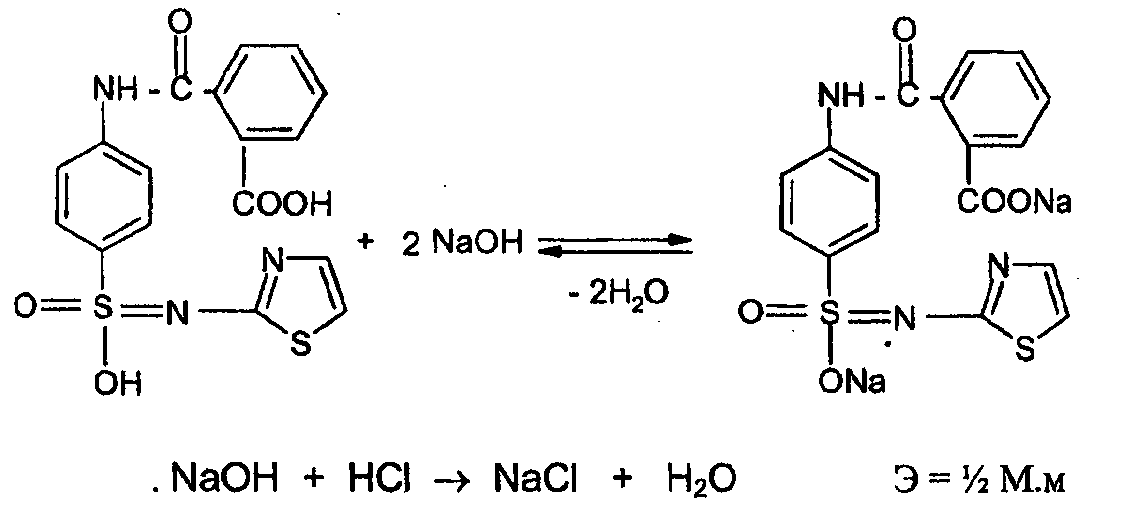
Определение проводят в присутствии органического растворителя, индикатор тимолфталеин или смешанный (тимоловый синий и фенолфталеин 1 : 1).
Кислые соли многоосновных кислот, например, натрия гидроцитрат.
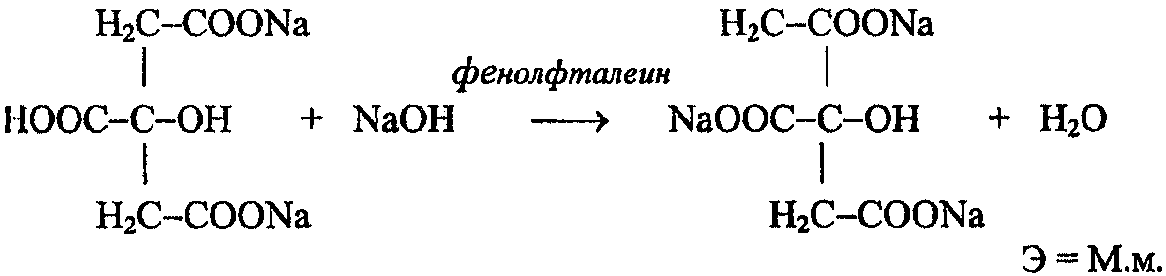
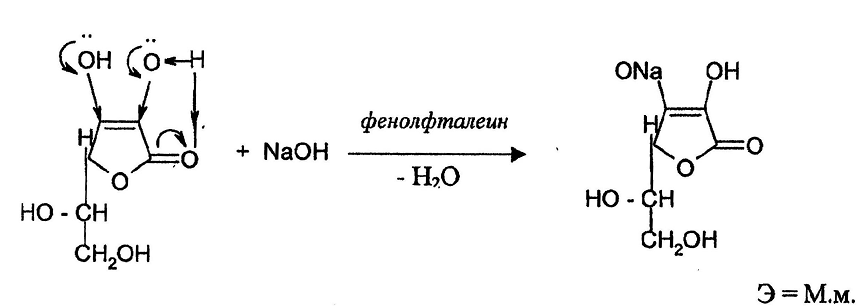
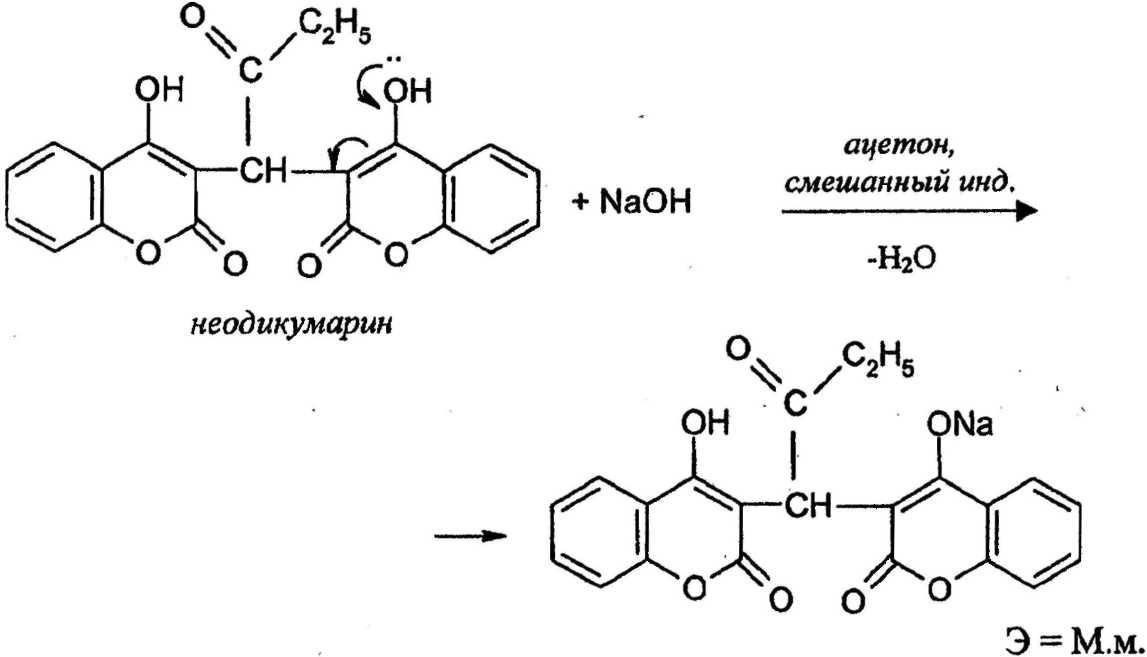
Вещества, содержащие енольный гидроксил(кислота аскорбиновая, бутадион, неодикумарин, фепромарон).
Енольные гидроксилы придают лекарственным веществам кислотные свойства вследствии эффекта сопряжения неподеленных электронных пар кислородного атома с π-электронами двойной связи.

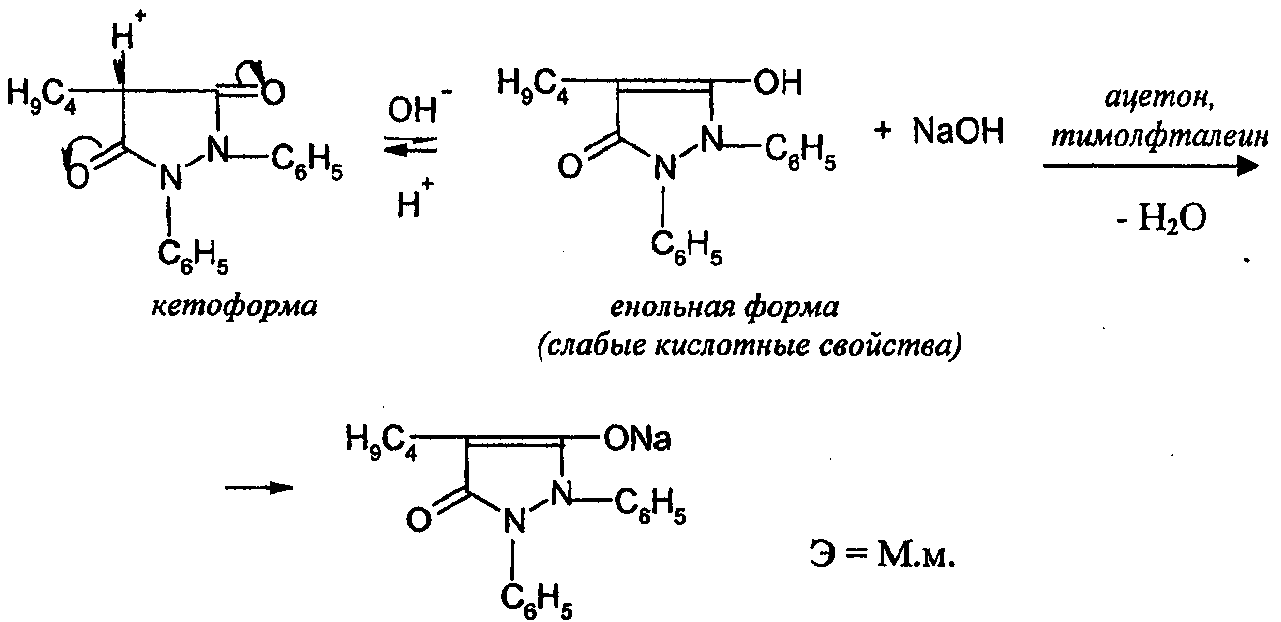
Кислотные свойства бутадиона обусловлены кето-енольной таутомерией.
Кислота аскорбиновая содержит ендиольную группировку в положении 2,3. Сопряжение карбонильной группы с двойной связью усиливает кислотность ендиольных групп. Кислород карбонильной группы (сильно электроотрицательный элемент) образует водородную связь с атомом водорода гидроксильной группы при С2, поэтому взаимодействие с натрия гидроксидом идет только по гидроксилу при С3.