
- •Ароматические кислоты и их соли производные салициловой кислоты
- •Химические свойства
- •Кислота бензойная Натрия бензоат
- •Получение
- •Описанне
- •Растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Салициловая кислота и ее производные
- •Кислота салициловая Натрия салицилат
- •Получение
- •Описанне
- •Растворимость
- •Подлинность
- •6. Реакции электрофильного замещения (на фенольный гидроксил).
- •Чистота
- •Количественное определение
- •1.Методы кuслотно-основного титрования.
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Примененне
- •Сложные эфиры салициловой кислоты
- •Получение
- •Описание
- •Растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Примененне
Хранение
В сухом, защищенном от света месте, чтобы предотвратить окисление салициловой кислоты за счет фенольного гидроксила, при комнатной температуре, в хорошо укупоренной таре, учитывая возможность возгонки кислоты салициловой. Натрия салицилат - список Б.
Применение
Кислоту салициловую применяют наружно как антисептическое, отвлекающее, раздражающее и кератолитическое средство в мазях 1 %10%, пастах, спиртовых растворах 1% и 2%.
Натрия салицилат оказывает противовоспалительное, жаропонижающее, болеутоляющее и противоревматическое действие, при остром ревматизме, ревматическом эндокардите и миокардите.
ПРОИЗВОДНЫЕ САЛИЦИЛОВОЙ КИСЛОТЫ
этой группе могут быть отнесены
сложные эфиры (I) и амиды (II) салициловой кислоты
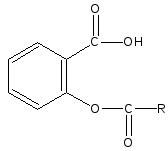
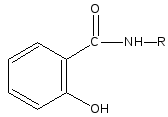
III
АМИДЫ САЛИЦИЛОВОЙ КИСЛОТЫ
|
Структура. Химическое название |
Строение и названияФГ |
МИН, латинское название. Формы выпуска. Фармакологическое действие |
|
Осалмид (Оксафенамид) п-оксифенилсалициламид (2-гидрокси –N - (4гидроксифенил ) бензамид ) |
Амидная группа – - C – NН - ║ О Фенольный гидроксил - ОН |
Osalmid Oxaphenamidum Субстанция, таблетки 0,25-0,5 Желчегонное средство
|
Получение
Осалмuд получают сплавлением фенилсалицилата с п-аминофенолом


+
2


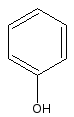
 +
+
Описание
Белый или белый с лиловато-серым оттенком порошок, без запаха.
Растворимость
Практически не растворим в воде. Легко растворим в спирте, растворах гидроксидов щелочных металлов.
Подлинность
1) ФС ИК-спектр поглощения осалмида в области 4000-400 см- (в диске с КВr) должен полностью совпадать с прилагаемым к ФС рисункам спектра.
2) ФС УФ-спектр поглощения в области 220-360 нм. Раствор осалмида в этаноле имеет максимум при 289±2 нм.
3) Температура плавления.
Реакции подлинности
1. ГФ с раствором железа (III) хлорида красно-фиолетовое окрашивание. Т.к. имеет свободные фенольные гидроксилы,

2. ГФ Реакции гидролитического разложения. Кипятят с НСI конц.
Осалмид (по амидной группе) при гидролизе в кислой среде разлагается на салициловую кислоту и п-аминофенол. Выделившийся п-аминофенол легко окисляется кислородом воздуха до п-хинонимина и конденсирует в щелочной среде с резорцином, образуя индофенолят натрия окрашенный в синий цвет, а в кислой среде индофеноловый краситель (красно-фиолетовое окрашивание).



Чистота
Примеси характеризующие общую степень очистки (хлориды, сульфаты, т.Ме и сульфатная зола, прозрачность и цветность (допускается опалесценция) и т.д.)
Специфические примеси
Примесь п-аминофенола (продукт синтеза осалмида) обнаруживают
ФС методом ТСХ на пластинках «Silufol»: должно быть одно пятно, не превышающее по величине и интенсивности пятно свидетеля.
или после извлечения его водой из препарата (препарат не растворим в воде) по реакции с резорцином (не д.б. фиолетового окрашивания).
Количественное определение
Метод Кьельдаля (метод определения общего азота), основанный на разложении азотсодержащих органических веществ с последующим количественным определение выделившегося аммиака. Осалмид сжигают (t°) в течении 3 часов с Н2SО4 конц. Происходит минерализация, органическое вещество кипит с серной кислотой и разрушается до CO2, Н2О, NН3, который связывается серной кислотой в (NН4)2SО4.
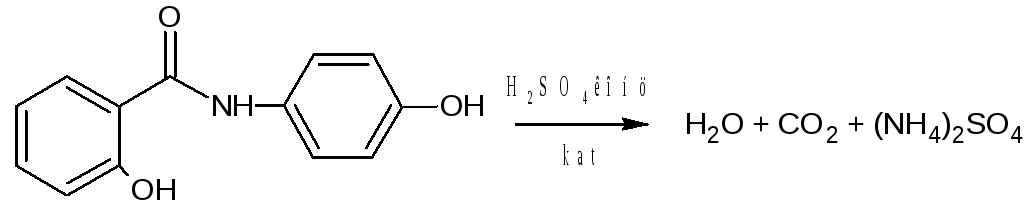
Затем добавляют 30% NаОН. Выделившийся аммиак отгоняют с водяным паром в приемник с борной кислотой, где образуется смесь солей мета- и тетра-борной кислот (можно NН3 ∙ Н3ВО3). После сбора отгона добавляют индикатор м/о+ м/с и титруют НСl.

f экв = 1
МФ. Алкалиметрия в среде протофильного растворителя.
Метод основан на солеобразовании осалмида, проявляющего слабые кислотные свойства за счёт фенольных гидроксилов -ОН в молекуле с титрантом в среде протофильного растворителя, усиливающего кислотные свойства анализируемого вещества. Растворитель диметилформамид, титрант - метилат натрия. f экв, (осалмида) = 1/2
O
CH3
+
2 C – N
H
CH3


![]()




OН+
CH3
+
2 C – N + 2CH3ONa
H
CH3






+
2HC3O-


O
CH3
2
C – N
H
CH3
OН+
CH3
2
C – N + 2CH3O-
H
CH3
+
2CH3OH









Конечную точку титрования (т.э.) определяют потенциометрически (индикатор стеклянный электрод).
Таблетки осалмида СФМ (ФС)
ФЭК по реакции с раствором железа (III) хлорида

