
Часть 2
.PDFГлава 6. Иммунопатологические процессы |
223 |
гастрита и энтерита, цирроз печени, ожоговая болезнь, аллергическая анемия, тромбоцитопения, агранулоцитоз, лекарственная аллергия.
Иммунодефицитные синдромы
Иммунодефицитные синдромы — крайнее проявление недостаточности иммунной системы. Они могут быть первичными, обусловленными недоразвитием (гипоплазией, аплазией) иммунной системы — наследственными и врожденными, или вторичными (приобретенными), возникающими в связи с болезнью или проводимым лечением.
Первичные иммунодефицитные синдромы
Первичные иммунодефицитные синдромы являются выражением недостаточности клеточного и гуморального иммунитета, клеточного иммунитета, гуморального иммунитета.
Синдромы недостаточности клеточного и гуморального иммунитета — комбинированные синдромы у детей и новорожденных, которые наследуются по аутосомно-доминантному типу (агаммаглобулинемия швейцарского типа, или синдром Гланцманна–Риникера; атаксия-телеангиэктазия ЛуиБар). При них находят гипоплазию как вилочковой железы, так и периферической лимфоидной ткани (табл. 6-1), которая и определяет дефект клеточного и гуморального иммунитета. В связи с несостоятельностью иммунитета у таких детей часто возникают инфекционные заболевания, которые имеют рецидивирующее течение и дают тяжелые осложнения (пневмонию, менингит, сепсис), отмечают задержку физиологического развития. При комбинированных иммунодефицитных синдромах часто возникают пороки развития и злокачественные мезенхимальные опухоли (атаксия-телеангиэктазия Луи-Бар).
Синдромы недостаточности клеточного иммунитета в одних случаях наследуются по аутосомно-доминантному типу (иммунодефицит с ахондроплазией, или синдром Мак-Кьюсика), в других — врожденные синдромы (агенезия или гипоплазия вилочковой железы, или синдром Дайджорджа). Помимо агенезии или гипоплазии вилочковой железы и Т-зависимых зон периферической лимфоидной ткани, что определяет дефицит клеточного иммунитета, для этих синдромов характерны множественные пороки развития. Дети погибают от пороков развития либо от осложнений инфекционных заболеваний.
Синдромы недостаточности гуморального иммунитета имеют наследственную природу, причем установлено сцепление их с Х-хромосомой. Болеют дети первых пяти лет жизни. Для одних синдромов (агаммаглобулинемии, сцепленной с Х-хромосомой, или синдрома Брутона) характерна потеря способности к синтезу всех иммуноглобулинов, что морфологически подтверждают отсутствием В-зависимых зон и клеток плазмоцитарного ряда в периферической лимфоидной ткани, прежде всего в лимфатических узлах и селезенке. Другим синдромам свойствен дефицит одного из иммуноглобулинов (например, избирательный дефицит IgA, или синдром Веста), тогда структура лимфоидной ткани остается сохранной. Однако при всех

Таблица 6-1. Первичные иммунодефицитные синдромы
Синдром |
Тип |
Клинико-морфологические |
Иммунные |
|
наследования |
проявления |
нарушения |
|
|
|
|
Комбинированные |
|
|
|
иммунодефицитные синдромы |
|
|
|
Комбинированный тип |
Аутосомно-рецессивный |
Гипоплазия вилочковой |
Тотальный дефект |
Гланцманна−Риникера, |
|
железы и периферической |
клеточного и гуморального |
или агаммаглобулинемия |
|
лимфоидной ткани, |
иммунитета, потеря |
швейцарского типа |
|
лимфопения, частые |
способности синтезировать |
|
|
инфекционные |
иммуноглобулины |
|
|
заболевания |
|
Атаксия-телеангиэктазия |
То же |
Гипоплазия вилочковой |
Дефект клеточного |
Луи-Бар |
|
железы и периферической |
иммунитета, недостаток |
|
|
лимфоидной ткани, |
иммуноглобулинов, частый |
|
|
лимфопения, атрофия |
дефицит IgA |
|
|
коры мозжечка (атаксия), |
|
|
|
телеангиэктазия |
|
|
|
бульбарной конъюнктивы, |
|
|
|
мезенхимальные |
|
|
|
злокачественные |
|
|
|
опухоли, |
|
|
|
рецидивирующая |
|
|
|
пневмония |
|
Комбинированный тип с |
То же |
Гипоплазия вилочковой |
Содержание |
наличием В-лимфоцитов и |
|
железы и периферической |
иммуноглобулинов |
иммуноглобулинов (синдром |
|
лимфоидной ткани, |
нормальное, возможна |
Незелофа) |
|
лимфопения, сепсис |
дисгаммаглобулинемия. |
|
|
|
Дефект клеточного |
|
|
|
иммунитета |
|
|
|
|
224
анатомия патологическая Общая

|
|
|
Окончание табл. 6-1 |
|
|
|
|
Синдром |
Тип |
Клинико-морфологические |
Иммунные |
|
наследования |
проявления |
нарушения |
|
|
|
|
Синдромы недостаточности |
|
|
|
клеточного иммунитета |
|
|
|
Агенезия или гипоплазия |
Неизвестен |
Отсутствие вилочковой |
Содержание |
вилочковой железы (синдром |
|
железы и околощитовидных |
иммуноглобулинов |
Дайджорджа) |
|
желез (тетания), |
нормальное. Дефект |
|
|
Т-лимфоцитов |
клеточного |
|
|
|
иммунитета |
|
|
|
|
Синдромы недостаточности |
|
|
|
гуморального иммунитета |
|
|
|
Агаммаглобулинемия, |
То же |
Структура лимфоидной |
Дефект гуморального |
сцепленная с Х-хромосомой |
|
ткани и вилочковой железы |
иммунитета, потеря |
(синдром Брутона) |
|
сохранена |
способности к синтезу |
|
|
|
иммуноглобулинов. |
Избирательный дефицит IgA |
|
Проявления аллергии. Частые |
Потеря способности к синтезу |
(синдром Веста) |
|
инфекции дыхательных |
IgA |
|
|
путей и желудочно- |
|
|
|
кишечного тракта в |
|
|
|
сочетании с аутоиммунными |
|
|
|
заболеваниями, синдром |
|
|
|
нарушенного всасывания, |
|
|
|
иногда с опухолями |
|
Сцепленный с Х-хромосомой |
|
Отсутствие В-зависимых |
|
клеток плазмоцитарного ряда |
|
зон в лимфатических |
|
|
|
узлах и селезенке, частные |
|
|
|
инфекционные заболевания |
|
|
|
|
|
процессы Иммунопатологические .6 Глава
225
226 |
Общая патологическая анатомия |
синдромах недостаточности гуморального иммунитета развиваются тяжелые бактериальные инфекции с преобладанием гнойно-деструктивных процессов в бронхах и легких, желудочно-кишечном тракте, коже, ЦНС, нередко заканчивающихся сепсисом.
Синдромы недостаточности системы моноцитарных фагоцитов и нейтрофилов — наследственные заболевания и синдромы: хроническая гранулематозная болезнь, синдромы Чедиака–Хигаси и Джоба.
Вторичные иммунодефицитные синдромы
Вторичные (приобретенные) иммунодефицитные синдромы возникают в связи с болезнью или определенным видом лечения.
Среди заболеваний, ведущих к недостаточности иммунной системы, основное значение имеет безудержно распространяющийся во многих странах мира СПИД — самостоятельное заболевание, вызываемое определенным вирусом. К вторичным иммунодефицитным синдромам ведут и другие инфекции, лейкозы, злокачественные лимфомы (лимфогранулематоз, лимфосаркома, ретикулосаркома), тимома, саркоидоз. При этих заболеваниях возникает недостаточность гуморального и клеточного иммунитета в результате дефекта популяции В- и Т-лимфоцитов, а возможно, и их предшественников.
Наиболее значительные виды лечения, ведущие к вторичной недостаточности иммунной системы, — лучевая терапия, применение глюкокортикоидов и иммунодепрессантов, антилимфоцитарной сыворотки, тимэктомия, дренирование грудного протока.
Недостаточность иммунной системы, связанная с лечением той или иной болезни называется патологией терапии.
При вторичных (как и при первичных) иммунодефицитных синдромах часто наблюдают гнойные инфекции, обострение туберкулезного процесса, сепсис.
Контрольные вопросы и задания
1.Какие изменения вилочковой железы связаны с нарушениями иммуногенеза?
2.Что такое реакции гиперчувствительности? Охарактеризуйте механизмы их развития.
3.Что такое реакции гиперчувствительности I типа? Назовите их причины и морфологические проявления.
4.Что такое реакции гиперчувствительности II типа? Назовите их причины, механизмы развития и морфологические проявления.
5.Что такое реакции гиперчувствительности III типа? Назовите их причины, механизмы развития и морфологические проявления.
6.Что такое реакции гиперчувствительности IV типа? Назовите их причины, механизмы развития и морфологические проявления.
7.Что такое аутоиммунные болезни? Назовите особенности их течения; приведите примеры этих болезней.
8.Что такое иммунодефицитные синдромы, и какова их классификация?
Глава 7
ПРОЦЕССЫ ПРИСПОСОБЛЕНИЯ (АДАПТАЦИИ)
И КОМПЕНСАЦИИ
Приспособление, или адаптация, — широкое биологическое понятие, включающее филогенез, онтогенез, эволюцию, наследственность и все формы регуляции функций организма в нормальных условиях и при патологии. Жизнь — непрерывная адаптация индивидуума к постоянно меняющимся условиям внешней среды. Адаптация биологического вида, состоящего из индивидуумов, зависит от способности приспособления индивидуумов к меняющимся условиям внешнего мира. Приспособительные реакции у здорового и у больного человека направлены на сохранение его гомеостаза и адаптацию к новым для него условиям жизни, в том числе к жизни после болезни. Здоровье и болезнь — состояния индивидуальные, и, следовательно, у конкретного человека видовые приспособительные реакции преломляются через его индивидуальные особенности, связанные с реактивностью, возрастом, полом, условиями жизни. Проблема приспособления — не только биологическая проблема, определяющая здоровье, но и медицинская, т.е. проблема патологии.
Компенсация — совокупность реакций организма, направленных на восстановление нарушенных функций, при повреждениях или болезнях. Следовательно, компенсация — частное проявление приспособления, развивающееся в условиях патологии, которое носит индивидуальный характер, поскольку определенной болезнью заболевает конкретный человек. Компенсаторные реакции — область медицины, область патологии. Человек как индивидуум обладает собственными реакциями, но одновременно как представитель биологического вида он имеет и видовые приспособительные реакции. Во время болезни и те и другие реакции направлены на восстановление гомеостаза, на выздоровление и их трудно разделить. Поэтому в клинической практике их часто обозначают как компенсаторно-приспо- собительные реакции.
ПРИСПОСОБЛЕНИЕ (АДАПТАЦИЯ)
С клинико-морфологических позиций все многообразие адаптационных изменений органов и тканей организма как в норме, так и при болезнях сводится к четырем основным процессам: атрофии, гипертрофии, регенерации и перестройке тканей.
228 |
Общая патологическая анатомия |
Атрофия
Атрофия (а — отрицательная частица, от греч. trophe — питание) — прижизненное уменьшение объема клеток, тканей, органов, сопровождаемое снижением или прекращением их функций.
Не всякое уменьшение органа является атрофией. При нарушениях в ходе онтогенеза орган может полностью отсутствовать — агенезия, сохранить вид раннего зачатка — аплазия, не достичь полного развития — гипоплазия. Уменьшение всех органов и общее недоразвитие всех систем организма — карликовый рост.
Существует атрофия физиологическая и патологическая. Физиологическая атрофия происходит на протяжении всей жизни чело-
века. Так, после рождения атрофируются и облитерируются пупочные артерии, артериальный (боталлов) проток; у пожилых людей атрофируются половые железы, у стариков — кости, межпозвоночные хрящи.
Патологическая атрофия — приспособление к изменениям, вызванным болезнями. Она имеет наибольшее значение в медицине и может быть вызвана различными причинами, наибольшее значение имеют недостаточное питание, нарушение кровообращения и деятельности эндокринных желез, центральной и периферической нервной системы, интоксикации. Патологическая атрофия — обратимый процесс. После ликвидации причин, вызывающих атрофию, если она не достигла высокой степени, возможно полное восстановление структуры и функции органа.
Патологическая атрофия может иметь общий или местный характер. Формы общей атрофии, или истощения:
–алиментарное истощение при голодании или нарушении усвоения пищи;
–раковая кахексия (от др.-греч. kakos — плохой, hexis — состояние);
–гипофизарная кахексия (болезнь Симмондса) при поражении гипофиза;
–церебральная кахексия (поражение гипоталамуса);
–истощение при других заболеваниях — хронических инфекциях, таких, как туберкулез, бруцеллез, хроническая дизентерия.
Внешний вид больного при истощении характерен: выраженная потеря массы тела, подкожная жировая клетчатка отсутствует, сохранившаяся клетчатка имеет буроватую окраску вследствие накопления пигмента липохрома. Мышцы атрофичны, кожа сухая, дряблая. Внутренние органы уменьшены. В печени и миокарде отмечают явления бурой атрофии (накопление пигмента липофусцина в клетках). В эндокринных железах — атрофия и дистрофия, выраженные в разной степени в зависимости от причины истощения. В коре головного мозга обнаруживают участки погибших нервных клеток. Развивается остеопороз.
Местная атрофия возникает от различных причин, согласно которым выделяют:
–дисфункциональную атрофию;
–атрофию, вызванную недостаточностью кровоснабжения;
Глава 7. Процессы приспособления (адаптации) и компенсации |
229 |
–атрофию, вызванную давлением;
–нейротическую атрофию;
–атрофию под действием физических и химических факторов. Дисфункциональная атрофия, или атрофия от адинамии, развивается
врезультате снижения функции органа:
–атрофии мышц при переломе костей, заболеваниях суставов, ограничивающих движения;
–зрительного нерва после удаления глаза;
–краев зубной ячейки, лишенной зуба.
Интенсивность обмена веществ тканей снижена, приток крови и получение питательных веществ недостаточны.
Атрофия, вызванная недостаточностью кровоснабжения, развивается вследствие сужения артерий, питающих орган. Недостаточный приток крови вызывает гипоксию, снижение функции паренхиматозных элементов, уменьшение размера клеток. Гипоксия стимулирует пролиферацию фибробластов — развивается склероз. Такой процесс наблюдают в миокарде, когда на фоне прогрессирующего атеросклероза венечных артерий развиваются атрофия кардиомиоцитов и диффузный кардиосклероз, при склерозе сосудов почек — атрофия и сморщивание почек.
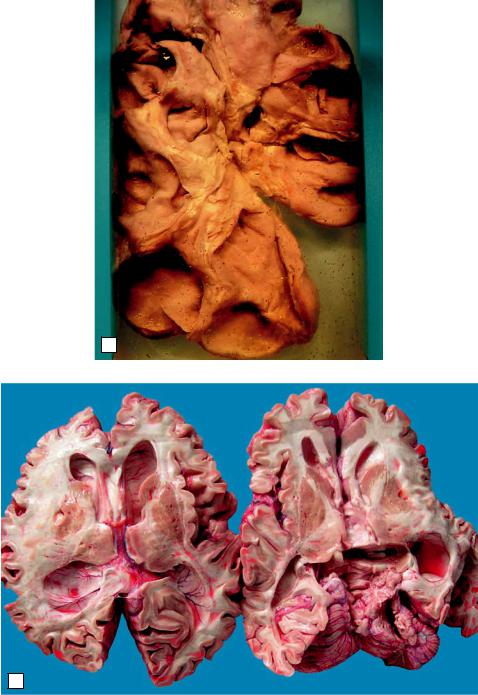
Атрофия, вызванная давлением, развивается даже в органах, состоящих из плотной ткани. При длительном давлении возникают нарушения целости ткани (узуры), например тел позвонков, грудины при давлении аневризмы. Атрофия от давления возникает в почках при затруднении оттока мочи. Моча растягивает просвет лоханки, сдавливает ткань почки, которая превращается в мешок с тонкими стенками, — гидронефроз. При затруднении оттока спинномозговой жидкости происходят расширение желудочков и атрофия ткани мозга — гидроцефалия (рис. 7-1). Основа атрофии от давления, по существу, — недостаточный приток крови к клеткам, который приводит к гипоксии.
Нейротическая атрофия обусловлена нарушениями связи органа с нервной системой при разрушении нервных проводников. Чаще она развивается
впоперечнополосатых мышцах в результате гибели моторных нейронов передних рогов спинного мозга или нервных стволов, относящихся к этим мышцам, — полиомиелит, воспаление лицевого нерва. Атрофия поперечнополосатых мышц неравномерна, разрастание межмышечной соединительной и жировой ткани усилено. Масса тканей при этом может увеличиваться — ложная гипертрофия.
Атрофия от действия физических и химических факторов — нередкое явление. Под действием лучевой энергии атрофия особенно выражена
вкостном мозге, половых органах. Йод и тиреостатические препараты подавляют функцию щитовидной железы, приводя к ее атрофии. При длительном применении АКТГ, глюкокортикоидов возникают атрофия коры надпочечников и надпочечниковая недостаточность.
Своеобразный вид адаптивной атрофии — острая инволюция тимуса.
230 |
Общая патологическая анатомия |
а
б
Рис. 7-1. Атрофия от давления: а – камни в почке и гидронефроз; б – гидроцефалия
Глава 7. Процессы приспособления (адаптации) и компенсации |
231 |
При атрофии клеток строма органа обычно сохраняет свой объем и при этом нередко подвергается склерозированию.
Внешний вид органа при местной атрофии различен. Часто орган уменьшен, поверхность его гладкая — гладкая атрофия. Реже орган, например почка, печень, принимает зернистый или бугристый вид — зернистая атрофия. При гидронефрозе, гидроцефалии, ложной гипертрофии органы увеличены, но не за счет паренхиматозных элементов, а вследствие скопления жидкости или разрастания жировой клетчатки. Иногда она разрастается вокруг атрофированного органа, например почки.
Значение атрофии для организма определено степенью уменьшения органа и снижения его функции. Если атрофия и склероз не достигли большой степени, то после устранения причины, вызвавшей атрофию органа, возможно восстановление его структуры и функции. При определенных условиях атрофированный орган впоследствии может подвергаться даже гипертрофии. Далеко зашедшая атрофия необратима.
КОМПЕНСАЦИЯ
Механизмы компенсации функции органа при болезни принципиально не отличаются от механизмов приспособления. Их основа — восстановление массы функционирующих клеток только до объема, который обеспечивает функцию органа. Многообразие компенсаторных и приспособительных изменений органов и тканей при болезнях сводится к трем основным реакциям: гипертрофии, регенерации и перестройке тканей.
Гипертрофия и гиперплазия
При длительном повышении нагрузки на орган или систему органов приспособление проявляется в виде гипертрофии (от греч. hyper — чрезмерно, trophe — питание) — т.е. в увеличении объема функционирующей ткани, обеспечивающей гиперфункцию органа. Основой гипертрофии является гиперплазия — увеличение количества клеток или внутриклеточных структур, компонентов стромы, количества сосудов. Так, за счет гиперплазии крист митохондрий развивается гипертрофия этих органелл — гигантские митохондрии; гиперплазия внутриклеточных структур обеспечивает гипертрофию клеток, а гиперплазия последних лежит в основе гипертрофии органа. Механизмы гипертрофии органов зависят от их структурных и функциональных особенностей: в одних случаях возникает преимущественно внутриклеточная гиперплазия, в других — гипертрофия развивается в основном за счет гиперплазии клеток. Возможно и сочетание этих механизмов. Гипертрофия — процесс обратимый и поддерживается гиперфункцией органа. Она исчезает при ликвидации причины, вызвавшей гиперфункцию.
Физиологическая, или рабочая, гипертрофия возникает у здоровых людей как приспособительная реакция на повышенную функцию тех или иных
232 |
Общая патологическая анатомия |
органов. Например, увеличение объема групп скелетных мышц или миокарда при занятии спортом или физическим трудом; гипертрофия матки и молочных желез при беременности и лактации. Основа такой гипертрофии — увеличение объема или количества клеток, определяющих функцию органа.
Гипертрофия при болезнях — механизм компенсации функций патологически измененных органов. В зависимости от характера и особенностей поражения выделяют несколько форм этой компенсаторной реакции:
–компенсаторную гипертрофию, которая развивается при длительной гиперфункции органа. При этом увеличивается масса функционирующей ткани, которая не поражена патологическим процессом (например, гипертрофия миокарда при артериальной гипертензии);
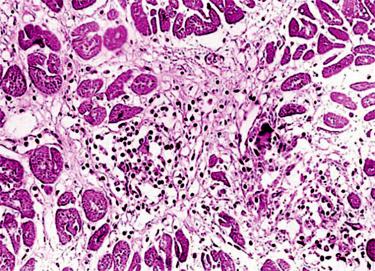
–регенерационную гипертрофию, развиваеющуюся в сохранившихся тканях поврежденного органа и компенсирующую утрату его части; возникает в сохранившейся мышечной ткани сердца при инфаркте миокарда (рис. 7-2), крупноочаговом кардиосклерозе, в сохранившейся ткани почки при нефросклерозе;
–викарную (заместительную) гипертрофию, которая развивается в сохранившемся парном органе при гибели или удалении одного из них; при викарной гипертрофии сохранившийся орган берет на себя функцию утраченного органа.
Однако увеличение объема и массы органа — не всегда компенсаторная реакция. Это может быть патологическая гипертрофия которая не только не компенсирует утраченную функцию, но нередко извращает ее. Такая гипертрофия является проявлением болезни и требует лечения.
Рис. 7-2. Регенерационная гипертрофия миокарда. По периферии рубца расположены гипертрофированные мышечные волокна
