
- •Брюшной тиф (Enteric fever)
- •Сальмонеллез
- •Пищевые отравления (Food poisoning), пищевые токсикоинфекции
- •Ботулизм
- •Дизентерия (шигеллез)
- •Амебиаз
- •Гельминтозы
- •Лабораторная диагностика гельминтозов
- •Дифиллоботриоз
- •Тениаринхоз
- •Лечение цестодозов
- •Энтеробиоз
- •Аскаридоз
- •Трихоцефаллез
- •Анкилостомидоз
- •Трихинеллез
- •Описторхоз
- •Энтеровирусная инфекция
- •Полиомиелит
- •Вирусные гепатиты
- •Основные биохимические показатели состояния печени при вирусных гепатитах
- •Лептоспироз
- •Парагрипп
- •Респираторно-синцитиальная инфекция
- •Риновирусная инфекция
- •Аденовирусная инфекция
- •Специфическая диагностика острых респираторных вирусных инфекций
- •Лечение орз
- •Менингококковая инфекция
- •Дифтерия
- •Инфекционный мононуклеоз
- •Герпетическая инфекция
- •Детские капельные инфекции у взрослых
- •Краснуха
- •Ветряная оспа
- •Паротитная инфекция
- •Специфическая диагностика вирусных капельных инфекций
- •Лечение вирусных капельных инфекций
- •Скарлатина
- •Малярия
- •Сыпной тиф (Louse-borne typhus) и болезнь брилла
- •Геморрагические лихорадки
- •Рожа (Erysipelas)
- •Эризипелоид (Erysipeloid)
- •Бруцеллез
- •Иерсиниозы (псевдотуберкулез, кишечный иерсиниоз) псевдотуберкулез
- •Кишечный иерсиниоз
- •Дифференциальная диагностика псевдотуберкулеза и кишечного иерсиниоза
- •Бешенство (Rabies)
- •Столбняк
- •Сибирская язва (Anthrax)
- •Вич-инфекция (спид)
- •Туляремия
- •Боррелиозы (эпидемический сыпной тиф, эндемический сыпной тиф, болезнь Лайма)
- •Лейшманиозы
- •Висцеральный лейшманиоз
- •Кожный лейшманиоз (Кожный лейшманиоз Старого Света)
- •Кожно-слизистый лейшманиоз (Кожный лейшманиоз Нового Света)
- •Специфическая диагностика лейшманиозов
- •Вирусные энцефалиты (клещевой, японский)
- •Клинические признаки септического состояния
- •Антибактериальная терапия
- •Неотложные состояния в клинике инфекционных болезней
Вич-инфекция (спид)
Э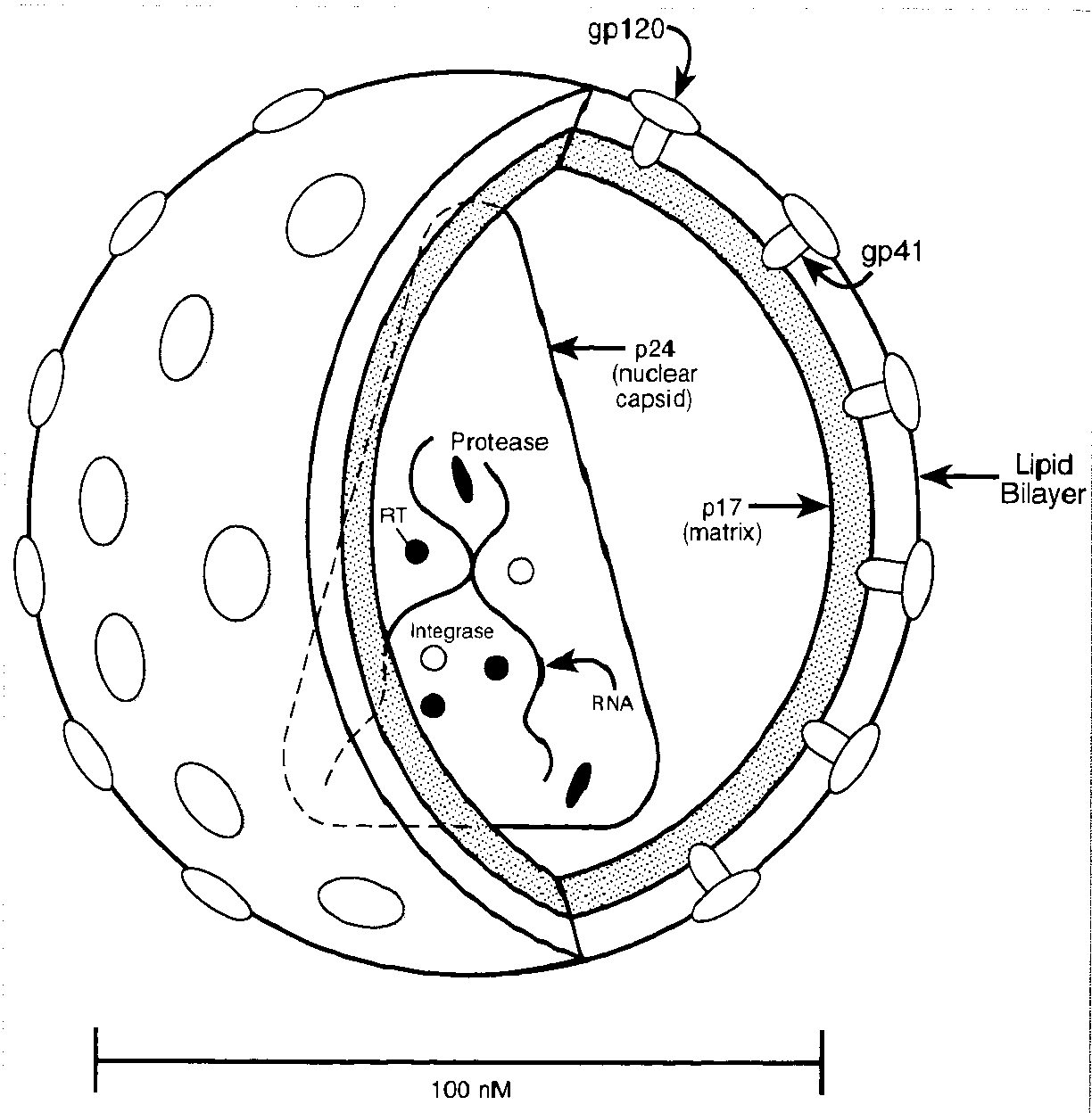 тиология
и патогенез.
Возбудитель — РНК-содержащий ретровирус
(ВИЧ — вирус иммунодефицита человека).
Ретровирусы содержат уникальный фермент
— обратную транскриптазу (ревертазу).
Обычно (например, при синтезе белка)
информация считывается с ДНК на РНК.
Благодаря обратной транскриптазе
(ревертазе) у ВИЧ происходит считывание
информации в обратном порядке (ретро)
с вирусной РНК на вирусную ДНК, которая
затем встраивается в хромосомную ДНК
клетки-хозяина.
тиология
и патогенез.
Возбудитель — РНК-содержащий ретровирус
(ВИЧ — вирус иммунодефицита человека).
Ретровирусы содержат уникальный фермент
— обратную транскриптазу (ревертазу).
Обычно (например, при синтезе белка)
информация считывается с ДНК на РНК.
Благодаря обратной транскриптазе
(ревертазе) у ВИЧ происходит считывание
информации в обратном порядке (ретро)
с вирусной РНК на вирусную ДНК, которая
затем встраивается в хромосомную ДНК
клетки-хозяина.
Известно 2-а варианта ВИЧ — ВИЧ-1 (HIV-1) и ВИЧ-2 (HIV-2). Первый является более вирулентным и более распространенным на земном шаре вирусом. Второй встречается в основном в Западной Африке. Внутри вируса, кроме упомянутой ревертазы, содержатся еще 2-а важных фермента: интеграза (встраивает ДНК вируса в ДНК клетки-хозяина) и протеаза (принимает участие в синтезе вирусных протеинов и сборке вирионов). Собственная оболочка вируса образована белком р24. Наружная оболочка вируса содержит белки gp41 (трансмембранный гликопротеин) и gp120 (внешний гликопротеин). Выявление антител к указанным белкам широко используется при проведении специфической диагностики.
Вирус попадает в организм человека парентеральным, половым или вертикальным путями. Клетками-мишенями чаще являются структуры, содержащие на своей поверхности молекулы CD4 — рецепторы для вирусной детерминанты gp120. К этим структурам прежде всего относятся Т-лимфоциты-хелперы (Т4-лимфоциты), а также моноциты/макрофаги, эпидермальные клетки Лангерганса, дендритные клетки лимфатических узлов и некоторые клетки ЦНС. Наиболее принципиальным звеном в патогенезе ВИЧ-инфекции является массовая гибель Т4-лимфоцитов, приводящая к иммуннодефицитным состояниям и, как следствие, к развитию оппортунистических инфекций, обусловленных условно-патогенной микрофлорой, и злокачественных новообразований.
При ВИЧ-инфекции поражается также и гуморальное звено иммунитета. Антитела начинают появляться (так называемая сероконверсия) в пределах 1-3 месяцев после инфицирования. Но они неполноценные и не могут освободить организм человека от вирусов, хотя способны значительно снизить его концентрацию в организме. Наиболее высокие концентрации вируса в организме человека регистрируются в первые 3 месяца после инфицирования (пока еще не произошла сероконверсия) и в терминальном периоде ВИЧ-инфекции.
Эпидемиология. ВИЧ-инфекция — антропоноз, источниками ее возбудителя для человека служат вирусоноситель и больной СПИДом. Вирус, хотя и в неодинаковой концентрации, может присутствовать почти во всех биологических жидкостях организма. Наибольшая концентрация вируса регистрируется в крови и сперме. Поэтому практически передача вируса осуществляется 3-мя основными путями:
половым
парентральным
от матери плоду/новорожденному
Половой путь. Больной ВИЧ-инфекцией менее заразен, чем сифилисом и гонореей (вероятность заражения при единичном половом контакте крайне низка). Проникать через внешне неповрежденные покровы вирус, по-видимому, малоспособен или не способен вообще. Риск заражения женщины от инфицированного мужчины значительно больше, чем мужчины от женщины (т. к. концентрация вируса в сперме по меньшей мере в 10-50 раз превосходит таковую в секрете влагалища). Риск заражения высок прежде всего у гомосексуалистов, проституток, людей, ведущих беспорядочную половую жизнь.
Парентеральный путь. Этим путем вирус передается при гемотрансфузиях, при пользовании одной иглой наркоманами при введении наркотиков внутривенно, при применении в лечебных учреждениях загрязненных свежей кровью игл, перфузионных систем, режущих инструментов и т. п. Вероятность заражения при одном проколе кожи контаминированным ВИЧ инструментом составляет 0,5-1%.
Вертикальный путь. Передача вируса от беременной женщины плоду. Вероятность рождения ВИЧ-инфицированного ребенка от ВИЧ-инфицированной матери составляет в среднем 30%.
Клиника. Чисто клинический диагноз ВИЧ-инфекции не правомочен, поскольку клинические проявления ее мало специфичны и могут наблюдаться при ряде других заболеваний. Для постановки диагноза необходимо лабораторное подтверждение. Однако заподозрить ВИЧ-инфекцию у пациента позволяют следующие признаки.
Большие признаки:
потеря массы тела > 10%
хроническая диарея в течение > 1 мес.
длительная лихорадка в течение > 1 мес.
Малые признаки:
упорный кашель > 1 мес.
генерализованный зудящий дерматит
герпес зостер в анамнезе
ротоглоточный кандидоз
хроническая прогрессирующая или диссеминированная герпетическая инфекция (herpes simplex)
генерализованная лимфоаденопатия
Диагноз ВИЧ-инфекции вероятен, если у больного обнаружены одновременно по крайней мере 2 больших признака и 1 малый. Кроме того, обнаружение у больного саркомы Капоши или криптококкового менингита — также достаточное основание для постановки диагноза.
Классификация стадий ВИЧ-инфекции по ВОЗ (1986 г.)
1. Острая ВИЧ-инфекция (как правило, совпадает с периодом сероконверсии; обычно сопровождается лихорадкой, генерализованной лимфоаденопатией, фарингитом, макуло-папуллезной сыпью, арталгиями, миалгиями, диареей, тошнотой, рвотой, увеличением печени и селезенки, реже разнообразной неврологической симптоматикой; длится от нескольких дней до нескольких (2-3 недель))
2. Бессимптомная ВИЧ-инфекция (продолжительность исчисляется годами — от 2 до 10 лет)
3. Персистирующая генерализованная лимфоаденопатия (увеличение не менее 2-х лимфатических узлов в 2-х разных группах, исключая паховые лимфатические узлы, у взрослых до размера более 1 см, сохраняющееся в течение не менее 3-х месяцев)
4. СПИД-ассоциируемый комплекс (проявляется развитием оппортунистических инфекций при содержании Т-хелперов в крови 200-400/мм3 (14%-28%))
5. Терминальная стадия ВИЧ-инфекции (проявляется развитием оппортунистических инфекций и злокачественных новообразований при содержании Т-хелперов в крови < 200/мм3 (< 14%), больные в этой стадии болезни обычно белее 2-х лет не живут)
К группе оппортунистических инфекций принято относить все те инфекции, которые манифестно проявляют себя у пациентов с иммунодефицитными состояниями. Те инфекции, которые характерно сопровождают терминальную стадию ВИЧ-инфекции, представляют собой особую, четко очерченную группу оппортунистических инфекций, которые правильно обозначать как “СПИД-индикаторные” или “СПИД-ассоциируемые” (всего их насчитывают 13 нозологических единиц). К ним относятся следующие группы:
Простейшие (токсоплазма, криптоспоридиум, пневмоциста и др.)
Грибы (кандида, криптококк, гистоплазма и др.)
Бактерии (сальмонелла, микобактерии)
Вирусы (простой герпес, цитомегаловирус)
Специфическая диагностика. Чаще всего антитела к ВИЧ обнаруживают с помощью иммуноферментных методов (ИФА). Однако при использовании этого метода нередко встречаются ложноположительные реакции. В связи с этим предложен и используется ряд методов для проверки специфичности результатов обнаружения антител. Для этого наиболее часто применяют реакцию “иммунный блотинг” в модификации Western Blot. Этот метод выявляет не комплексные антитела к ВИЧ, а антитела к отдельным его структурным белкам (p24, gp120, gp41 и др.). Естественно, что обнаружение антител сразу к двум или нескольким структурным белкам вируса делает диагноз ВИЧ-инфекции практически безапелляционным. Однако использование иммунного блотинга лимитирует его высокая стоимость. Значительно реже с целью диагностики используют методы выявления вируса и его антигенов. К таким реакциям относится полимеразная цепная реакция (ПЦР) и реакция обнаружения белка р24. С помощью этих реакции возможна постановка диагноза еще до сероконверсии (в первые 3-и недели после инфицирования).
Лечение. Хорошо документированных случаев выздоровления больных ВИЧ-инфекцией до настоящего времени нет. Достаточно эффективная антиретровирусная терапия все еще не разработана. Однако целесообразность применения этиотропной терапии у ВИЧ-инфицированных и больных СПИДом беззаговорочна, т. к. она снижает концентрацию вируса в крови, продлевает срок жизни больных и в 3 раза снижает риск рождения ВИЧ-инфицированных детей от ВИЧ-инфицированных матерей.
В настоящее время широко используются следующие группы антиретровирусных препаратов:
ингибиторы обратной транскриптазы (ревертазы) — азидотимидин, зидовудин, диданозин, зальцитабин, ставудин, ламивудин
ингибиторы протеазы — саквинавир, ритонавир, индинавир (криксиван)
Большинство исследователей отмечают, что эра монотерапии ВИЧ-инфекции в связи с развитием резистентности вирусов вследствие их мутации закончилась. Рекомендовано проводить комплексную терапию различными комбинациями препаратов. Наиболее эффективной считается комбинация азитотимидина, ламивудина и индинавира.
Значительная роль в терапии ВИЧ-инфицированных принадлежит лечению оппортунистических инфекций, которое проводится с учетом возбудителя антибактериальными, антигрибковыми, антипротозойными и антивирусными препаратами.
ЧУМА
Этиология. Возбудитель — Yersinia pestis. Представляет собой неподвижную овоидную короткую палочку, характерно биполярное окрашивание. Она обладает выраженным полиморфизмом, спор и жгутиков не имеет, грамотрицательна, растет на простых питательных средах. Факторы патогенности — экзо- и эндотоксин. Иерсинии продуцируют ферменты агрессии — гиалуронидазу, коагулазу, гемолизин, фибринолизин и др. Достаточно устойчивы во внешней среде, особенно при низких температурах.
Эпидемиология. Основным резервуаром инфекции являются грызуны (суслики, сурки, песчанки, хомяки, полевки, крысы), больной человек также является источником инфекции. Заражение чумой происходит несколькими путями: трансмиссивным — через укусы инфицированных блох, контактным — при снятии шкурок инфицированных промысловых грызунов и разделке мяса зараженных животных; алиментарным — при употреблении в пищу продуктов, обсемененных бактериями; аэрогенным — от больных легочной формой чумы. Восприимчивость людей к чуме высокая. Индекс контагиозности приближается к единице. Иммунитет после перенесенного заболевания стойкий.
Патогенез. В организм человека возбудитель чумы проникает через кожу, дыхательные пути, желудочно-кишечный тракт. Входные ворота в большой степени определяют развитие той или иной клинической формы чумы. При проникновении через кожу первичный аффект в месте внедрения, как правило, отсутствует. С током лимфы чумные бактерии заносятся в ближайшие регионарные лимфатические узлы, где происходит их размножение. Возбудители фагоцитируются нейтрофилами и мононуклеарными клетками. Но фагоцитоз оказывается незавершенным, что затрудняет запуск иммунного процесса. В лимфатических узлах развивается серозно-геморрагическое воспаление с образованием бубона. Утрата лимфатическим узлом барьерной функции приводит к генерализации процесса. Бактерии гематогенно разносятся в другие лимфатические узлы, внутренние органы, вызывая воспаление (вторичные бубоны и гематогенные очаги). Размножение иерсиний во вторичных очагах инфекции приводит к развитию септических форм чумы, для которых характерно развитие инфекционно-токсического шока и образование септикопиемических очагов в различных внутренних органах. Гематогенный занос чумных бактерий в легочную ткань приводит к развитию вторичной чумной пневмонии с образованием обильного серозно-геморрагического экссудата, содержащего огромное количество иерсиний. Септическая форма чумы сопровождается экхимозами и кровоизлияниями в кожу, слизистые и серозные оболочки, стенки крупных и средних сосудов. Типичны тяжелые дистрофические изменения сердца, печени, селезенки, почек и других внутренних органов.
Клиническая классификация:
А. Преимущественно локальные формы: кожная, бубонная, кожно-бубонная.
Б. Внутреннедиссеминированные, или генерализованные формы: первично-септическая, вторично-септическая.
В. Внешнедиссеминированные: первично-легочная, вторично-легочная, кишечная. Кишечная форма как самостоятельная большинством авторов не признается.
Клиника. Инкубационный период чумы составляет 2—6 дней. Заболевание, как правило, начинается остро. Для всех форм чумы характерна следующая симптоматика:
быстрое повышение температуры тела до 39—40°С, сопровождающееся сильным ознобом и чувством жара
миальгии, мучительная головная боль, головокружение
гиперемия лица и конъюнктив
губы сухие, язык отечный, сухой, дрожащий, обложен густым белым налетом (как бы натерт мелом), увеличен
речь смазанная, неразборчивая, токсическое поражение нервной системы: от оглушенности и заторможенности до возбуждения, бреда, галлюцинаций, нарушается координация движений
прогрессивно нарастающая сердечно-сосудистая недостаточность: тахикардия (до 120— 160 уд. в 1 мин), цианоз, аритмия пульса, значительное снижение артериального давления
увеличение печени и селезенки
у тяжелобольных развивается геморрагический синдром, сопровождающийся кожными проявлениями, кровавой или цвета кофейной гущи рвотой, жидким стулом со слизью и кровью
нейтрофильный лейкоцитоз со сдвигом лейкоцитарной формулы влево, СОЭ повышена
Помимо общих проявлений чумы, развиваются поражения, присущие различным формам болезни.
Кожная форма. В месте внедрения возбудителя возникают изменения в виде некротических язв, фурункула, карбункула. Для некротических язв характерна быстрая, последовательная смена стадий: пятно, везикула, пустула, язва. Чумные кожные язвы характеризуются длительным течением и медленным заживлением с образованием рубца.
Бубонная форма. Бубон — резко болезненное увеличение лимфатических узлов, спаянных в единый конгломерат между собой и с подкожной клетчаткой. Бубон, как правило, бывает один. Наиболее частые локализации чумных бубонов — паховая, подмышечная, шейная области. Ранний признак формирующегося бубона — резкая болезненность, вынуждающая больного принимать вынужденное положение. Кожа над бубоном напряжена, приобретает красный цвет. Лимфангитов не наблюдается. По окончании стадии формирования бубона наступает фаза его разрешения, протекающая в одной из трех форм: рассасывание, вскрытие и склерозирование.
Первично- и вторичносептические формы чумы проявляются сходной симптоматикой, но отличаются динамикой развития и течения процесса. Первые возникают после инфицирования, вторые — как осложнение других форм заболевания. Для этих форм характерны крайне выраженные проявления, описанные в общей части. В этих случаях заболевание развивается бурно и часто приводит к смертельному исходу.
Первичнолегочные (развиваются после инфицирования) и вторичнолегочные (развиваются как осложнение других форм заболевания) формы клинически проявляются однотипно. Наиболее специфическими симптомами являются: сильная боль в грудной клетке; пенистая, жидкая, “ржавая” мокрота на фоне скудных данных физикального обследования легких.
Специфическая диагностика. Используют бактериоскопический, бактериологический, биологический и серологический методы, проводимые в специальных лабораториях, работающих в соответствии с инструкциями о режиме работы противочумных учреждений. Материалом для исследования служат пунктаты из бубона, содержимое везикул, пустул, карбункулов, отделяемое из язв, мокрота, кровь, моча, рвотные массы, секционный патологоанатомический материал. Специфическое свечение бактерий при использовании метода флюоресцирующих антител, наличие в препаратах, окрашенных по Граму, овоидных биполярных палочек с учетом клинических, патологоанатомических, эпидемиологических и эпизоотологических данных позволяет поставить предварительный диагноз чумы и проводить соответствующие мероприятия до выделения возбудителя.
В практике лабораторной диагностики чумы широко применяются серологические методы: ИФА, РНГА, РНАт, РНАг, РТНГА. Важное значение имеет постановка биологической пробы на морских свинках и белых мышах, позволяющая увеличить вероятность выделения культур и облегчить их идентификацию.
Лечение. Больные чумой подлежат строгой изоляции и обязательной госпитализации. Основная роль в этиотропном лечении принадлежит антибиотикам — стрептомицину, препаратам тетрациклинового ряда, левомицетину, назначаемым в больших дозах.
Стрептомицин эффективен при всех формах чумы. При бубонной форме его вводят в дозах 0,5— 1,0 г 3 раза в сутки, больным с септической и легочной формами чумы — по 1 г 4 раза в сутки в течение первых 4— 5 дней, а с 5 — 6-го дня переходят на трехразовое введение по 0,75 г. Окситетрациклин вводят внутримышечно в дозе 0,2 г 6 раз в сутки. Используют также доксициклин, метациклин, морфоциклин. Левомицетин назначают в суточной дозе 6—8 г со снижением дозы после нормализации температуры. При лечении больных легочными и септическими формами чумы назначают комбинацию 2-3 препаратов. Курс лечения антибиотиками больных всеми формами чумы составляет не менее 7— 10 сут.
Индивидуальная профилактика. Подвергшиеся риску заражения подлежат изоляции и наблюдению в течение 6 дней, а также экстренной профилактике (превентивному лечению). При экстренной профилактике препаратом выбора является стрептомицин (по 0,5 2 раза в день).
В очагах чумы по эпидемическим показаниям проводится профилактическая вакцинация. С этой целью применяется живая вакцина. После вакцинации создается относительный иммунитет продолжительностью до 6 мес.
