
Posob.GFS
.pdf
3.Эпимеры, определение, примеры.
4.Открытые и циклические формы (пиранозы и фуранозы). Таутомер-
ные превращения, мутаротация, - и - аномеры.
4. Химические свойства моносахаридов. Образование простых и сложных эфиров. Реакции полуацетальной гидроксильной группы: восстановитель-
ные свойства, образование О-гликозидов. Отношение гликозидов, простых и сложных эфиров моносахаридов к гидролизу. Окисление моносахаридов.
Альдоновые, альдаровые и уроновые кислоты (D-Глюконовая, D-
глюкуроновая, D-галактуроновая кислоты). Восстановление моносахаридов в полиолы (D-сорбит, ксилит). Изомеризация моносахаридов в щелочной среде.
5. Аминосахара: D-глюкозамин, N-ацетил-D-глюкозамин.
6. Олигосахариды. Принцип строения. Восстанавливающие и невосстанав-
ливающие дисахариды. Таутомерия восстанавливающих дисахаридов.
7. Химические свойства мальтозы, лактозы, сахарозы.
8.Полисахариды. Принцип строения. Гомо - и гетерополисахариды.
9.Гомополисахариды: (амилоза, амилопектин, гликоген, декстран, целлюло-
за). Пектины. Монокарбоксилцеллюлоза, полиакрилцеллюлоза – основа ге-
мостатических перевязочных материалов.
10. Гетерополисахариды. Представление о структуре гиалуроновой кисло-
ты, хондроитинсульфатов, гепарина.
41
Углеводы.
Углеводы – это природные органические соединения, состав которых отвеча-
ет формуле CnH2mOm (Cn(H2O)m), где n,m≥ 4.
Это группа природных веществ, относящихся к полигидроксикарбонильным соединениям, а также вещества, близкие им по строению.
Наиболее известны глюкоза, крахмал, целлюлоза, гликоген, гепарин и дру-
гие, играющие важное значение в жизненных процессах человека и живот-
ных.
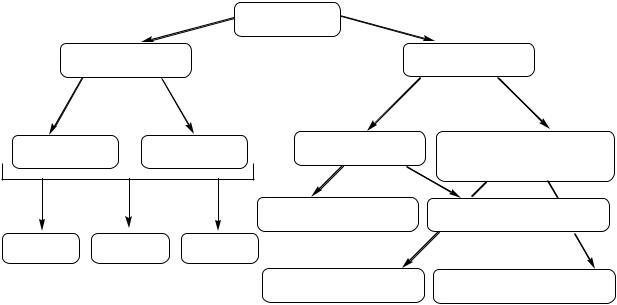
Классификация.
По способности к гидролизу углеводы делят на моносахариды – не гидроли-
зующиеся, и полисахаридывещества, при гидролизе которых образуются молекулы моносахаридов.
Углеводы
Моносахариды |
Полисахариды |
Альдозы |
Кетозы |
Олигосахариды |
Высокомолекулярные |
|
полисахариды |
||
|
|
|
|
|
|
Восстанавливающие |
Невосстанавливающие |
Тетрозы |
Пентозы Гексозы |
|
|
|
|
Гомополисахариды |
Гетерополисахариды |
42
Моносахариды.
Простейшие углеводы, не подвергающиеся гидролизу. Наибольшее значение в природе имеют пентозы и гексозы,состав которых отвечает формуле
CnH2mOm (Cn(H2O)m), где n,m= 5,6.
Номенклатура.
В номенклатуре углеводородов используются главным образом тривиальные названия: рибоза, фруктоза, глюкоза и так далее. Названия могут содержать префикс «дезокси» - который обозначает отсутствие гидроксильной группы
(«без гидроксила»).
|
CHO |
|
CHO |
|||||
H |
|
|
OH |
H |
|
|
|
H |
|
|
|
|
|||||
H |
|
|
OH |
H |
|
|
|
OH |
|
|
|
|
|
||||
H |
|
|
OH |
H |
|
|
|
OH |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
CH2OH |
|||||
D-рибоза D-дезоксирибоза
43

Изомерия.
1. Структурная изомерия.
 Межклассовая изомерия.
Межклассовая изомерия.
Для моносахаридов характерна межклассовая изомерия. По функциональной принадлежности моносахариды являются альдегидоили кетономногоатом-
ными спиртами. По характеру карбонильной группы моносахариды делят на альдозы, либо кетозы соответственно.
Например, для гексоз общей формулы С6(Н2О)6(С6Н12О6) можно изобразить структурные изомеры:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
CH |
|
|
CH |
|
CH |
|
|
CH |
|
C |
H |
H3C |
|
|
CH |
|
|
CH |
|
CH |
|
C |
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
OH |
|
|
|
OH |
|
OH |
|
OH |
|
OH |
|
|
OH |
|
OH |
|
|
O |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
альдогексоза (альдоза) |
|
|
кетогексоза (кетоза) |
|
||||||||||||||||||||||||
2. Пространственная изомерия.
 Оптическая изомерия
Оптическая изомерия
Наличие нескольких асимметрических атомов углерода в молекулах моноса-
харидов обусловливает существование большого числа оптических изомеров.
Например, для альдогексоз общей формулы С6Н12О6, наличие четырех асси-
метрических атомов обеспечивает существование 16 оптических изомеров.
* |
* |
* |
* |
|
|
O |
||||||||
|
|
N= 2n = 24 = 16 |
||||||||||||
H3C |
|
|
CH |
|
|
CH |
|
CH |
|
|
CH |
|
C |
|
|
|
|
|
|
||||||||||
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
H |
|
|
OH |
|
OH |
|
|
OH |
|||||||
|
|
|
|
|
|
|||||||||
Это энантиомеры (зеркальные изомеры, 8 пар), диастереомеры(оптические изомеры, не являющиеся зеркальными копиями друг друга) и эпимеры.Все изомеры, кроме зеркальных, отличаются друг от друга свойствами и имеют свое название.
44

Для обозначения энантиомеров используется D,L- номенклатура. При-
надлежность моносахаридов к D- или L-ряду определяется по конфигурации последнего (наиболее удаленного от карбонильной группы) хирального ато-
ма углерода по аналогии со стандартом – глицериновым альдегидом:
|
|
1CHO |
|
|
|
|
|
CHO |
|
|
|
|
|
|
|
|
|
|
|
|||||
H |
2 |
|
|
OH |
|
HO |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
HO |
|
|
|
H |
|
H |
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
H |
|
|
OH |
|
HO |
|
|
|
|
|
H |
|
CHO |
|
|
CHO |
||||||||
5 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
H |
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
OH |
|
HO |
|
|
|
|
|
H |
|
|
|
OH |
|
HO |
|
|
|
H |
||||
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
CH2OH |
|
CH2OH |
|
|
CH2OH |
||||||||||||
D-глюкоза |
|
L-глюкоза |
D-глицериновый |
L-глицериновый |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
альдегид |
альдегид |
|||||||||
Природные сахара в основном относятся к D-ряду и поступают в орга-
низм извне, с пищей.
Эпимеры – это диастереомеры, отличающиеся друг от друга конфигурацией только одного асимметрического атома углерода. D-Манноза и D-галактоза из ряда альдогексоз и кетогексоза -D-фруктоза, являются эпимерамиD-
глюкозы:
|
|
1CHO |
|
|
|
|
2 |
CHO |
|
|
|
CHO |
|
|
|
CH2OH |
||||||||||||
H |
2 |
|
OH |
HO |
|
|
|
H |
H |
|
|
|
|
|
OH |
|
|
2 C |
|
|
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||
3 |
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
HO |
|
|
H |
HO |
|
|
|
|
|
|
H |
HO |
|
|
|
|
|
|
H |
HO |
|
|
|
|
|
|
H |
|
|
4 |
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
||||||||
H |
|
OH |
H |
|
|
|
|
|
OH |
HO |
|
|
|
|
H |
H |
|
|
|
|
|
OH |
||||||
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
H |
|
OH |
H |
|
|
|
|
|
OH |
H |
|
|
|
|
|
OH |
H |
|
|
|
|
|
OH |
|||||
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CH2OH |
|
|
|
CH2OH |
|
|
|
CH2OH |
|
|
CH2OH |
|||||||||||||||
D-глюкоза |
D-манноза |
D-галактоза |
D-фруктоза |
|||||||||||||||||||||||||
45
 Цикло-оксо-таутомерия
Цикло-оксо-таутомерия
Для всех моносахаридов характерно явление цикло-оксо-таутомерии, или ок-
со-окси-таутомерии, то есть наряду с открытой (не циклической формой) они существуют и в циклических формах. В пространстве углерод-углеродная цепь изогнута, поэтому карбонильная группа располагается близко к гидро-
ксильной группе 4 или 5 атома углерода. Между этими группами одной мо-
лекулы происходит взаимодействие и образуется внутренний полуацеталь.
гликозидный гидроксил
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
6 |
CH2OH |
|
|
|
|
|
H |
1 |
|
OH |
|
|
|
|
|
1C |
H |
|
|
|
HO |
1 |
|
H |
|
|
|
|
6 |
CH2OH |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
H |
|
|
OH |
|
|
|
|
H |
|
|
OH |
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
O OH |
|||||||||||||||
H |
|
5 |
|
H |
2 |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
H |
|
5 |
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
OH |
H |
|
|
|
HO |
3 |
|
|
|
|
|
|
HO |
3 |
|
H |
|
|
|
HO |
3 |
|
|
|
|
|
|
OH |
H |
|
|
|||||||||||
|
1 |
|
|
|
H O |
|
|
|
|
|
|
|
|
H O 4 |
|
1 |
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
2 |
OH |
H |
|
|
OH |
|
|
|
|
H |
|
|
OH |
|
|
|
H |
|
|
OH |
|
|
OH |
|
|
|
|
2 |
H |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
||||||||||||||||||||||||
|
|
|
3 |
|
|
|
|
|
4 |
|
|
|
|
|
4 |
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
H |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
OH |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
H |
|
|
O |
|
H |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
D-глюкопираноза |
5 |
|
|
|
5 |
|
|
5 |
|
|
|
|
D-глюкопираноза |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH |
OH |
|
|
|
|
|
CH2OH |
|
|
|
|
|
CH |
OH |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
6 |
2 |
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
6 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
D-глюкоза
|
6CH2OH |
|
|
H |
1 |
OH |
HO |
1 |
|
H |
|
6CH2OH |
|
|
|||
HO |
5 |
H |
|
H |
H |
2 |
OH |
H |
2 |
|
OH |
HO |
5 |
H |
O |
OH |
|
|
O |
|
|
|
|
|
|
|
|
||||||||
|
4 |
|
|
1 |
|
|
|
HO |
|
|
H O |
|
4 |
OH |
H 1 |
||
|
OH |
H |
HO |
|
H O |
|
|
|
|
||||||||
|
|
3 |
3 |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|||||||||||
|
H |
|
3 |
2 |
OH |
H |
4 |
|
H |
4 |
|
|
|
H |
3 |
|
2 H |
|
|
H |
|
|
|
|
|
H |
|
OH |
|||||||
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
H |
5 |
OH |
H |
5 |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
D-глюкофураноза |
|
CH OH |
|
CH |
OH |
|
|
D-глюкофураноза |
|||||||||
|
6 |
2 |
|
6 |
2 |
|
|
|
|||||||||
Для альдогексоз более характерна пиранозная форма (шестичленный кисло-
родсодержащий гетероцикл), для альдопентоз и кетогексоз – фуранозная (пя-
тичленный кислородсодержащий цикл). Все это отражается в названии цик-
лических форм, например, -D-глюкопираноза.
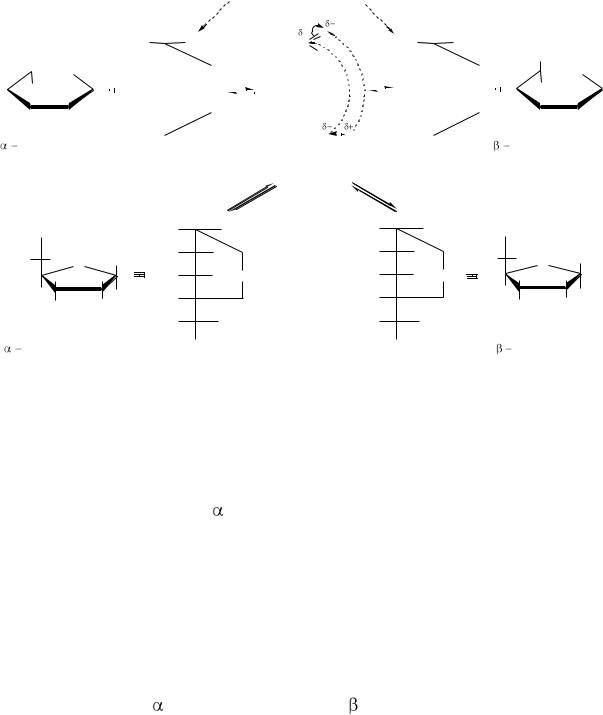
Вновь образовавшийся гидроксил носит название полуацетального, или
гликозидного и может по-разному располагаться в пространстве относи-
тельно цикла, образуя еще один асимметрический атом углерода в цикличе-
ской форме. Если полуацетальный гидроксил располагается по одну сторону с гидроксилом, определяющим принадлежность к D- или L-ряду, то такой изомер называется -изомером, а другой – -изомером. Изображение цикли-
46

ческих форм моносахаридов при помощи формул Фишера имеет недостатки
– неестественно длинная связь кислорода в цикле, плохо отражает геометрию цикла. Поэтому для циклических форм чаще используют формулы Хеуорса,
где цикл изображается плоским пятиили шестичленным кольцом.
Алгоритм построения формул Хеуорса:
1.Написать структуру открытой формы монозы и пронумеровать угле-
родные атомы по принципам международной номенклатуры.
2.Написать формулу Фишера для циклической формы.
3.Изобразить цикл нужного размера и пронумеровать его по часовой стрелке, атом кислорода, как правило, изображается в правом верхнем углу.
4.Заместители, находящиеся справа от углеродной цепи в формуле Фи-
шера, располагаются снизу от плоскости цикла, располагающиеся сле-
васверху от плоскости.
5.Исключение заместители атома углерода, гидроксил которого образует цикл (С4 или С5), заместители справасверху, слеваснизу.
Стереоизомеры, отличающиеся друг от друга расположением толькополу-
ацетального гидроксила в пространстве, называются аномерами.
Процесс образования циклических форм называется аномеризацией.
Циклическая и открытая формы легко переходят друг в друга и находятся в динамическом равновесии – цикло-оксотаутомерия.
При комнатной температуре в таутомерной смеси преобладает циклические формы, при нагревании – открытая. Именно циклическая форма участвует в образовании ди- и полисахаридов.
В кристаллическом состоянии циклические формы закреплены и - и -
изомеры стабильны и могут быть отделены друг от друга. При растворении часть молекул переходит в открытую форму, а из нее образуются все виды циклических форм. Так как каждая форма (диастереомер) имеет свой угол
47
вращения луча поляризованного света, то до установления динамического равновесия угол вращения будет постоянно меняться.
Изменение во времени угла вращения плоскости поляризации света свеже-
приготовленного раствора углеводов называется мутаротацией.
Химические свойства.
Циклическая и открытая (альдегидная) формы находятся в равновесии.
Поэтому возможны реакции, характерные для альдегидной группы (в откры-
той форме) икак для многоатомного спирта (в открытой или циклической форме).
I. Реакции по карбонильной группе.
Для моносахаридов характерны практически все реакции, характерные для альдегидов и кетонов. Однако, так как концентрация открытой формы в тау-
томерной смеси мала (для водного раствора глюкозы 0.024%), для моносаха-
ридов не протекает, например, реакция с гидросульфидом натрия (NaHSO3).
 Для моносахаридов протекают реакции нуклеофильного присоедине-
Для моносахаридов протекают реакции нуклеофильного присоедине-
ния (АN) синильной кислоты, водорода (восстановление).
Реакция с синильной кислотой проходит очень легко, образуется окси-
нитрил.
|
O |
|
|
OH |
|
C |
|
C |
C N |
|
H |
|
|
H |
H |
OH |
+ H C N |
H |
OH |
HO |
H |
|
HO |
H |
H |
OH |
|
H |
OH |
H |
OH |
|
H |
OH |
|
CH2OH |
|
CH2OH |
|
|
D-глюкоза |
|
оксинитрил D-глюкозы |
|
48

При восстановлении образуются многоатомные спиртызаменители са-
хара.
+ |
O |
|
|
|
|
CH2OH |
|||||
|
|
C |
H |
|
|
|
|
||||
|
|
|
|
|
|
H |
|
|
OH |
||
H |
|
|
|
OH |
t 0, Ni |
|
|
||||
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||
HO |
|
|
|
H + H2 |
|
|
HO |
|
|
H |
|
|
|
|
|
|
|
|
|||||
H |
|
|
|
OH |
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|||||
H |
|
|
|
OH |
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
CH2OH |
||
|
|
CH OH |
|
|
|
||||||
|
|
|
|
2 |
|
|
|
|
|
|
|
D-глюкоза |
|
|
|
сорбит |
|||||||
Глюкоза образует сорбит, фруктоза смесь сорбита и маннита, рибозари-
бит.
 Моносахариды вступают в реакции нуклеофильного замещенияс
Моносахариды вступают в реакции нуклеофильного замещенияс
пентахлоридом фосфора и азотистыми нуклеофилами (гидразином, гидро-
ксиламином, фенилгидразином).
С гидразиноном реакция имеет свои особенности. С недостатком гидразина образуется типичный продукт – гидразон.
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
H |
|
C N |
|
NH |
|
C6H5 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
H |
|
|
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
HO |
|
|
|
H + H N |
|
NH |
|
C H |
5 |
|
HO |
|
|
|
|
|
|
H + H2O |
||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
2 |
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
H |
|
|
OH |
|
|
|
|
|
|
H |
|
|
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
H |
|
|
OH |
|
|
|
|
|
|
H |
|
|
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH OH |
|
|
|
|
|
|
|
|
|
|
CH2OH |
|||||||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D-глюкоза |
|
|
|
|
|
|
гидразон D-глюкозы |
|||||||||||||
При добавлении избытка реагента из глюкозы, маннозы и фруктозы образу-
ется озазон.
49

|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
H |
|
C |
|
N |
|
|
NH |
|
C6H5 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
C |
|
N |
|
|
NH |
|
C6H5 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|||||||||||||||||
HO |
|
|
|
H + 3 H N |
|
NH |
|
C H |
5 |
|
HO |
|
|
|
|
|
|
H + NH2 C6H5 + NH3 + 2 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
2 |
6 |
|
|
|
|
|
|
|
|
|
|
H2O |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H |
|
|
OH |
|
|
|
|
|
|
H |
|
|
|
|
|
OH |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
H |
|
|
OH |
|
|
|
|
|
|
H |
|
|
|
|
|
OH |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH OH |
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
||||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D-глюкоза |
|
|
|
|
|
|
озазон D-глюкозы |
|
|
||||||||||||
II. Реакции по гидроксильным группам.
Протекают как в открытой, так и в циклических формах.
 Кислотные свойства
Кислотные свойства
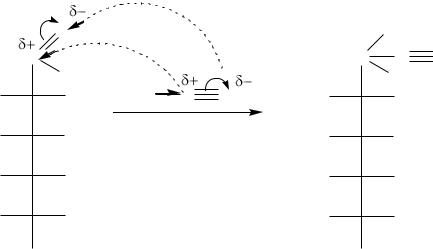
Моносахариды как и многоатомные спирты взаимодействуют с активными металлами и щелочами, образуя сахараты, дают качественную реакцию на многоатомные спирты с гидроксидом меди (II):
|
|
CHO |
|
|
|
|
|
|
|
|
|
|
|
CHO |
|
|
|
|
|
|
|
|
||||
H |
|
|
OH |
|
|
D-глюкоза |
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
||||||||
HO |
|
|
|
H |
|
|
|
|
|
|
HO |
|
|
|
H |
|
|
|
CH OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
H |
|
|
O H HO |
|
|
HO |
|
|
|
H |
t0 |
H |
|
|
O |
|
H |
O |
|
|
2 |
|
H |
|||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
+ |
Cu |
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
Cu |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H - 2 H2O |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
H |
|
|
OH |
|
OH H |
|
O |
|
|
|
H |
|
|
O |
H |
|
O |
|
|
|
|
H |
||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
H |
|
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
D-глюкоза |
|
|
HO |
|
|
|
H |
|
|
|
|
|
|
|
|
HO |
|
|
|
|
H |
|||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
CHO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CHO |
||||||||
 Вступают в типичные реакции электрофильного замещения (SE)
Вступают в типичные реакции электрофильного замещения (SE)
В реакции алкилированияс галогеналканами образуются простые эфиры:
|
|
CH2OH |
|
|
|
|
|
CH2OCH3 |
|
|
|||||
H |
|
O |
H |
|
H |
|
O |
H |
|||||||
|
|
|
|||||||||||||
|
OH |
H |
|
+ 5 CH3I |
|
|
OCH3 H |
|
+ 5 HI |
||||||
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
OH |
|
|
|
OH |
|
|
|
|
|
|
|
OCH3 |
|||
|
|
|
|
OCH3 |
|
|
|||||||||
|
H |
OH |
|
|
|
|
H |
OCH3 |
|||||||
-D-глюкоза
Сминеральными и органическими кислотами протекает реакция этерифика-
ции и образуются сложные эфиры. Наиболее важны эфиры фосфорной ки-
слоты:
50
