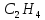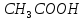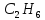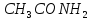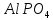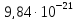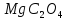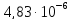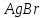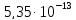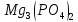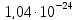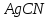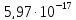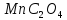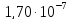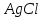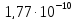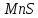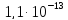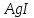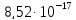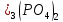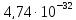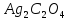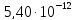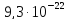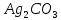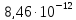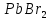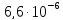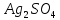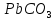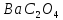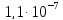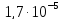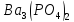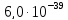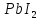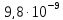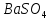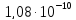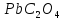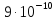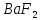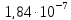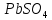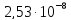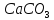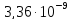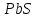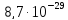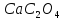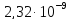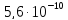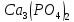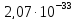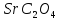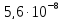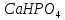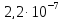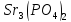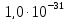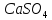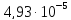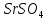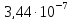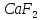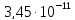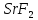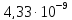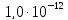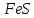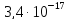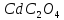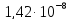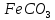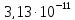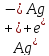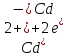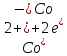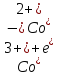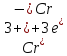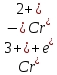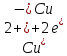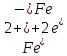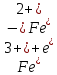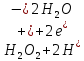- •Техніка безпеки в хімічній лабораторії
- •Заняття 1. Біогенні елементи; біологічна роль, застосування в медицині.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Характерні реакції іонів деяких макро – та мікроелементів
- •Заняття 2. Комплексоутворення в біологічних системах.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •КомплексНі сполуки
- •Заняття 3. Величини, що характеризують кількісний склад розчинів. Приготування розчинів.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Приготування розчину кобальт (іі) нітрату розбавленням більш концентрованого розчину
- •Заняття 4. Кислотно-основна рівновага в організмі. Водневий показник біологічних рідин.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Гідроліз солей
- •Заняття 5. Основи титриметричного аналізу.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Визначення молярної концентрації еквівалента натрій гідроксиду за титрованим розчином сульфатної кислоти
- •Заняття 6. Буферні системи, їх біологічна роль.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Приготування буферних розчинів і вивчення їх властивостей
- •Завдання:
- •Визначення буферної ємності ацетатного буферного розчину
- •Завдання:
- •Заняття 7. Колігативні властивості розчинів.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Визначення теплот нейтралізації
- •Заняття 9. Кінетика біохімічних реакцій.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Дослідження залежності швидкості розкладу тіосульфатної кислоти від її молярної концентрції
- •Заняття 10. Хімічна рівновага. Добуток розчинності.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Визначення нормального окисно-відновного потенціалу
- •Заняття 12. Сорбція біологічно-активних речовин. Іонний обмін. Хроматаграфія.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Адсорбція ацетатної кислоти на активованому вугіллі
- •Кількісне визначення іонів кальцію у розчині методом іонообмінної адсорбції
- •Розділення суміші барвників за допомогою методу тонкошарової хроматографії
- •Розділення суміші катіонів заліза(ііі) і купруму(іі) за допомогою адсорбційної колонкової хроматографії
- •Заняття 13. Одержання ,очистка та властивості колоїдних розчинів.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Одержання, очищення та властивості колоїдних розчинів
- •Заняття 14. Коагуляція колоїдних розчинів. Властивості розчинів біополімерів.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Визначення порогу коагуляції
- •Визначення ізоелектричної точки (іет) альбуміну сироватки крові
- •Довідкова інформація
- •Приклад письмової роботи (Модуль 1)
- •Письмова робота
- •Приклад письмової роботи (Модуль 2)
- •Письмов робота
Довідкова інформація
МАТЕМАТИЧНІ ОПЕРАЦІЇ
Логарифм числа b з основою a – це показник ступеня, в яку необхідно возвести число a, щоб отримати число b.
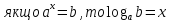
|
властивості ступенів: |
властивості логарифмів: | ||||
|
1. |
|
|
1. |
|
|
|
2. |
|
|
2. |
|
|
|
3. |
|
|
3. |
|
|
|
4. |
|
|
4. |
|
|
|
5. |
|
|
5. |
|
|
|
6. |
|
|
|
|
|
|
7. |
|
|
|
|
|
|
8. |
|
|
|
|
|
таблиця десяткових логарифмів
|
|
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
1 |
000 |
041 |
079 |
114 |
146 |
176 |
204 |
230 |
255 |
279 |
|
2 |
301 |
322 |
342 |
362 |
380 |
398 |
415 |
431 |
447 |
462 |
|
3 |
477 |
491 |
505 |
519 |
532 |
544 |
556 |
568 |
580 |
591 |
|
4 |
602 |
613 |
623 |
634 |
644 |
653 |
663 |
672 |
681 |
690 |
|
5 |
699 |
708 |
716 |
724 |
732 |
740 |
748 |
756 |
763 |
771 |
|
6 |
778 |
785 |
792 |
799 |
806 |
813 |
820 |
826 |
833 |
839 |
|
7 |
845 |
851 |
857 |
863 |
869 |
875 |
881 |
887 |
892 |
898 |
|
8 |
903 |
909 |
914 |
919 |
924 |
929 |
935 |
940 |
945 |
949 |
|
9 |
954 |
959 |
964 |
969 |
973 |
978 |
982 |
987 |
991 |
996 |
приклад розрахунку pH за значенням [H+]
[H+] = 5,3∙10-1 моль/л. pH = -lg [H+] = -lg 5,3∙10-1 = -(0,724 - 1) = -(-0,276) ≈ 0,28
приклад розрахунку [H+] за значенням pH
pH = 0,42. [H+] = antilg (-pH) = antilg (-0,42) = antilg (0,580 - 1) = 3,8∙10-1 моль/л
ТЕРМОДИНАМІЧНІ ВЛАСТИВОСТІ ДЕЯКИХ РЕЧОВИН
|
речовина |
стан |
|
|
|
|
|
р |
0 |
152,2 |
0 |
|
|
г |
-383,5 |
213,8 |
-394,4 |
|
|
г |
-110,5 |
197,7 |
-137,2 |
|
|
г |
0 |
223,1 |
0 |
|
|
г |
0 |
130,7 |
0 |
|
|
г |
-36,3 |
198,7 |
-53,4 |
|
|
г |
-92,3 |
186,9 |
-95,3 |
|
|
г |
-241,8 |
188,8 |
-228,6 |
|
|
р |
-285,8 |
70,0 |
-237,1 |
|
|
г |
-187,8 |
109,6 |
-120,4 |
|
|
г |
0 |
191,6 |
0 |
|
|
г |
-45,9 |
192,8 |
-16,4 |
|
|
тв |
-314,4 |
94,6 |
-202,9 |
|
|
тв |
-365,6 |
151,1 |
-183,9 |
|
|
г |
91,3 |
210,8 |
87,6 |
|
|
г |
81,6 |
220,0 |
103,7 |
|
|
г |
33,2 |
240,1 |
51,3 |
|
|
г |
0 |
205,2 |
0 |
|
|
г |
142,7 |
238,9 |
163,2 |
|
|
г |
-451,8 |
213,9 |
|
|
|
г |
70,3 |
240,0 |
|
|
|
р |
-279,5 |
172,4 |
|
|
|
р |
-266,0 |
262,9 |
|
|
фталева кислота |
тв |
-782,0 |
207,9 |
|
|
фталевий ангідрид |
тв |
-460,1 |
180 |
|
|
L – молочна кислота |
aq |
-686 |
222 |
-539 |
|
D - глюкоза |
тв |
-1274,5 |
212,1 |
-910,0 |
|
D - глюкоза |
aq |
-1263,8 |
269,5 |
-917,0 |
|
сахароза |
тв |
-2222 |
360 |
-1545 |
ТЕПЛОТИ ЗГОРЯННЯ ДЕЯКИХ РЕЧОВИН
|
речовина |
стан |
|
речовина |
стан |
|
|
|
г |
-285,8 |
|
р |
-2723,9 |
|
|
г |
-382,8 |
|
к |
-2802,5 |
|
|
г |
-890,8 |
|
к |
-5639,7 |
|
|
г |
-1411,2 |
|
р |
-874,2 |
|
|
г |
-1560,7 |
|
р |
-1184,6 |
ДОБУТКИ РОЗЧИННОСТІ ДЕЯКИХ МАЛОРОЗЧИННИХ ЕЛЕКТРОЛІТІВ ПРИ 25ºС
|
Речовина |
ДР |
Речовина |
ДР |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СТАНДАРТНІ ЕЛЕКТРОДНІ ПОТЕНЦІАЛИ У ВОДНИХ РОЗЧИНАХ ПРИ 25ºС
|
напівреакція |
|
|
|
0,800 |
|
|
-0,403 |
|
|
-0,28 |
|
|
1,92 |
|
|
-0,744 |
|
|
-0,407 |
|
|
1,232 |
|
|
0,340 |
|
|
-0,447 |
|
|
0,771 |
|
|
1,776 |
|
|
0,695 |
|
|
0,5355 |
|
|
-1,185 |
|
|
1,507 |
|
|
-0,257 |
|
|
-0,1375 |
|
|
0,151 |
|
|
-0,760 |
РЯД АКТИВНОСТІ МЕТАЛІВ / ЕЛЕКТРОХІМІЧНИЙ РЯД НАПРУГ


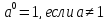
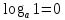
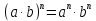
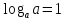
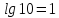
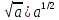
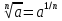
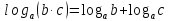
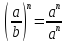
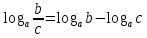
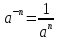
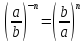
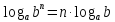
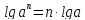
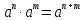
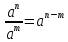
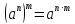
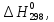
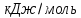
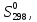
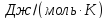
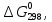
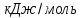
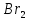
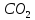
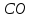
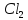
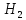
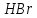
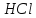
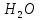
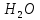
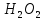

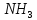
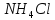

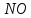
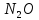
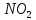

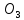
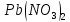
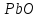
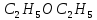
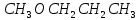
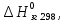
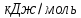
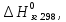
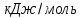
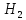
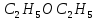
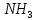
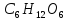 (глюкоза)
(глюкоза)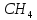
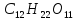 (сахароза)
(сахароза)